Questões Sobre Funções Inorgânicas - Química - 1º ano do ensino médio
Questão 71
Observe o esquema abaixo:
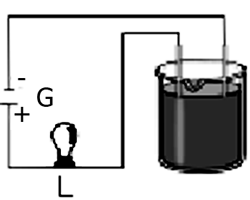
A força de um ácido é medida pelo seu grau de ionização (α), ou seja, pela relação entre o número de moléculas ionizadas e o número total de moléculas dissolvidas. Em qual das soluções, de mesma concentração e na mesma temperatura a lâmpada (L) do esquema apresenta maior brilho?
- A) HF
- B) HNO3
- C) H3PO4
- D) H2S
FAZER COMENTÁRIO- E) H4SiO4
A alternativa correta é letra B
A questão aborda o conceito de força dos ácidos. Para que a lâmpada apresente maior brilho, é necessário uma maior quantidade de íons presentes na solução, para que possa haver uma maior corrente elétrica.Assim, dentre os compostos citados, todos ácidos, o que apresenta maior força é o HNO3 , ácido considerado mais forte devido a regra geral de retirar o número de átomos de hidrogênio do número de átomos de oxigênio, como essa subtração resulta em 2, indica que o ácido é forte.Nos outrso casos, o HF e H2S são hidrácidos fracos pelo fato de o oxigênio e o enxofre possuirem uma alta eletronegatividade.Aplicando a regra de força de oxiácidos para o H3PO4 e H4SiO4, resulta em 1 e 0, indicando que são moderados e fraco, respectivamente.Por isso, quando este está em solução, toda a quantidade de HNO3 presente se ioniza, liberando uma maior quantidade de íons do que os demais ácidos fracos mencionados nas outras alternativas, que se ionizam parcialmente.Portanto a resposta correta é a alternativa B.Questão 72
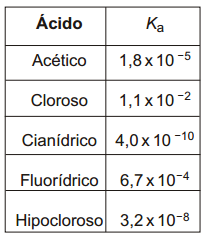 Considerando soluções aquosas contendo a mesma concentração desses ácidos, a ordenação CORRETA de suas forças é
Considerando soluções aquosas contendo a mesma concentração desses ácidos, a ordenação CORRETA de suas forças é- A) cloroso > fluorídrico > acético > hipocloroso > cianídrico.
- B) cianídrico > hipocloroso > acético > fluorídrico > cloroso.
- C) fluorídrico > cianídrico > hipocloroso > acético > cloroso.
FAZER COMENTÁRIO- D) fluorídrico = cianídrico = hipocloroso = acético = cloroso, pois são monopróticos.
A alternativa correta é letra A
Para ácidos, quanto maior a constante de dissociação mais forte é o ácido, pois suas forças intermoleculares serão mais fracas e o ácido se dissociará mais fácil. A sequência, observando a tabela ficará, então: cloroso > fluorídrico > acético > hipocloroso > cianídrico. Portanto, a alternativa correta é a letra A.73) Considere os ácidos oxigenados: HNO2 HClO3 H2SO3 H3PO4 Seus nomes, respectivamente, são acido:
- A) Nitroso, clórico, sulfuroso, fosfórico.
- B) Nítrico, clorídrico, sulfúrico, fosfórico.
- C) Nítrico, hipocloroso, sulfuroso, fosforoso.
- D) Nitroso, perclórico, sulfúrico, fosfórico.
FAZER COMENTÁRIO- E) Nítrico, cloroso, sulfídrico, hipofosforoso,
A alternativa correta é letra A
Oxiácidos são nomeados de acordo com o ácido-padrão de cada elemento.O ácido padrão possui nomenclatura ácido ____ico.Ácidos com um oxigênio a menos que o padrão possui nomenclatura ácido ____oso.Portanto, os nomes dos ácidos são:HNO2: ácido nitroso (Possui um oxigênio a menos que o HNO3: ácido nítrico)HClO3: ácido clórico (ácido padrão)H2SO3: ácido sulfuroso (Possui um oxigênio a menos que o H2SO4: ácido sulfúrico)H3PO4: ácido fosfórico (ácido padrão)74) A transformação química utilizada por Santos-Dumont para produzir o hidrogênio gasoso pode ser representada corretamente por:
- A) Fe (s) + H2SO4 (aq) → FeSO4 (aq) + H2 (g)
- B) Fe (s) + H2SO2 (aq) → FeSO4 (aq) + H2 (g)
- C) Fe (s) + HSO4 (aq) → FeSO4 (aq) + H (g)
- D) Fe (s) + HSO (aq) → FeSO (aq) + H (g)
FAZER COMENTÁRIO- E) Fe (s) + H2SO4 (aq) → FeSO2 (aq) + H2 (g)
A alternativa correta é letra A
Deve-se saber que o ácido sulfúrico tem formula H2SO4, e a reação produz sulfato de ferro FeSO4, portanto A é a alternativa correta.75) O ácido que é classificado como oxiácido, diácido e é formado por átomos de três elementos químicos diferentes é:
- A) H2S
- B) H4P2O7
- C) HCN
- D) H2SO3
FAZER COMENTÁRIO- E) HNO3
A alternativa correta é letra D
Um ácido é classificado como oxiácido se ele possui oxigênio em sua fórmula molecular.Um diácido é aquele que, quando ionizado, libera dois íons H+ para a solução, ou seja, ele deve possuir dois hidrogênios ionizáveis.Dentre as alternativas, o único ácido que pode ser classificado como oxiácido e diácido é H2SO3. Portanto a alternativa D.76) O ácido cianídrico é gás de ação venenosa mais rápida que se conhece: uma concentração de 0,3mg por litro de ar é imediatamente mortal. É o gás usado nos estado americanos, que adotam a pena de morte por câmara de gás. A primeira vítima foi o seu descobridor Carl Wilhelm Scheele, que morreu ao deixar cair um vidro contendo solução de ácido cianídrico, cuja fórmula molecular é:
- A) HCOOH
- B) HCN
- C) HCNS
- D) HCNO
FAZER COMENTÁRIO- E) H4Fe(C
A alternativa correta é letra B
Os hidrácidos são ácidos que contém apenas hidrogênio e um ânion. De acordo com a nomenclatura, a terminação -ídrico é indicada apenas para esse tipo de ácido.Portando o ácido cianídrico é aquele em que o ânion cianeto (CN-) liga-se ao hidrogênio, sem a presença de oxigênio na molécula.Portanto o ácido cianídrico é o HCN, alternativa B.Questão 77
A tabela abaixo apresenta algumas características e aplicações de alguns ácidos: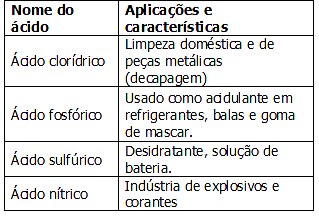 As fórmulas dos ácidos da tabela são respectivamente:
As fórmulas dos ácidos da tabela são respectivamente:- A) HCl, H3PO4, H2SO4, HNO3
- B) HClO, H3PO3, H2SO4, HNO2
- C) HCl, H3PO3, H2SO4, HNO3
- D) HClO2, H4P2O7, H2SO3, HNO2
FAZER COMENTÁRIO- E) HClO, H3PO4, H2SO3, HNO3
A alternativa correta é letra A
A fórmula dos ácidos apresentados na tabela são:ácido clorídrico:HClácido fosfórico: H3PO4ácido sulfúrico: H2SO4ácido nítrico: HNO3Portanto a alternativa correta é a alternativa A.Questão 78
Com base na tabela de graus de ionização apresentada a seguir,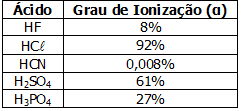 Podemos concluir que o ácido mais forte é:
Podemos concluir que o ácido mais forte é:- A) HF.
- B) HCl.
- C) HCN.
- D) H2SO4.
FAZER COMENTÁRIO- E) H3PO4.
A alternativa correta é letra B
O grau de ionização de um ácido é determinado por:A ionização de um ácido segue a seguinte equação:HX → H+ + X-A força dos ácidos é medida pelo grau de ionização. Quanto maior o grau de ionização, maior será a quantidade de moléculas de H+ no meio e mais forte será o ácido.Dessa forma, o ácido mais forte é o HCl.79) “A adição de bicarbonato de sódio aos anestésicos locais pode reduzir significativamente a dor da injeção. O principal motivo, embora não o único, para que os anestésicos causem dor no local da injeção é, provavelmente, sua característica ácida”.
- A) Os bicarbonatos são bases fortes e, com isso, neutralizam a acidez do anestésico.
- B) O bicarbonato de sódio reduz a dor, porque sua hidrólise formará um ácido mais forte do que o anestésico presente.
- C) Os bicarbonatos são sais que reagem com ácido liberando água e dióxido de carbono.
- D) Os bicarbonatos são ácidos mais fortes do que o ácido clorídrico.
FAZER COMENTÁRIO- E) Os bicarbonatos são sais que neutralizam o ácido presente nos anestésicos, liberando hidrogênio.
A alternativa correta é letra C
O bicarbonato de sódio é um sal que prevêm de uma base forte, o hidróxido de sódio (NaOH) e de um ácido fraco, o ácido carbônico (H2CO3). O bicarbonato, quando reage com um ácido qualquer, libera gás carbônico:HA + HCO3- → H2O + A- + CO2Continua após a publicidade..80) Sobre os compostos HCl, H2SO4, H3BO3 e H2CO3 são feitas as afirmações: I. Todos sofrem ionização quando em meio aquoso, originando íons livres. II. Segundo Arrhenius, todos são ácidos porque, quando em meio aquoso, originam como cátions íons H+. III. Todos são compostos moleculares. IV. De acordo com o grau de ionização, HCl e H2SO4 são ácidos fortes. V. Os compostos H3BO3 e H2CO3 formam soluções aquosas com alta condutividade elétrica. Estão corretas as afirmativas:
- A) I, II, III, IV e V.
- B) I, apenas.
- C) I e II, apenas.
FAZER COMENTÁRIO- D) I, II e III, apenas.
- E) I, II, III e IV, apenas.
« Anterior 1 … 6 7 8 9 Próximo »A alternativa correta é letra E
Vamos analisar cada uma das alternativas. (I) Correto. Todos os compostos citados sofrem ionização em meio aquoso, originando o cátion H+ e seus respectivos ânions. (II) Correto. Todos os compostos citados correspondem à descrição de ácido de Arrhenius. (III) Correto. Todos apresentam ligações covalentes entre seus átomos sendo, portanto, compostos moleculares. (IV) Correto. O HCl e o H2SO4 apresentam alto grau de ionização, sendo considerados ácidos fortes. (V) Incorreto. O H3BO3 e H2CO3 apresentam baixo grau de ionização (ácidos fracos) sendo, portanto, condutores fracos de corrente elétrica. Estão coerentes as assertivas I, II, III e IV, portanto, a resposta correta é a alternativa E.
- B) O bicarbonato de sódio reduz a dor, porque sua hidrólise formará um ácido mais forte do que o anestésico presente.
- B) HCl.
- B) HClO, H3PO3, H2SO4, HNO2
- B) HCN
- B) H4P2O7
- B) Fe (s) + H2SO2 (aq) → FeSO4 (aq) + H2 (g)
- B) Nítrico, clorídrico, sulfúrico, fosfórico.
- B) cianídrico > hipocloroso > acético > fluorídrico > cloroso.
- B) HNO3
