Continua após a publicidade..
O gráfico a seguir relaciona as massas de magnésio que reagem com oxigênio para formar óxido de magnésio.
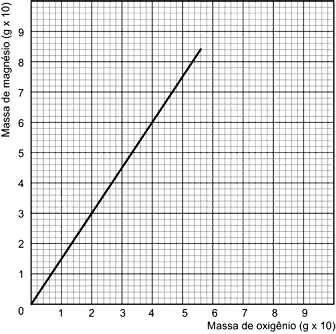
Considere os reagentes em extrema pureza e reação completa. A análise desse gráfico permite afirmar que
- A) as massas de oxigênio e magnésio, envolvidas nas reações, são inversamente proporcionais.
- B) a massa de oxigênio, necessária para reagir com 48 g de magnésio, é de 4,8 g.
- C) usando-se 60 g de magnésio e 60 g de oxigênio, formam-se 100 g de óxido de magnésio, havendo um excesso de 20 g de oxigênio.
- D) usando-se 60 g de magnésio e 60 g de oxigênio, formam-se 120 g de óxido de magnésio.
- E) a proporção entre as massas de magnésio e oxigênio que reagem para formar óxido de magnésio é de 2 de Mg para 3 de O.
Resposta:
A alternativa correta é letra C
A reação de Magnésio com oxigênio é representada por:
Alternativa (a) - Incorreta, pois são diretamente proporcionais, de acordo com os dados do gráfico e com a equação da reação, aumentando a quantidade de massa de magnésio é necessário maior massa de oxigênio para formar o óxido de magnésio.
Alternativa (b) - Incorreta, pois interpolando no gráfico 2x 10g de oxigênio reagem com 3 x 10g de magnésio. A proporção da reação é 2 (Oxigênio): 3(Magnésio). Então 2x10g de O2 –––– 3x10g de Magnésio
X –––– 48g de Magnésio
X=32g de O2
Alternativa (c) - Correta, pois de acordo com a relação
2x10g de O2 –––– 3x10g de Mg
X –––– 60g de Magnésio
X=40g de O2
Para formar 100g de Óxido de Magnésio necessita-se de 60g de Magnésio e de 40g de Oxigênio.
(60g de Magnésio –––– 40g de O2––– 100g de óxido de Magnésio)- (Lei de Lavoisier - conservação das massas), como foi utilizado 60g de Oxigênio 20g está em excesso.
Alternativa (d) - Incorreta, pois como mostrado na alternativa anterior 60g de Magnésio reagem com 40g de oxigênio , adicionando maior quantidade de oxigênio só promove um excesso do mesmo e não maior produção de Óxido de Magnésio.
Alternativa (e) - Incorreta, pois como está demonstrado na alternativa b esta proporção é de 2 de Oxigênio:3 de Magnésio

Deixe um comentário