Questões Sobre Leis Ponderais - Química - 1º ano do ensino médio
11) Pela lei de Proust, a decomposição térmica do carbonato de cálcio (CaCO3), produz, respectivamente, 11g de gás carbônico e 14g de óxido de cálcio (CaO). Com base nesses dados, determine a massa do carbonato de cálcio que pode ser produzida por 8 g de óxido de cálcio:
- A) 25,00g.
- B) 14,29g.
- C) 6,29g.
- D) 10,10g.
FAZER COMENTÁRIO- E) 7,90g.
A alternativa correta é letra B
Pela lei de Proust (lei das proporções definidas), pode-se afirmar que as massas dos reagentes e dos produtos numa reação química, mantém uma proporção em massa constante. Temos então as seguintes relações:Como de 14g de CaO para 8g, houve uma variação na razão de 1,75 (8 = 14/1,75), conforme a lei de proust, o outro produto também deverá ser reduzido na mesma proporção. Ou seja, ao se utilizar 8g de CaO são necessários 6,29g de CO2 (6,29 = 11/1,75).Assim, a massa total de CaCO3 produzida na reação inversa à sua decomposição será de 14,29g, correspondente à soma das massas dos reagentes utilizados.Alternativa correta, B.12) Em um laboratório de química, dois estudantes realizam um experimento com o objetivo de determinar a velocidade da reação apresentada a seguir. MgCO3(s) + 2HCl(aq) → MgCl2(aq) + H2O(l) + CO2(g) Sabendo que a reação ocorre em um sistema aberto, o parâmetro do meio reacional que deverá ser considerado para a determinação da velocidade dessa reação é:
- A) a diminuição da concentração de íons Mg2+
- B) o teor de umidade no interior do sistema
- C) a diminuição da massa total do sistema
- D) a variação da concentração de íons Cl–
FAZER COMENTÁRIO- E) a elevação da pressão do sistema
A alternativa correta é letra C
A reação apresenta a formação de um gás, o CO2. Em um ambiente aberto, esse gás é liberado e a massa total dos produtos é menor do que a massa dos reagentes. Dessa forma, a diminuição da massa total do sistema no decorrer do tempo é um método eficaz de se avaliar a velocidade dessa reação. Portanto, a resposta correta é a alternativa C.Questão 13
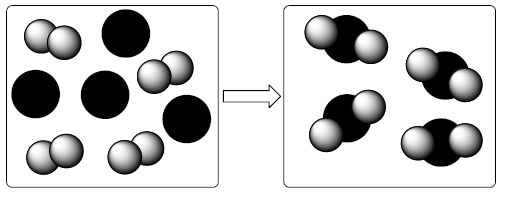 Qual é a equação química que descreve de maneira correta a reação que está esquematizada no desenho?FAZER COMENTÁRIO
Qual é a equação química que descreve de maneira correta a reação que está esquematizada no desenho?FAZER COMENTÁRIO- A) A2 + B
A2B
- B) A2 + 4B
2AB2
- C) 2A + B4
2AB2
- D) A + B2
AB2
- E) A4+ B4
4AB
A alternativa correta é letra A
Resposta A
As esfera correspondem aos átomos e os átomos formam as moléculas desta forma temos 4 átomos do elemento B que será representado na equação como 4B e teremos 4 moléculas formadas por dois átomos de A logo A2. Estes são os reagentes pois estão localizados antes da seta. Após a seta temos o produto resultante que corresponde a 4 moléculas formadas de um átomo de B e dois átomos de A ou seja A2B. Desta forma,
4A2 +4 B4A2B
simplificando a equação:
A2 + BA2B
14) Qualquer que seja a procedência ou processo de separação do NaCl, podemos afirmar que sua composição é sempre 39,32% de sódio e 60,68% de cloro, com base na lei de:
- A) Lavoisier.
- B) Dalton.
- C) Proust.
- D) Richter.
FAZER COMENTÁRIO- E) Avogadro.
A alternativa correta é letra C
Com base na lei de Proust, podemos afirmar que, independentemente do processo utilizado para se obter substâncias puras, a composição em massa de tais substâncias é constante. Ou seja, a massa dos ragentes e produtos numa reação química mantém uma proporção constante.Portanto, qualquer que seja a procedência ou processo de separação do NaCl, podemos afirmar que sua composição é sempre 39,32% de sódio e 60,68% de cloro, com base na lei de Proust.Alternativa correta, C.15) A Lei da Conservação da Massa, enunciada por Lavoisier em 1774, é uma das leis mais importantes das transformações químicas. Ela estabelece que, durante uma transformação química, a soma das massas dos reagentes é igual à soma das massas dos produtos. Esta teoria pode ser explicada, alguns anos mais tarde, pelo modelo atômico de Dalton. Entre as ideias de Dalton, a que oferece a explicação mais apropriada para a Lei da Conservação da Massa de Lavoisier é a de que:
FAZER COMENTÁRIO- A) os átomos não são criados, destruídos ou convertidos em outros átomos durante uma transformação química.
- B) os átomos são constituídos por 3 partículas fundamentais: prótons, nêutrons e elétrons.
- C) todos os átomos de um mesmo elemento são idênticos em todos os aspectos de caracterização.
- D) um elétron em um átomo pode ter somente certas quantidades específicas de energia.
- E) toda a matéria é composta por átomos.
A alternativa correta é letra A
A ideia de Dalton que se relaciona melhor com a Lei da Conservação das Massas, proposta por Lavoisier, é a exposta na alternativa A, pois trata-se da ideia mais próxima de que nada se perde, nada se cria, tudo se transforma, dito por Lavoisier. Portanto, a resposta correta é a alternativa A.16) Querendo verificar a Lei da Conservação das Massas (Lei de Lavoisier), um estudante realizou a reação esquematizada abaixo:
- A) A lei de Lavoisier não é válida nas condições normais de temperatura e pressão.
- B) A lei de Lavoisier não é válida para reações em soluções aquosas.
- C) De acordo com a lei de Lavoisier a massa dos produtos é igual à massa dos reagentes quando estes se encontram no mesmo estado físico.
- D) Para se verificar a lei de Lavoisier é necessário que o sistema seja fechado, o que não ocorreu na experiência realizada.
FAZER COMENTÁRIO- E) Houve excesso de um dos reagentes, o que invalida a lei de Lavoisier.
A alternativa correta é letra D
A Lei de Lavoisier pode ser verificada quando é adotado um sistema fechado, fato que não ocorreu na experiência. Assim, em sistema aberto, há a liberação do gás CO2 para o ambiente, acarretando em uma menor massa medida.Portanto, a resposta correta é a alternativa D.17) Provoca-se reação da mistura formada por 10,0g de hidrogênio e 500g de cloro. Após a reação constata-se a presença de 145g de cloro remanescente, junto com o produto obtido. A massa, em gramas, da substância formada é
- A) 155
- B) 290
- C) 365
- D) 490
FAZER COMENTÁRIO- E) 510
A alternativa correta é letra C
A resolução desta questão está baseada no princípio de conservação da massa (Lei de Lavoisier), assim a massa total inicial é igual a massa total final quando considera-se sistema fechado.Assim,10,0g + 500g = 145g + xx = 365g de produtoPortanto, a resposta correta é a alternativa C.18) “Em um sistema fechado, a massa total dos reagentes é igual à massa total dos produtos”. A afirmação acima está centrada na:
- A) Lei de Lavoisier
- B) Lei de Proust
- C) Lei de Dalton
- D) Lei de Graham
FAZER COMENTÁRIO- E) Lei de Amagat
A alternativa correta é letra A
Na questão, há a apresentação do enunciado da Lei da conservação das massas, também conhecida como Lei de Lavoisier.As demais leis estão relacionadas a proporções definidas em uma reação química (extensão da lei de Lavoisier) , leis relacionadas a comportamento de gases em mistura (Lei de Dalton, Amagat e Graham).Portanto, a resposta correta é a alternativa A.19) Os dados da equação : 25g de A + 75g de B → 40g de C + 60g de D. Estão de acordo com a lei de:
- A) Proust
- B) Avogadro
- C) Lavoisier
- D) Dalton
FAZER COMENTÁRIO- E) Gay-Lussac
A alternativa correta é letra C
Os dados da equação então de acordo com a Lei de Lavoisier, ou lei da conservação das massas. Podemos afirmar isto porque, tal lei afirma que numa reação química, num sistema fechado, não há variação da massa total do sistema. Ou seja, a soma das massas dos reagentes deverá ser igual à soma das massas dos produtos.Tal fato está de acordo com os dados da questão: 100g de reagentes, geram 100g de produtos, não havendo variação da massa total do sistema: 100g antes e 100g depois da reação.Portanto, a alternativa correta é C.Continua após a publicidade..20) ” Na natureza nada se cria, nada se perde, tudo se transforma”. Essa frase é atribuída a Antoine Laurent Lavoisier e se refere à:
- A) Lei das Proporções constantes
- B) lei das proporções múltiplas
- C) lei da conservação das massas
- D) lei volumétrica
FAZER COMENTÁRIO- E) lei da gravidade
« Anterior 1 2A alternativa correta é letra C
Ao se afimar que ” Na natureza nada se cria, nada se perde, tudo se transforma”, o que quer dizer é que não há na natureza eliminação ou criação da matéria, ela apenas pode ser convertida em outras formas.Aplicando-se esse princípio à Química, pode-se dizer que numa reação química, num sistema fechado, a massa dos reagentes é igual à massa dos produtos. Ou seja, a massa total neste sistema permanece constante.Por este motivo, pode-se considerar que tal afirmação se refere à Lei de Conservação das Massas.Alternativa correta, C. - B) lei das proporções múltiplas
- B) Avogadro
- B) Lei de Proust
- B) 290
- B) A lei de Lavoisier não é válida para reações em soluções aquosas.
- B) Dalton.
- B) o teor de umidade no interior do sistema
- B) 14,29g.
