Continua após a publicidade..
A figura mostra modelos de algumas moléculas com ligações covalentes entre seus átomos.
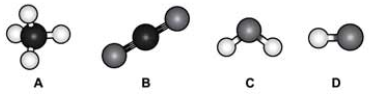
Analise a polaridade dessas moléculas, sabendo que tal propriedade depende da
• diferença de eletronegatividade entre os átomos que estão diretamente ligados. (Nas moléculas apresentadas, átomos de elementos diferentes têm eletronegatividades diferentes.)
• forma geométrica das moléculas.
Observação: Eletronegatividade é a capacidade de um átomo para atrair os elétrons da ligação covalente.
• forma geométrica das moléculas.
Observação: Eletronegatividade é a capacidade de um átomo para atrair os elétrons da ligação covalente.
Dentre essas moléculas, pode-se afirmar que são polares apenas
- A) A e B
- B) A e C
- C) A, C e D
- D) B, C e D
- E) C e D
Resposta:
A alternativa correta é letra E
O efeito da eletronegatividade sobre as moléculas é que os elétrons compartilhados não se distribuem de maneira igual sobre os átomos. Os átomos mais eletronegativos trazem os elétrons para perto de si e acumulam em sua proximidade suas cargas elétricas negativas. Por consequência, os átomos menos eletronegativos ficam mais distantes dos elétrons e na vizinhança deles as cargas positivas tendem a predominar. O resultado é que as moléculas que apresentam essa característica desenvolvem dois polos elétricos, um negativo, próximo ao átomo mais eletronegativo onde os elétrons se concentram, e outro positivo, próximo ao átomo menos eletronegativo, que fica distante dos elétrons. Além disso, existe o efeito da estrutura das moléculas, as moléculas simétricas acabam tendo um momento de dipolo igual a zero, ou seja, são apolares pelo fato das cargas se anularem. Assim, as moléculas representadas por A (CH4) e B (CO2), são simétricas e, portanto, apolares. A molécula representada por D (HCl) é constituída por dois átomos diferentes, sendo o cloro um dos átomos mais eletronegativos, logo, este atrai os elétrons para si, formando um momento dipolar negativo sobre este e o hidrogênio, que fica pobre em elétrons, apresenta um momento dipolar positivo. Pela diferença de cargas, esta é uma molécula polar. Já a molécula C (H2O) é polar pois os elétrons tendem a se concentrar próximos do elemento eletronegativo, o oxigênio, formando uma carga dipolo negativa sobre este e uma carga dipolo positiva sobre os átomos de hidrogênio. Como esta apresenta uma estrutura angular, os momentos de dipolo não se anulam e a molécula apresenta um momento dipolar diferente de zero, sendo polar. Dessa forma, a alternativa que apresenta moléculas polares é a E.

Deixe um comentário