Continua após a publicidade..
As curvas de pressão de vapor, em função da temperatura, para um solvente puro, uma solução concentrada e uma solução diluída são apresentadas na figura a seguir.
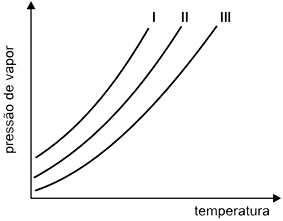
Considerando que as soluções foram preparadas com o mesmo soluto não volátil, pode-se afirmar que as curvas do solvente puro, da solução concentrada e da solução diluída são, respectivamente,
- A) I, II e III
- B) I, III e II
- C) II, III e I
- D) II, I e III
- E) III, II e I
Resposta:
A alternativa correta é letra B
Em uma solução (mistura homogênea de dois compostos), é definido um estado de equilíbrio, tendo propriedades e características próprias. Tais propriedades são chamadas de propriedades coligativas e dependem do número de partículas em solução. Quando é adicionado um soluto na solução inicial, há a mudança neste estado de equilíbrio, alterando as propriedades, já que a quantidade de partículas aumentou. Uma propriedade alterada é a tonoscopia (abaixamento da pressão de vapor), intimamente ligada com a ebulioscopia (aumento da temperatura de fusão). Com isso, pode-se comparar os diagramas, sendo que quanto maior a pressão de vapor, mais volátil é a solução e mais diluída (ou pura) ela é. Neste caso, a curva I trata-se do solvente puro, II é do soluto diluído e III é do solvente concentrado. Portanto, a resposta correta é a alternativa B.

Deixe um comentário