Continua após a publicidade..
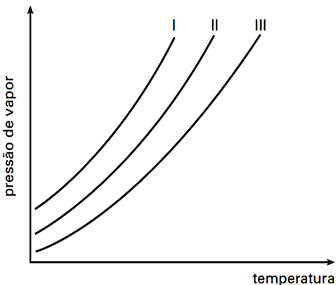
As curvas de pressão de vapor, em função da temperatura, para um solvente puro, uma solução concentrada e uma solução diluída são apresentadas na figura abaixo. Considerando que as soluções foram preparadas com o mesmo soluto não volátil, pode-se afirmar que as curvas do solvente puro, da solução concentrada e da solução diluída são, respectivamente,
As curvas de pressão de vapor, em função da temperatura, para um solvente puro, uma solução concentrada e uma solução diluída são apresentadas na figura abaixo. Considerando que as soluções foram preparadas com o mesmo soluto não volátil, pode-se afirmar que as curvas do solvente puro, da solução concentrada e da solução diluída são, respectivamente,
- A) I, II e III.
- B) I, III e II.
- C) II, III e I.
- D) II, I e III.
- E) III, II e I.
Resposta:
A alternativa correta é letra B
Com adição do soluto puro não volátil, há uma diminuição na pressão de vapor da solução. Assim, analisando as curvas, dada um temperatura, sabe-se que a curva com menor pressão equivale à solução mais concentrada , a curva do meio é a solução diluída e a com maiores pressões é a do solvente puro.
Portanto, a resposta correta é a alternativa B.

Deixe um comentário