Continua após a publicidade..
Para realização de certa atividade experimental, os alunos de uma turma foram organizados em cinco grupos. Cada grupo recebeu uma amostra de um metal que deveria ser identificado e, por isso, os grupos deveriam calcular sua densidade a partir dos valores de massa, determinados em uma balança, e de volume, determinados por meio do deslocamento do volume de água contida em uma proveta. As cinco amostras recebidas pelos grupos apresentavam-se com as superfícies polidas e suas características são indicadas na tabela.
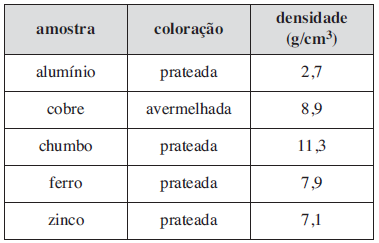
Após constatar que os grupos identificaram corretamente os metais, o professor fez as seguintes observações:
• O metal do grupo 1 tinha coloração avermelhada.
• O metal do grupo 2 tinha menor densidade dentre os metais do experimento.
• O metal do grupo 3 tinha massa = 39,5 g e a proveta utilizada por esse grupo tinha volume de 25 mL com água e de 30 mL com água mais amostra.
• O metal do grupo 4 tinha maior densidade que o do grupo 5.
A amostra recebida pelo grupo 5 foi a do metal
• O metal do grupo 1 tinha coloração avermelhada.
• O metal do grupo 2 tinha menor densidade dentre os metais do experimento.
• O metal do grupo 3 tinha massa = 39,5 g e a proveta utilizada por esse grupo tinha volume de 25 mL com água e de 30 mL com água mais amostra.
• O metal do grupo 4 tinha maior densidade que o do grupo 5.
A amostra recebida pelo grupo 5 foi a do metal
- A) cobre.
- B) zinco.
- C) chumbo.
- D) ferro.
- E) alumínio.
Resposta:
A alternativa correta é letra B
Lembrando que 1cm3 = 1 mL e seguindo a ordem das informações dadas pelos grupos e analisando a tabela mostrada na questão:
Grupo 1: Cobre
Grupo 2: Alumínio
Grupo3: Ferro; onde sua densidade é calculada pela divisão entre a massa (39,5g) pela variação de volume (30 mL- 25 mL = 5 mL) , totalizando uma densidade de 7,9 g/mL.
Assim restaram apenas dois compostos a serem analisados: Chumbo e Zinco.
Grupo 4: Chumbo, pois tem maior densidade dentre os dois compostos restantes (11,9 g /mL)
Grupo 5: Zinco, tem densidade igual a 7,1 g/mL , onde esta é menor do que a do chumbo.
Letra B.
Grupo 1: Cobre
Grupo 2: Alumínio
Grupo3: Ferro; onde sua densidade é calculada pela divisão entre a massa (39,5g) pela variação de volume (30 mL- 25 mL = 5 mL) , totalizando uma densidade de 7,9 g/mL.
Assim restaram apenas dois compostos a serem analisados: Chumbo e Zinco.
Grupo 4: Chumbo, pois tem maior densidade dentre os dois compostos restantes (11,9 g /mL)
Grupo 5: Zinco, tem densidade igual a 7,1 g/mL , onde esta é menor do que a do chumbo.
Letra B.

Deixe um comentário