Continua após a publicidade..
A figura a seguir é um modelo simplificado de um sistema em equilíbrio químico. Este equilíbrio foi atingido ao ocorrer uma transformação química em
solução aquosa.
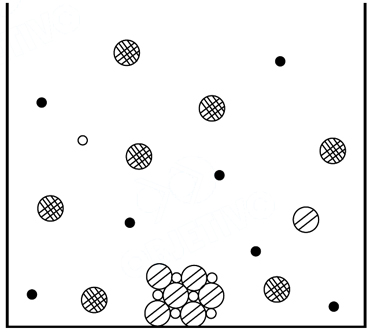
Considere que as soluções dos reagentes iniciais são representadas por
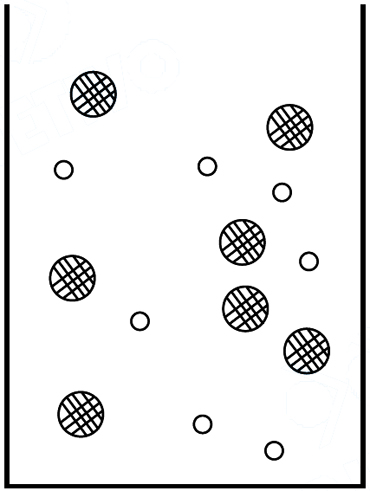
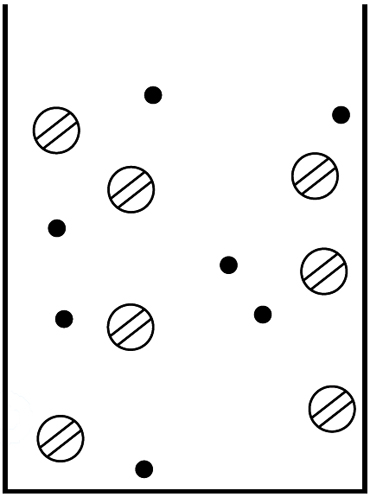
Assim, qual das seguintes equações químicas pode representar, de maneira coerente, tal transformação?
- A) H+ + Cl– + Na+ + OH– ↔ Na+ + Cl– + H2O
- B) 2Na+ + CO32– + 2H++ 2Cl–↔ 2Na+ + 2Cl– + H2O + CO2
- C) Ag+ + NO3– + Na+ + Cl– ↔ AgCl + Na+ + NO3–
- D) Pb2+ + 2NO3– + 2H+ + 2Cl– ↔ PbCl2 + 2H+ + 2NO3–
- E) NH4+ + Cl– + H2O ↔ NH4OH + H+ + Cl–
Resposta:
A alternativa correta é letra C
Para ambos os reagentes a proporção entre eles é de 1:1 nos recipientes.
A mistura resultante mostra a formação de retículo sólido na proporção de íons em 1:1.
Portanto, a alternativa que se adequa a condição da solução apresentada na figura é a que indica a formação de um sólido na proporção iônica de 1:1. Na formação de PbCl2 , temos uma proporção de 1:2 enquanto que na formação de AgCl de 1:1.

Deixe um comentário