Continua após a publicidade..
O sulfato de alumínio é utilizado como clarificante no tratamento de água, pela ação dos íons alumínio que agregam o material em suspensão. No tratamento de 450L de água, adicionaram-se 3,078kg de sulfato de alumínio, sem que houvesse variação de volume. Admitindo-se a completa dissociação do sal, a concentração de íons alumínio, em mol.L-1, é igual a:
- A) 0,02
- B) 0,03
- C) 0,04
- D) 0,05
Resposta:
A alternativa correta é letra C
A fórmula molecular do Sultafo de Alumínio é Al2(SO4)3, 1mol de Sulfato de Alumínio corresponde a :
27g x 2 + 32g x 3 + 16 x 4 x 3 = 342g/mol
Na massa de 3,078 kg, a quantidade de matéria de Al2(SO4)3 é igual a:
3.078g / 342g.mol-1 = 9mol
Para o volume de 450L de solução formada após a adição do sal, a concentração de Al2(SO4)3 é:
9mol / 450L = 0,02mol.L-1
O sulfato de alumínio é um sal que, em solução aquosa, se dissocia segundo a equação:
Al2(SO4)3(s)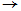 2 Al3+(aq) + 3 SO42-(aq)
2 Al3+(aq) + 3 SO42-(aq)
Como 1 mol de Al2(SO4)3 acarreta a formação de 2 mols de Al3+, tem-se que a concentração de íons Al3+ é igual a:
2 x 0,02 = 0,04mol/L.
Portanto, a alternativa correta é a letra C.

Deixe um comentário