Questões Sobre Tabela Periódica: Propriedades - Química - 1º ano do ensino médio
11) Assinale o elemento considerado de menor eletronegatividade:
- A) silício
- B) oxigênio
- C) fósforo
- D) carbono
FAZER COMENTÁRIO- E) césio
A alternativa correta é letra E
Os elementos de menor eletronegatividade são os metais alcalinos. Dentre as alternativas, todos, exceto o césio, são não-metais ou semimetais.Portanto, a resposta correta é a alternativa E.12) Na Tabela Periódica, o elemento químico bromo (Br) está localizado no 4º período e no grupo 7A (ou 17), logo abaixo do elemento cloro (Cl). Com relação à substância simples bromo (Br2, ponto de fusão -7,2°C, ponto de ebulição 58,8°C sobre pressão de 1 atm), um estudante de química fez as seguintes afirmações:
- A) I.
- B) I e II.
- C) II e III.
- D) I e III.
FAZER COMENTÁRIO- E) III.
A alternativa correta é letra C
I) Falsa, nas condições ambientes o Bromo é líquido e não gasoso.II) Verdadeira, o Br2 se adiciona ao eteno, formando o 1,2-dibromoetanoIII) Verdadeira, o Br2 reage com H2 formando brometo de hidrogênio (ácido bromídrico)Logo C é correta.13) O rubídio (família = 1 e período = 5) é utilizado nas células fotoelétricas e o silício (família = 4 e período = 3), na fabricação de artefatos microeletrônicos. Comparando esses elementos, é correto afirmar que:
FAZER COMENTÁRIO- A) o silício possui maior raio atômico.
- B) o silício apresenta maior afinidade eletrônica.
- C) o rubídio apresenta maior energia de ionização.
- D) o silício é menos eletronegativo.
- E) o rubídio apresenta menor tendência a perder elétrons.
A alternativa correta é letra B
Pelo fato do silício pertencer a uma família mais distante (4 comparada com 1), pode-se dizer que sua tendência em atrair elétrons (afinidade eletrônica) é maior que a do rubídio. Comparando os períodos, tem-se que o número de camadas no átomo de rubídio é maior que no silício, tendo um maior raio atômico.Portanto, a resposta correta é a alternativa B.Questão 14
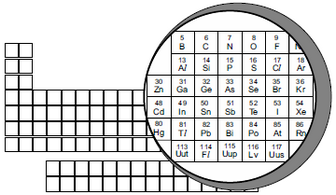 Até o momento, só foi possível sintetizar poucos átomos de fleróvio na forma dos isótopos 288 e 289, pela fusão dos elementos plutônio e cálcio em um acelerador de partículas. Para o fleróvio-289, o processo de síntese pode ser representado pela equação nuclear a seguir:
Até o momento, só foi possível sintetizar poucos átomos de fleróvio na forma dos isótopos 288 e 289, pela fusão dos elementos plutônio e cálcio em um acelerador de partículas. Para o fleróvio-289, o processo de síntese pode ser representado pela equação nuclear a seguir:
Considere as seguintes afirmações:
I. A aparência macroscópica do fleróvio é desconhecida, mas, provavelmente, será a de um sólido metálico.
II. Na formação do fleróvio-288, por processo análogo ao da síntese do fleróvio-289, são liberados 3 prótons.III. No grupo da tabela periódica ao qual pertence o fleróvio, há elementos que formam óxidos covalentes.É correto o que se afirma apenas em:- A) IFAZER COMENTÁRIO
- B) II
- C) III
- D) I e III
- E) II e III
A alternativa correta é letra D
Vamos analisar cada uma das afirmativas. A afirmativa I é verdadeira, pois o elemento fleróvio está no grupo 14 e abaixo do elemento chumbo, que é metal e sólido; espera-se que ele também seja um sólido metálico. A afirmativa II é falsa, pois pela equação apresentada, na formação do fleróvio-288 seriam liberados 4 nêutrons. Por fim, a afirmativa III é verdadeira, pois os elementos carbono e silício formam óxidos covalentes. Estão coerentes as assertivas I e III, portanto, a resposta correta é a alternativa D.15) Um átomo apresenta normalmente 2 elétrons na primeira camada, 8 elétrons na segunda camada, 18 elétrons na terceira camada e 7 elétrons na quarta camada. A família e o período em que se encontra esse elemento são, respectivamente:
- A) família dos halogênios, sétimo período.
- B) família do carbono, quarto período.
- C) família dos halogênios, quarto período.
- D) família dos calcogênios, quarto período.
FAZER COMENTÁRIO- E) família dos calcogênios, sétimo período.
A alternativa correta é letra C
Pelo que está descrito na questão, o elemento possui 35 elétrons e apresenta a seguinte distribuição eletrônica:1s2 2s2 2p6 3s2 3p6 4s2 3d10 4s2 4p5Assim, pode-se dizer que o elemento pertence ao quarto período e a família dos halogênios (sete elétrons de valência).Portanto, a resposta correta é a alternativa C.Questão 16
 (http://chemistry.about.com. Adaptado)Analisando a classificação periódica, mesmo sem conhecer todos os elementos que ela apresenta, é possível afirmar que
(http://chemistry.about.com. Adaptado)Analisando a classificação periódica, mesmo sem conhecer todos os elementos que ela apresenta, é possível afirmar que
- A) os não metais podem ser deformados com golpes de martelo.
- B) os metais alcalino-terrosos são mais densos que os metais alcalinos.
- C) os halogênios, em condições normais de temperatura e pressão, são líquidos coloridos.
- D) o oxigênio e o nitrogênio são gases à temperatura ambiente e seus átomos apresentam seis elétrons na camada mais externa.
FAZER COMENTÁRIO- E) os elementos de uma mesma família da classificação periódica possuem propriedades semelhantes porque eles ocorrem no mesmo lugar da Terra.
A alternativa correta é letra B
Analisando-se cada uma das alternativas, temos:
a) Os não metais podem ser deformados com golpes de martelo. FALSO. A característica de sofrer deformação, ou seja, mudança na forma pela aplicação de uma determinada força, é denominada maleabilidade. Esta propriedade é típica dos elementos classificados como metais.b) Os metais alcalino-terrosos são mais densos que os metais alcalinos. VERDADEIRO. Considerando-se a tabela periódica da forma como está organizada atualmente, a propriedade periódica denominada densidade atômica aumenta da esquerda para a direita até o centro da tabela. Assim, como o grupo dos metais alcalinos-terrosos (família 2A) está mais à direita que o grupo dos metais alcalinos (1A), pode-se afirmar que os alcalinos-terrosos são mais densos que os alcalinos.c) Os halogênios, em condições normais de temperatura e pressão, são líquidos coloridos. FALSO. Nas condições normais de temperatura e pressão apenas o halogênio Bromo encontra-se no estado líquido. Flúor e Cloro são gases e Iodo é um sólido nestas condições.
d) O oxigênio e o nitrogênio são gases à temperatura ambiente e seus átomos apresentam seis elétrons na camada mais externa. FALSO. À temperatura ambiente os elementos oxigênio e nitrogênio são gases, inclusive, são os principais componentes do ar que respiramos. No entanto, estes dois elementos fazem parte de grupos diferentes na tabela periódica, o que indica que possuem diferentes quantidades de elétrons na camada de valência. De fato, o oxigênio (grupo 6A) apresenta 6e- na sua camada de valência, enquanto que o nitrogênio (grupo 5A) possui 5e- na camada de valência.e) os elementos de uma mesma família da classificação periódica possuem propriedades semelhantes porque eles ocorrem no mesmo lugar da Terra. FALSO. As propriedades semelhantes para elementos de uma mesma família (ou grupo) da tabela periódica é devido principalmente ao fato de possuírem a mesma quantidade de elétrons na camada de valência.17) Um átomo do elemento químico x, usado como corante para vidros, possui número de massa igual a 79 e número de nêutrons igual a 45. Considere um elemento y, que possua propriedades químicas semelhantes ao elemento x.
- A) 7.
- B) 9.
- C) 15.
FAZER COMENTÁRIO- D) 16.
A alternativa correta é letra D
O número de massa (A) de um elemento químico é determinado pela soma do seu número de prótons (P) e nêutrons (N). Sendo o número de nêutrons igual a 45, podemos determinar o número atômico, ou número de prótons, do elemento X e identificá-lo na tabela periódica.
Desta forma, identificamos que o elemento X possui número atômico 34, correspondendo ao elemento Selênio, localizado da família 6A ou 16 da tabela periódica.
Para que um elemento químico apresente propriedades químicas (reatividade) semelhantes às de outro elemento, ambos devem pertencer à mesma família, ou coluna, da tabela periódica. Portanto, dentre as opções apresentadas, apenas o elemento de número atômico 16, o oxigênio, pertence à família 6A e terá reatividade semelhante ao Selênio.
Alternativa correta, D.18) Recentemente, quatro novos elementos químicos foram incorporados à tabela de classificação periódica, sendo representados pelos símbolos Uut, Uup, Uus e Uuo. Dentre esses elementos, aquele que apresenta maior energia de ionização é:
FAZER COMENTÁRIO- A) Uut.
- B) Uup.
- C) Uus.
- D) Uuo.
A alternativa correta é letra D
A energia de ionização refere-se a energia necessária para retirar um elétron da camada de valência. Sabendo que o núcleo do átomo é composto de cargas neutras e positivas, sendo que essas últimas atraem os elétrons que estão na eletrosfera e também que a energia de ionização depende também do tamanho do raio do átomo e da força de atração que o núcleo exerce sobre os elétrons é possível concluir que quanto maior o raio do átomo, mais distante do núcleo o elétron de valência está e menor é a atração que o núcleo exerce sobre esse elétron.
Quanto menor é essa atração, menor é a energia necessária para retirar o elétron.
A questão pergunta sobre a maior energia de ionização, aplicando o raciocínio semelhante é possível inferir, após verificar na tabela periódica qual o elemento com menor raio, que o ítem correto é a letra D.
19) As pilhas alcalinas e comuns que contêm compostos de zinco e de manganês podem ir para o lixo comum. Entretanto, certas pilhas e baterias recarregáveis devem ter outro descarte, conforme:“Estabelece que pilhas e baterias que contenham em suas composições chumbo, cádmio, mercúrio e seus compostos tenham os procedimentos de reutilização, reciclagem, tratamento ou disposição final ambientalmente adequados” – Data da legislação: 30.06.1999 – Publicação DOU: 22.07.1999.
FAZER COMENTÁRIO- A) mais tóxicos e bioacumulativos.
- B) menos tóxicos e bioacumulativos.
- C) mais tóxicos e de maior densidade.
- D) menos tóxicos e de maior densidade.
- E) menos tóxicos e de menor densidade.
A alternativa correta é letra A
Chumbo, cádmio e mercúrio são metais pesados tóxicos que se acumulam no organismo, sendo portanto bioacumulativos.Continua após a publicidade..20) Zinco, selênio, ferro e fósforo são sais minerais que participam de inúmeras trocas elétricas e mantêm o cérebro acordado e ativo. Estão presentes em sementes e grãos, raízes e folhas verde-escuras.
- A) apenas I.
- B) apenas II.
- C) apenas III.
- D) apenas I e II.
FAZER COMENTÁRIO- E) apenas II e III
« Anterior 1 2 3 Próximo »A alternativa correta é letra D
Analisando as afirmativas, vemos que somente a I e a II estão corretas, pois: o elemento Selênio encontra-se no grupo 16 tendo 6 elétrons na camada de valência.O selênio encontra-se à direita da tabela e a afinidade eletrônica cresce nos grupos de baixo para cima e nos períodos da esquerda para a direita.Portanto, a alternativa correta é a letra D. - B) apenas II.
- B) 9.
- B) os metais alcalino-terrosos são mais densos que os metais alcalinos.
- B) família do carbono, quarto período.
- B) I e II.
- B) oxigênio
