Questões Sobre Tabela Periódica: Propriedades - Química - 1º ano do ensino médio
21) Em 2014, na Alemanha, um elemento pesado foi confirmado por experimentos com um colisor de partículas e ocupará sua justa posição como Elemento 117 na Tabela Periódica. Bombardeando amostras de berquélio radioativo com átomos de cálcio, pesquisadores criaram átomos com 117 prótons, originando um elemento químico, aproximadamente, 42% mais pesado que o chumbo e com meia-vida relativamente longa. Os físicos apelidaram, temporariamente, o novo integrante da Tabela Periódica como “ununséptio” (Uus), alusão direta ao numeral 117, que é a soma dos 20 prótons do cálcio com os 97 do berquélio.
- A) 294.
- B) 207.
- C) 166.
- D) 117 .
- E) 42.
A alternativa correta é letra A
A massa atômica aproximada do ununséptio é de 294 que corresponde a aproximadamente 42% mais pesado que o chumbo.( Pb: 207)
207+ 42/100 x 207 = 207 + 86,94 = aproximadamente 294
207+ 42/100 x 207 = 207 + 86,94 = aproximadamente 294
Questão 22
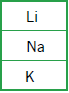
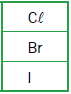
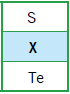
Com base nos critérios desta classificação, a letra X corresponde ao seguinte elemento químico:
- A) O.
- B) As.
- C) Se.
- D) Po.
A alternativa correta é letra C
A tríade que contém o elemento X, as massas atômicas do enxofre (S) e do telúrio (Te) são iguais a 32 e a 127,5, respectivamente.
A média aritmética dessas duas massas equivale a:
A média aritmética dessas duas massas equivale a:
32+127,5/2 = 79,5
Os elementos químicos cujas massas atômicas mais se aproximam de 79,75 são o selênio (Se), com massa igual a 79, e o bromo (Br), com massa igual a 80. Entre esses dois elementos, porém, o selênio é aquele que apresenta propriedades químicas semelhantes ao enxofre e ao telúrio, sendo sua configuração eletrônica da camada de valência igual a ns2np4. Logo, considerando os critérios dessa antiga classificação periódica, a letra X corresponde ao Selênio (Se).
Questão 23
Um aluno estava analisando a Tabela Periódica e encontrou vários conjuntos de três elementos químicos que apresentavam propriedades semelhantes.
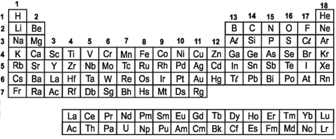
Assinale a alternativa na qual os conjuntos de três elementos ou substâncias elementares estão corretamente associados às propriedades indicadas no quadro abaixo.
- A)

- B)
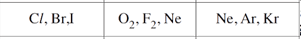
- C)
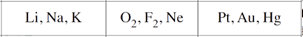
- D)

- E)

A alternativa correta é letra E
Para possuírem números atômicos consecutivos, os elementos ou substâncias elementares devem ser consecutivos em um mesmo período (cada linha horizontal da Tabela Periódica). Isso ocorre para os elementos Pt, Au e Hg (período 6). Para reatividades semelhantes, os elementos ou substâncias elementares devem pertencer a um mesmo grupo (cada coluna da Tabela Periódica). Isso ocorre para Li, Na e K (família dos metais alcalinos). Para mesmo estado físico a temperatura ambiente, tem-se o Ne, Ar e Kr, da família dos gases nobres, que são gases à temperatura ambiente. Portanto, a resposta correta é a alternativa E.
Questão 24
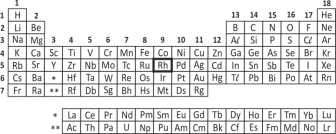
Assinale a alternativa correta a respeito do ródio.
- A) Possui massa atômica menor que a do cobalto (Co).
- B) Apresenta reatividade semelhante à do estrôncio (Sr), característica do 5º período.
- C) É um elemento não metálico.
- D) É uma substância gasosa à temperatura ambiente.
FAZER COMENTÁRIO- E) É uma substância boa condutora de eletricidade.
A alternativa correta é letra E
O ródio é um metal de transição, do quinto período da tabela periódica. Somente pelo fato de ser um metal de transição já sabemos que ele possui boa condutibilidade elétrica e assim sendo, a alternativa E é a correta. Faremos uma breve análise das outras alternativas. (a) O ródio possui massa maior que a do cobalto que é do quarto período. (b) O ródio possui reatividade diferente do estrôncio, que se trata de um metal alcalino terroso, os quais possuem uma reatividade singular. (c) Como já dito anteriormente, o ródio é um metal de transição. E (d) O ródio por se tratar de um metal, está no estado sólido a temperatura ambiente (não que isto seja uma regra válida todos, vide o mercúrio).Questão 25
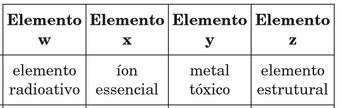
Observe o esquema da Tabela Periódica, no qual estão destacados quatro elementos químicos, identificados pelas letras w, x, y e z.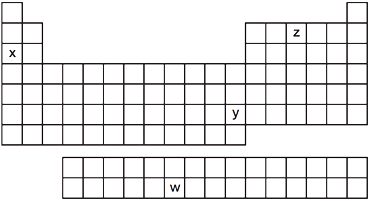 Considerando suas posições na Tabela Periódica, assinale a alternativa que melhor associa esses quatro elementos químicos com as propriedades discutidas acima.FAZER COMENTÁRIO
Considerando suas posições na Tabela Periódica, assinale a alternativa que melhor associa esses quatro elementos químicos com as propriedades discutidas acima.FAZER COMENTÁRIO- A)
- B)

- C)

- D)

- E)

A alternativa correta é letra A
W é um elemento químico de alto número atômico o que o torna instável e portanto radioativo. X pertence à família 1, dos metais alcalinos, os quais formam ligações iônicas e consequentemente íons; esses são importantes à manutenção da vida. Y está localizado nas famílias de metais de transição e seus íons são tóxicos. E Z é um não-metal e possui 5 elétrons na camada de valência, o que aponta ser o nitrogênio, elemento essencial na estrutura das proteínas. Portanto, a resposta correta é a alternativa A.26) Tendo em mente o conceito de eletronegatividade, dentre os elementos abaixo, qual é o mais eletronegativo?
- A) Berílio
- B) Carbono
- C) Nitrogênio
- D) Oxigênio
FAZER COMENTÁRIO- E) Sódio
A alternativa correta é letra D
Eletronegatividade é uma propriedade periódica dos elementos químicos definida como a tendência de um átomo, ao participar de uma ligação química, em atrair elétrons.Dentre os elementos químicos, os três de maior eletronegatividade são Flúor, Oxigênio e Nitrogênio, nesta ordem. Portanto, dentre os elementos citados na questão, o de maior eletronegatividade é o Oxigênio.Alternativa correta, D.27) A Eletronegatividade é uma das principais propriedades dos elementos químicos e indica habilidade em receber elétrons. Os elementos mais eletronegativos da tabela periódica encontram-se:
- A) à direita e abaixo.
- B) à esquerda e abaixo.
- C) à direita e acima.
- D) à esquerda e acima.
FAZER COMENTÁRIO- E) no centro e abaixo.
A alternativa correta é letra C
Os elementos mais eletronegativos são os não-metais, localizados à direita e acima da tabela periódica pelo fato de receberem elétrons para completar a camada de valência.Portanto, a resposta correta é a alternativa C.28) O elemento que pertence ao grupo 2 A, sua família é :
- A) metais alcalinos
- B) gases nobres
- C) halogênios
FAZER COMENTÁRIO- D) metais alcalino-terrosos
- E) calcogênios
A alternativa correta é letra D
Na tabela periódica, as linhas verticais são chamadas grupos, ou família (18 no total). Sendo denominados da seguinte maneira:1- Metais alcalinos;2- Metais alcalino-terrosos;3 à 12- Metais;13- Família do Boro;14- Família do Carbono;15- Família do Nitrogênio;16- Calcogênios;17- Halogênios;18- Gases Nobres.Assim, os elementos do grupo 2A são metais alcalino-terrosos.Portanto, a resposta correta é a alternativa D.Questão 29
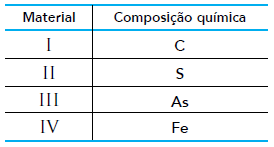 Sabe-se que a condutividade elétrica de um sólido depende do tipo de ligação interatômica existente em sua estrutura. Nos átomos que realizam ligação metálica, os elétrons livres são os responsáveis por essa propriedade.
Sabe-se que a condutividade elétrica de um sólido depende do tipo de ligação interatômica existente em sua estrutura. Nos átomos que realizam ligação metálica, os elétrons livres são os responsáveis por essa propriedade.
Assim, o material mais eficiente para a fabricação do dispositivo é representado pelo seguinte número:FAZER COMENTÁRIO- A) I
- B) II
- C) III
- D) IV
A alternativa correta é letra D
Como o objetivo do dispositivo é conduzir eletricidade, temos que escolher o material que melhor o faz. Os materiais da tabela são: Ferro (Fe), Carbono (C), Enxofre (S) e Arsênio. Dessa tabela o ferro é o melhor condutor de eletricidade já que ele possui os chamados elétrons livres, note que ele é o único metal dessa tabela.Continua após a publicidade..30) Cloro, bromo e iodo são elementos químicos classificados como halogênios. Logo, eles
FAZER COMENTÁRIO- A) localizam-se no mesmo grupo (ou família) da tabela periódica.
- B) estão no mesmo período da tabela periódica.
- C) possuem o mesmo número atômico.
- D) apresentam mesma eletronegatividade.
- E) são isótopos entre si.
A alternativa correta é letra A
Cloro, Bromo e Iodo são elementos químicos considerados como halogênios. Logo, eles localizam-se no mesmo grupo (7A ou 17) da tabela periódica, estão em períodos diferentes e apresentam eletronegatividade diferentes. - B) gases nobres
- B) à esquerda e abaixo.
- B) Carbono
- B) Apresenta reatividade semelhante à do estrôncio (Sr), característica do 5º período.
