Questões Sobre Teoria Atômica-Molecular - Química - 1º ano do ensino médio
11) Sabendo-se que a massa molecular da sacarose – C12H22O11 – é de 342 u.m.a. pode-se afirmar que:
- A) uma molécula de sacarose pesa 342 g.
- B) uma molécula de sacarose pesa 342 mg.
- C) 6,02 x 1023 moléculas de sacarose pesam 342 g.
- D) 342 moléculas de sacarose pesam 6,02 x 1023g.
FAZER COMENTÁRIO- E) 6,02 x 1023 moléculas de sacarose pesam 342 u.m.a.
A alternativa correta é letra C
Sabendo-se que a definição de massa molar é a seguinte: massa total de um mol de moléculas, ou seja, é a massa total de 6,02 x 1023 moléculas do determinado composto. Assim, sabendo que uma molécula de sacarose tem massa igual a 342 u.m.a, pode-se concluir que um mol de moléculas de sacarose tem massa total de 342 g.Portanto, a resposta correta é a alternativa C.12) Um estudante teve a curiosidade de saber qual é a massa de oxigênio puro e qual é o número de átomos existente em um recipiente de 2,46 litros, quando submetido à pressão de 1,0 atm e à temperatura de 27ºC. Para tanto, solicitou sugestões ao professor, de Química, que lhe deu algumas aulas sobre comportamento térmico dos gases e estas informações: esse gás é diatômico e a notação química do átomo de oxigênio é 8O16. Além disso, o professor lhe forneceu os valores de algumas constantes, que estão indicadas no quadro abaixo. (Número de Avogadro = 6,02.1023 e Constante universal dos gases perfeitos = 0,082 atm.litro/mol.kelvin)Se o estudante efetuou todas as operações corretamente, encontrou:
- A) 3,2 g e 6,02.1022átomos.
- B) 3,2 g e 3,01.1022átomos.
- C) 3,2 g e 12,04.1022átomos.
- D) 1,6 g e 6,02.1022átomos.
FAZER COMENTÁRIO- E) 1,6 g e 3,01.1022átomos.
A alternativa correta é letra C
Primeiramente, é necessário encontrar a quantidade de matéria existentes em 2,46 litros nas condições de 1 atm e 27°C.Aplicando a equação de Clapeyron, e substituindo T=27+273 = 300 K, tem-se o seguinte:Como a quantidade de matéria foi de 0,1 mol e como o O2 é diatômico, a quantidade de átomos é o dobro da quantidade de matéria encontrado (número de átomos é de 0,2 mol).Assim, utilizando a constante de Avogadro e a massa molar, encontram-se, respectivamente:Portanto, a resposta correta é a alternativa C.13) Dois óxidos de enxofre foram analisados separadamente, revelando as seguintes porcentagens:
- A) SO2; S2O3.
- B) SO2; SO3.
- C) SO3; SO2.
- D) S2O3; SO2.
FAZER COMENTÁRIO- E) SO2: S2O5.
A alternativa correta é letra C
Nos dois casos, tem-se óxido de enxofre, ou seja, apenas os elementos oxigênio e enxofre estão presentes.Para o óxido I, adotando como base 100g de óxido, temos que 60g é oxigênio e 40g é enxofre. Dividindo cada massa pela massa molar de cada elemento, calcula-se o número de mols de cada um deles:Fazendo a divisão entre os números de mol de oxigênio e enxofre,,chega-se na proporção entre Oxigênio e Enxofre igual a 3. Assim, arredondando para o inteiro mais próximo, chega-se no composto : SO3.De maneira análoga para o Óxido II, tem-se o inteiro mais próximo igual a 2, portanto, o óxido em questão é o SO2.Portanto, a resposta correta é a alternativa C.Questão 14
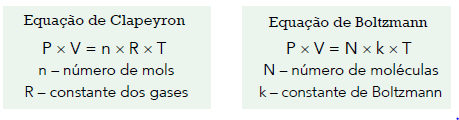 De acordo com essas equações, a razão RK é aproximadamente igual a:FAZER COMENTÁRIO
De acordo com essas equações, a razão RK é aproximadamente igual a:FAZER COMENTÁRIO- A)
- B)
- C)
- D)
A alternativa correta é letra D
Primeiramente vamos escrever as duas equações:(1) PV = nRT
(2) PV = NkTAgora vamos dividir uma pela outra (1)/(2):
PV/PV = nRT/NkT
1 = nR/Nk
R/k = N/n
N - é o número de moléculas
n - é o número de mols
Para calcular o número de moléculas de uma amostra devemos fazer o produto do número de mols que tem tal amostra vezes a constante de Avogadro (6,023 x 1023).
N = 6,023 x 1023 * n
Substituindo esta expressão na fórmula acima:
R/k = ( 6,023 x 1023 * n)/n = 6,023 x 1023
O que é aproximadamente 6 x 1023.
Alternativa D)15) A definição atual de massa atômica de um elemento corresponde a:
- A) 1 x (massa do átomo desse elemento: massa do átomo 12
- B);
- C) 12 x (massa do átomo desse elemento: massa do átomo 12
- D);
FAZER COMENTÁRIO- E) 1/12 x (massa do átomo desse elemento: massa do átomo 12
A alternativa correta é letra C
A definição de massa atômica de um elemento corresponde a quantas vezes a sua massa é maior que a 1/12 da massa do átomo de carbono-12. Isto está citado na alternativa C de uma maneira "encoberta".Portanto, a resposta correta é a alternativa C.Questão 16
 FAZER COMENTÁRIO
FAZER COMENTÁRIO- A) 5 x 1023
- B) 1 x 1023
- C) 5 x 1022
- D) 1 x 1022
- E) 5 x 1021
A alternativa correta é letra C
Para resolver este problema, precisamos saber o volume total de grafite em questão:
Vgrafite = Abase . h
Como o diâmetro da base é de 2 milímetros, o raio será de 1 milímetro e a área da base será:
Convertendo milímetros para metros:
R = 1mm = 10-1 cm
Calculando área da base:
Abase = = . 10-2
Aproximando = 3,14 temos:
Abase = 3,14 . 10-2 cm2
Para encontrar o volume basta multiplicarmos a área da base pela altura:
h = 15 cm
Vgrafite = 3,14 . 10-2 . 15 = 0,471 cm3
Agora que conhecemos o volume de grafite, utilizamos a relação dada no enunciado 2,2g/cm3 para encontrar a massa total de grafite:
Mgrafite = 2,2 . 0,471 = 1,0362 g
Conhecendo a massa, utilizamos a relação 12g/mol, massa molar do carbono, para encontrar a quantidade de mols de carbono presente na massa de grafite:
Qmols = = 0,08635 mols
Finalmente, utilizamos a constante de Avogadro para converter o número de mols em número de átomos:
N átomos = 0,08635 . 6 . 1023 = 0,5181 . 1023
N átomos = 5,181 . 1022
Portanto, a alternativa que mais se aproxima do número de átomos presente nessa grafite é a letra c.Questão 17
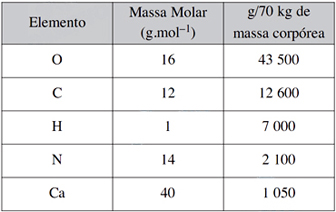 Com base nos dados apresentados, pode-se concluir:FAZER COMENTÁRIO
Com base nos dados apresentados, pode-se concluir:FAZER COMENTÁRIO- A) o número de átomos de N no corpo de um adulto corresponde a 30% do número de átomos de H.
- B) H é o elemento que, isoladamente, contribui com o maior número de átomos.
- C) por ter maior massa molar, o elemento cálcio é o mais abundante no corpo humano.
- D) não é possível saber qual elemento é o mais abundante no corpo humano, pois todos formam moléculas.
- E) os átomos do elemento C, presentes no corpo humano, são diferentes daqueles átomos do elemento C que formam o CO2.
A alternativa correta é letra B
Para a resolução da questão, devemos calcular a quantidade em mols de cada elemento químico. Isto pode ser feito através da fórmula:onde n é o numero de mols, m é a massa fornecida na tabela e M é a massa molar. Efetuando-se os cálculos temos:O = 2.718,75 molsC = 1.050 molsH = 7.000 molsN = 150 molsCa = 26,25 molsSabendo que o número de átomos é proporcional à quantidade de mols, podemos concluir que é elemento hidrogênio (H) é o que mais contribui em número de átomos. Portanto, a resposta correta é a alternativa B.18) As substâncias indicadas abaixo são de grande importância como fertilizantes porque fornecem nitrogênio. Indique qual delas é potencialmente a mais rica fonte desse elemento.
- A) uréia, CO(NH2)2.
- B) nitrato de amônio, NH4NO3.
- C) sulfato de amônio, (NH4)2SO4.
- D) guanidina, HCN(NH2)2.
FAZER COMENTÁRIO- E) nitrato de potássio, KNO3.
A alternativa correta é letra D
A Massa Molar de cada composto acima é, respectivamente, 60, 80, 132, 59 e 101 g/mol. Porém, a massa de nitrogênio (por mol) de cada é respectivamente, 28, 28, 28, 42 e 14 g.Portanto, para descobrir qual deles é mais rico em nitrogênio, é preciso calcular a relação massa de nitrogênio por massa molar:Logo, aquele que obtiver a maior razão é o composto mais rico em nitrogênio por grama de massa. Como podemos observar os resultados, a guanidina é a potencialmente mais rica.Alternativa D.19) O cobre consiste em dois isótopos com massa 62,96u e 64,96u e abundância isotópica de 70,5% e 29,5%, respectivamente. A massa atômica do cobre é:
- A) 63,96u.
- B) 63,00u.
- C) 63,80u.
- D) 62,55u.
FAZER COMENTÁRIO- E) 63,55u.
A alternativa correta é letra E
A massa atômica do cobre é determinada pela média ponderada da abundância de cada isótopo, dessa forma, tem-se:Portanto, a resposta correta é a alterativa E.Continua após a publicidade..Questão 20
 A prata é um metal que apresenta excelente ductilidade e a maior condutividade elétrica dentre todos os elementos químicos. Um fio de prata possui 10m de comprimento (l) e área de secção transversal (A) de 2,0 x 10–7 m2.
A prata é um metal que apresenta excelente ductilidade e a maior condutividade elétrica dentre todos os elementos químicos. Um fio de prata possui 10m de comprimento (l) e área de secção transversal (A) de 2,0 x 10–7 m2.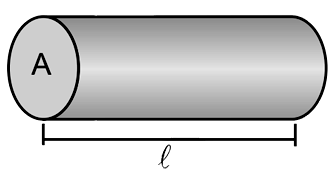 Considerando a densidade da prata igual a 10,5 g/cm3, a massa molar igual a 108 g/mol e a constante de Avogadro igual a 6,0 x 1023 mol–1, o número aproximado de átomos de prata nesse fio será
Considerando a densidade da prata igual a 10,5 g/cm3, a massa molar igual a 108 g/mol e a constante de Avogadro igual a 6,0 x 1023 mol–1, o número aproximado de átomos de prata nesse fio será- A) 1,2 x 1022.
- B) 1,2 x 1023.
- C) 1,2 x 1020.
- D) 1,2 x 1017.
FAZER COMENTÁRIO- E) 6,0 x 1023.
« Anterior 1 2 3 4 5 Próximo »A alternativa correta é letra B
Primeiramente, é necessário conhecer o volume de prata contido no fio, para isso, tem-se:Encontrado o volume, determina-se a quantidade de átomos de prata através do uso da densidade, massa molar e constante de Avogadro, como é mostrado a seguir:Portanto, a resposta correta é a alternativa B. - B) 1,2 x 1023.
- B) 63,00u.
- B) nitrato de amônio, NH4NO3.
- B) SO2; SO3.
- B) 3,2 g e 3,01.1022átomos.
- B) uma molécula de sacarose pesa 342 mg.
