Questões Sobre Teoria Atômica-Molecular - Química - 1º ano do ensino médio
21) Sabe-se que, quando uma pessoa fuma um cigarro, pode inalar de 0,1 até 0,2mg de nicotina. Foram descobertos em laboratório que cada miligrama de nicotina contém 74,00% de carbono, 8,65% de hidrogênio e 17,35% de nitrogênio. A fórmula mínima da nicotina é:
- A) C6H7N.
- B) C5H7N.
- C) C10H12N.
- D) C5H6N2.
FAZER COMENTÁRIO- E) C4H3N2.
A alternativa correta é letra B
Adotando como base 100g, tem-se, em quantidades molares para cada elemento os seguintes valores:Divindo todos os valores pela menor quantidade que é 1,24 e arredondando para o natural mais próximo, tem-se:Dessa forma, a fórmula mínima da nicotina é igual a C5H7N.Portanto, a resposta correta é a alternativa B.22) Usando-se a técnica de espectrometria de massas, é possível determinar a razão 13C/12C no vinho espumante e em suas bolhas de gás carbônico. Dependendo do valor dessa razão, é possível afirmar se o açúcar e o gás carbônico foram formados somente pelo processo natural de fermentação ou se houve adição desses compostos durante o processo de produção do vinho espumante.
- A) Apenas I.
- B) Apenas II.
- C) Apenas III.
- D) Apenas I e II.
FAZER COMENTÁRIO- E) Apenas II e III.
A alternativa correta é letra A
As espécies químicas 13C e 12C são denominadas isótopos. Isótopos são átomos de um mesmo elemento químico que apresentam diferentes massas atômicas. Sendo átomos de um mesmo elemento, apresentam o mesmo número de prótons, variando apenas no número de nêutrons. Sendo assim, podemos analisar cada uma das proposições: I, CORRETO. Ambas as espécies apresentam o mesmo número atômico (número de prótons), logo, ocupam a mesma posição na tabela periódica. II, ERRADO. A espécie 13C é mais densa que 12C, porque ela apresenta um nêutron a mais. Ambas apresentam o mesmo número de prótons. III, ERRADO. Considerando-se os átomos neutros, ambas as espécies apresentam o mesmo número de elétrons, pois apresentam o mesmo número de prótons. As eletronegatividades entre as espécies não deve variar. Desta forma, a resposta correta é a A.Questão 23
 Dados – M (g mol-1 ): H = 1; C = 12; N = 14; O = 16.Qual é o valor da massa molar (em g mol-1 ) desse composto?FAZER COMENTÁRIO
Dados – M (g mol-1 ): H = 1; C = 12; N = 14; O = 16.Qual é o valor da massa molar (em g mol-1 ) desse composto?FAZER COMENTÁRIO- A) 169.
- B) 174.
- C) 177.
- D) 183.
- E) 187.
A alternativa correta é letra D
Somando os elementos presentes na molécula a seguinte fórmula molecular é obtida C9H13NO3. Para saber a massa molar (em g mol-1 ) desse composto é necessário utilizar os dados que a questão expõe fazendo a multiplicação das quantidades de C,H,N e O pelas suas respectivas massas molares em seguida somando o resultado.
Letra D.24) Desde o século XIX, uma das questões mais preocupantes para os químicos era a definição do peso dos átomos. Atualmente, as massas atômicas dos elementos químicos são representadas, em sua maior parte, por números fracionários. O elemento magnésio, por exemplo, apresenta massa atômica aproximada de 24,3 unidades de massa atômica.
- A) os átomos de magnésio podem apresentar um número de elétrons diferente do número de prótons.
- B) o número de nêutrons é sempre maior que o número de prótons nos átomos de magnésio.
- C) o elemento magnésio pode originar diferentes variedades alotrópicas.
- D) a massa de um átomo de magnésio é relativamente 24,3 vezes maior que a de um átomo do isótopo 12 do carbono.
FAZER COMENTÁRIO- E) o elemento magnésio é formado por uma mistura de isótopos naturais que apresentam massas atômicas diferentes.
A alternativa correta é letra E
O número de massa de qualquer elemento químico é definido pela soma de prótons e nêutrons que o átomo desse elemento possui. O magnésio, por exemplo, possui 12 prótons e, normalmente, 12 nêutrons. Logo, seu número de massa é 24 u (unidades de massa). Entretanto, existem na natureza outros tipos de átomo de magnésio, com 14 ou 15 nêutrons. Esses átomos que possuem o mesmo número de prótons (sendo, portanto do mesmo elemento) mas diferentes números de nêutrons e de massa atômica são os chamados isótopos. A massa atômica do elemento, encontrada na tabela periódica, é a média ponderada do número de massa de todos os isótopos deste. Portanto, a resposta correta é a alternativa E.25) O número de moléculas de sacarose, presente numa embalagem que contém 5,7 g desse açúcar, é igual a
- A) 1,0 .1022
- B) 6,0 . 1023
- C) 1,0 . 1024
- D) 2,0 . 1026
FAZER COMENTÁRIO- E) 1,9 . 1020
A alternativa correta é letra A
Primeiramente, a quantidade molar na amostra de sacarose é a seguinte:n = 5,7g / 342 g/moln = 5,7/342 molPara encontrar o total de moléculas, basta multiplicar n pela constante de Avogadro:Total de moléculas = 6.1023 x 5,7/342Total de moléculas = 1,0 x 1022Portanto, a resposta correta é a alternativa A.26) Uma das metas do Conselho Nacional do Meio Ambiente é que os carros novos emitam 2,0 g de monóxido de carbono (CO) por quilômetro. Nessas condições, quantas moléculas do gás serão emitidas, aproximadamente, por um carro ao percorrer 15 km?
- A) 2,0.
- B) 3,0.
- C) 3,2 x 1023.
- D) 6,4 x 1023.
FAZER COMENTÁRIO- E) 9,0 x 1023.
A alternativa correta é letra D
No total de 15 km tem-se o total de 30 g de CO, isso equivale a um total de n moles de CO:Agora, multiplicando n pela constante de Avogadro, tem-se um total de 6,4 x 1023 moléculas de CO.Portanto, a resposta correta é a alternativa D.27) O sulfato de cobre é um dos componentes da “calda bordalesa”, mistura muito utilizada na agricultura para combater as doenças fúngicas em hortaliças e árvores frutíferas.
- A) 36%
- B) 56%
- C) 11%
- D) 5%
FAZER COMENTÁRIO- E) 1%
A alternativa correta é letra A
Primeiramente, sabendo que a massa molar de cada elemento é a seguinte:Cu: 63,5 g/molO : 16 g/molS : 32 g/molH : 1 g/molAssim, a massa molar do CuSO4.5H2O é de 249,5 g/mol, e a massa total de água na molécula é de5x18 = 90 g/mol.Assim, a porcentagem de água na molécula é de 36%.Portanto, a resposta correta é a alternativa A.28) Cientistas podem ter encontrado o bóson de Higgs, a “partícula de Deus”
FAZER COMENTÁRIO- A) Cu.
- B) I.
- C) Mo.
- D) Pb.
A alternativa correta é letra A
A unidade de massa atômica (u.m.a.) é bem próxima ao valor da massa do hidrogênio. Como o hidrogênio é constituído apenas por um próton e por um elétron, a u.m.a. também é bem próxima ao valor da massa do próton.
Consultando-se a tabela de classificação periódica, observa-se que a massa atômica do cobre (Cu) é igual a 63,5 u.m.a., ou seja, corresponde a cerca de 63,5 vezes a massa do próton, ou a cerca de metade da massa do bóson de Higgs, cuja massa vale 126 vezes a massa do próton.29) A glicose é um açúcar de fórmula molecular C6H12O6. O número de moléculas existentes em 1 kg de glicose é aproximadamente:
- A) 3,33 . 1024
- B) 5,56 . 1024
- C) 3,33 . 10-24
- D) 6,02 . 1023
FAZER COMENTÁRIO- E) 4,38 . 1024
A alternativa correta é letra A
A massa molar da glicose pode ser determinada da seguinte maneira:massa de C = 6 x 12 g/mol = 72 g/molmassa de H = 12 x 1 g/mol = 12 g/molmassa de O = 6 x 16 g/mol = 96 g/molCom isso,descobrimos que a massa molar da glicose é igual a 180 g/mol.Assim sendo, um quilo de glicose equivalerá a uma quantidade molar de 1000g/180g = 5,56 moles.Como sabemos que em 1 mol de glicose existem 6,0.1023 moléculas (constante de Avogadro), utilizando uma simples regra de três, chegaremos que, em 5,56 moles de glicose, existirá um total de 3,33.1024 moléculas. Portanto, a resposta correta é a alternativa A.Continua após a publicidade..Questão 30
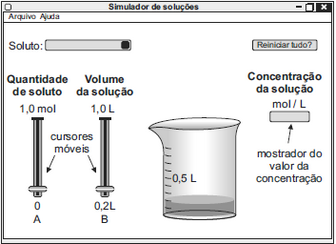 O estudante escolheu um soluto e moveu os cursores A e B até que o mostrador de concentração indicasse o valor 0,50 moI/L. Quando esse valor foi atingido, os cursores A e B poderiam estar como mostrado emFAZER COMENTÁRIO
O estudante escolheu um soluto e moveu os cursores A e B até que o mostrador de concentração indicasse o valor 0,50 moI/L. Quando esse valor foi atingido, os cursores A e B poderiam estar como mostrado emFAZER COMENTÁRIO- A)
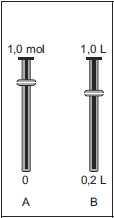
- B)
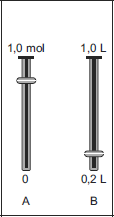
- C)
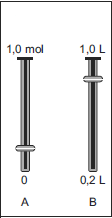
- D)
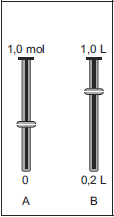
- E)
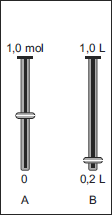
A alternativa correta é letra D
Para que a concentração final seja 0,5 M, deve-se escolher um mostrador que relacione uma quantidade de soluto menor que a de solvente e cujos valores sejam proporcionais a 1:2, no caso aproximadamente 0,4 de soluto : 0,8 de solvente.

- B) 5,56 . 1024
- B) 56%
- B) 3,0.
- B) 6,0 . 1023
- B) o número de nêutrons é sempre maior que o número de prótons nos átomos de magnésio.
- B) Apenas II.
- B) C5H7N.
