Questões Sobre Teoria Atômica-Molecular - Química - 1º ano do ensino médio
31) Considere amostras de 1 g de cada uma das seguintes substâncias: eteno (C2H4), monóxido de carbono (CO) e nitrogênio (N2). Essas três amostras
- A) apresentam a mesma quantidade, em mol, de moléculas.
- B) apresentam a mesma quantidade, em mol, de átomos.
- C) apresentam ligações covalentes polares.
- D) são de substâncias isômeras.
- E) são de substâncias simples.
A alternativa correta é letra A
Mol determina a quantidade, seja esta de moléculas, átomos, íons ou elétrons. A molécula é a menor porção de uma substância que apresenta todas as suas propriedades físicas e químicas sendo formadas por dois ou mais átomos. Os átomos que constituem as moléculas podem ser do mesmo tipo como o N2 ou de tipos diferentes, como C2H4 e CO. É possível calcular a massa de uma molécula realizando a soma das massas atômicas de cada átomo que forma a respectiva molécula. O resultado é denominado Massa Molecular (MM). Primeiro é preciso saber qual é a massa atômica de cada átomo, que é dada pela Tabela Periódica dos elementos. A massa molecular será a soma das massas atômicas dos átomos.
A massa atômica disponível na tabela periódica para cada elemento envolvido nessa questão:
C – 12 u.m.a. (unidade por massa atômica)
O – 16 u.m.a. (unidade por massa atômica)
H – 1 u.m.a. (unidade por massa atômica)
N – 14 u.m.a. (unidade por massa atômica)
Com isso, temos a massa molar (massa de substância contida em 1 mol da mesma)
C2H4 = (2 x 12) + (4 x 1) = 28 g/mol
CO= (1 x 12) + (1 x 16) = 28 g/mol
N2 = (2 x 14) = 28 g/mol
Se temos 1g de cada substância logo o número de mols para as três será o mesmo:
n = 1g / (28g.mol-1) = 0,036 mols
E por isso a alternativa A está correta, pois apresentam o mesmo número de mols de moléculas.
Em relação às outras alternativas:
Não possuem o mesmo número de mols de átomos, pois as moléculas apresentadas apresentam quantidade de átomos que as compõem diferentes.
A ligação covalente é caracterizada pelo compartilhamento de elétrons, ocasionando uma atração mútua e mantendo a molécula unida. A polaridade da ligação está relacionada ao elemento que realiza a ligação. Sendo a ligação realizada por dois elementos iguais, como no caso do N2, então não há diferença de eletronegatividade e a molécula é apolar.
Isômeros apresentam a mesma formula molecular, apesar de serem diferentes. Como vemos, não é o caso das substâncias apresentadas.
Substâncias simples são formadas por um único tipo de elemento, e das que foram apresentadas na questão há apenas uma.
A massa atômica disponível na tabela periódica para cada elemento envolvido nessa questão:
C – 12 u.m.a. (unidade por massa atômica)
O – 16 u.m.a. (unidade por massa atômica)
H – 1 u.m.a. (unidade por massa atômica)
N – 14 u.m.a. (unidade por massa atômica)
Com isso, temos a massa molar (massa de substância contida em 1 mol da mesma)
C2H4 = (2 x 12) + (4 x 1) = 28 g/mol
CO= (1 x 12) + (1 x 16) = 28 g/mol
N2 = (2 x 14) = 28 g/mol
Se temos 1g de cada substância logo o número de mols para as três será o mesmo:
n = 1g / (28g.mol-1) = 0,036 mols
E por isso a alternativa A está correta, pois apresentam o mesmo número de mols de moléculas.
Em relação às outras alternativas:
Não possuem o mesmo número de mols de átomos, pois as moléculas apresentadas apresentam quantidade de átomos que as compõem diferentes.
A ligação covalente é caracterizada pelo compartilhamento de elétrons, ocasionando uma atração mútua e mantendo a molécula unida. A polaridade da ligação está relacionada ao elemento que realiza a ligação. Sendo a ligação realizada por dois elementos iguais, como no caso do N2, então não há diferença de eletronegatividade e a molécula é apolar.
Isômeros apresentam a mesma formula molecular, apesar de serem diferentes. Como vemos, não é o caso das substâncias apresentadas.
Substâncias simples são formadas por um único tipo de elemento, e das que foram apresentadas na questão há apenas uma.
32) O número de átomos de magnésio em 6g desse elemento é igual a
- A) ¼ de átomo.
- B) 24 x 1023 átomos.
- C) ¼ x 6x 1023 átomos.
- D) 6,0 x 1023 átomos.
FAZER COMENTÁRIO- E) 6 átomos.
A alternativa correta é letra C
Primeiramente, é necessário encontrar a quantidade molar de magnésio. Para isso, basta dividir a massa de magnésio pela sua massa molar:Agora, multiplicando 0,25 pela constante de Avogadro, tem-se um valor total de moléculas igual a 1/4 x 6x1023 ou 1,5 x 1023.Portanto, a reposta correta é a alternativa C.33) Entre os vários íons presentes em 200 mililitros de água de coco há aproximadamente 320 mg de potássio, 40 mg de cálcio e 40 mg de sódio. Assim, ao beber água de coco, uma pessoa ingere quantidades diferentes desses íons, que, em termos de massa, obedecem à sequência: potássio > sódio = cálcio. No entanto, se as quantidades ingeridas fossem expressas em mol, a sequência seria:
- A) potássio > cálcio = sódio.
- B) cálcio = sódio > potássio.
- C) potássio > sódio > cálcio.
FAZER COMENTÁRIO- D) cálcio > potássio > sódio.
A alternativa correta é letra C
Para cada um dos elementos, vamos calcular o número de mols ingeridos por uma pessoa ao ingerir 200 mL de água de coco:
Potássio (K):Cálcio (Ca):Sódio (Na):Assim, a ordem decrescente em mol para esses elementos é, conforme solicitado no enunciado, é: potássio > sódio > cálcio. Portanto, a resposta correta é a alternativa C.Questão 34
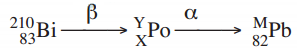 O número atômico X, o número de massa Y e o número de massa M, respectivamente, são:O número atômico X, o número de massa Y e o número de massa M, respectivamente, são:
O número atômico X, o número de massa Y e o número de massa M, respectivamente, são:O número atômico X, o número de massa Y e o número de massa M, respectivamente, são:- A) 82, 207, 210.
- B) 83, 206, 206.
- C) 83, 210, 210.
- D) 84, 210, 206.
FAZER COMENTÁRIO- E) 84, 207, 208.
A alternativa correta é letra D
Para resolver essa questão é necessário conhecer as características das partículas alfa e beta. A partícula alfa possui massa 4 e número atômico 2, já a partícula beta possui massa 0 e número atômico de -1. Assim, o bismuto quando emite uma partícula beta continua com sua massa constante (isso por que a massa da partícula beta é 0) e tem seu número atômico variando da seguinte forma: 83-(-1)=84 (o primeiro sinal negativo vem do fato do bismuto estar perdendo essa partícula beta e o segundo sinal negativo é da carga da partícula beta). Continuando o decaimento, o polônio ao emitir uma partícula alfa tem sua massa diminuída em 4, ou seja, 210-4=206 e tem seu número atômico diminuído em 2, 84-2=82. Assim, o X (número atômico do polônio)=84, o Y (número de massa do polônio)=210 e M (número de massa do chumbo)= 206. Logo a resposta é a letra D.35) Em 3,0 mol de H2SO4 e 5,0 mol de Br2 há, respectivamente:
- A) 1,8. 1024 moléculas e 3,0. 1024 moléculas.
- B) 3,0. 1023 moléculas e 5,0. 1023 moléculas.
- C) 1,8. 1024 moléculas e 3,0. 1024 átomos.
- D) 1,8. 1024 átomos e 3,01. 1024 átomos.
FAZER COMENTÁRIO- E) 6,0. 1023 moléculas e 12. 1023 moléculas.
A alternativa correta é letra A
Utilizando a constante de Avogadro igual a 6,0.1023 moléculas por mol, tem-se:Portanto, a resposta correta é a alternativa A.36) A fórmula do gás sulfídrico é H2S. Portanto, em qualquer amostra pura desse gás há: (Dados: H = 1 e S = 32).
- A) 1 g de hidrogênio para 16 g de enxofre.
- B) 2 g de hidrogênio para 1 g de enxofre.
- C) 100 átomos de hidrogênio para 200 átomos de enxofre.
- D) 6,02.1023átomos de hidrogênio para 6,02 • 1023átomos de enxofre.
FAZER COMENTÁRIO- E) 20% de hidrogênio em massa.
A alternativa correta é letra A
Com os valores de massa molar dados acima, pode-se concluir que a massa molar do H2S é de 34 g/mol.Usando a fração mássica de cada elemento, baseado na suas massas molares correspondentes, chega-se que:Fração mássica do enxofre : 32/34Fração mássica do hidrogênio: 2/34Com isso, para cada 32 g de enxofre, necessita-se de 2 g de hidrogênio, ou do mesmo modo, necessita-se de 1 g de hidrogênio para cada 16 g de enxofre.Portanto, a resposta correta é a alternativa A.37) 1,8 • 1023 moléculas de uma substância A têm massa igual a 18,0 g. A massa molar de A, em g/mol, vale:
- A) 18,0.
- B) 60,0.
- C) 75,0.
- D) 90,0.
FAZER COMENTÁRIO- E) 120,0.
A alternativa correta é letra B
Primeiramente, é necessário saber quantos moles equivalem a 1,8 • 1023 moléculas:Para a massa molar da substância A, faz-se o seguinte:Portanto, a resposta correta é a alternativa B.38) Em 3,0 mols de H2SO4 e 5 mols de Br2 há, respectivamente,
- A) 1,8 x 1024 moléculas e 3,01 x 1024 moléculas;
- B) 3,0 x 1023 moléculas e 5,0 x 1023 moléculas;
- C) 1,8 x 1024 moléculas e 3,01 x 1023 moléculas;
- D) 1,8 x 1024 átomos e 3,01 x 1024 moléculas;
FAZER COMENTÁRIO- E) 1,8 x 1024 moléculas e 5,0 x 1024 átomos;
A alternativa correta é letra A
Utilizando a constante de Avogadro igual a 6,02.1023 moléculas por mol, tem-se:Portanto, a resposta correta é a alternativa A.39) Três mols de benzeno (C6H6) contêm uma massa de:
- A) 78 g
- B) 39 g
- C) 156 g
- D) 72 g
FAZER COMENTÁRIO- E) 234 g
A alternativa correta é letra E
A massa molar do benzeno é calculada da seguinte maneira:MM(benzeno) = 6.12 + 6.1 = 78 g/molDessa forma, três moles equivalem a 3.78 = 234 g de benzeno.Portanto, a resposta correta é a alternativa E.Continua após a publicidade..40) Assinale a alternativa que indica o número de átomos existentes em 4 mols de magnésio:
- A) 24. 1024
- B) 2,4. 1024
- C) 2,4. 1022
- D) 6. 1023
FAZER COMENTÁRIO- E) 6. 1024
« Anterior 1 2 3 4 5 Próximo »A alternativa correta é letra B
Para saber a quantidade de átomos existentes em 4 mols de magnésio, fazemos o seguinte cálculo:Q = Constante de Avogadro . n,sendo Q a quantidade total de átomos e n o número de mols.Assim, tem-se:Q = 6,0 . 1023. 4Q = 24 . 1023 = 2,4 . 1024Portanto, a resposta correta é a alternativa B. - B) 2,4. 1024
- B) 39 g
- B) 3,0 x 1023 moléculas e 5,0 x 1023 moléculas;
- B) 60,0.
- B) 2 g de hidrogênio para 1 g de enxofre.
- B) 3,0. 1023 moléculas e 5,0. 1023 moléculas.
- B) 83, 206, 206.
- B) cálcio = sódio > potássio.
- B) 24 x 1023 átomos.
