Continua após a publicidade..
O gráfico mostra a variação de temperatura em função da quantidade de calor absorvida pelas substâncias A e B de massa mA = 150 g e mB = 100 g.
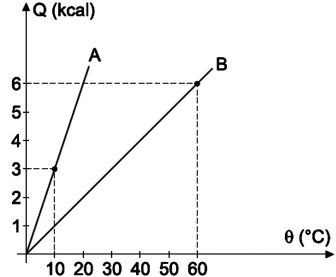
Misturando-se as duas substâncias: A (mA= 150 g e θA = 60 °C) e B (mB = 100 g e θB = 40 °C), a temperatura final de equilíbrio será:
- A) 55 °C.
- B) 50 °C.
- C) 45 °C.
- D) 60 °C.
- E) 40 °C.
Resposta:
A alternativa correta é letra A
A quantidade de calor, é dada pela equação:
Quando ocorre o equilíbrio térmico, as quantidades de calor finais são iguais, logo, só precisamos igualar as duas equações das substância A e B:
Agora vamos resolver as equações para encontrar o calor específico (c) de A e de B.
Calor sensível de A (utilizando dados do gráfico):
Logo, o calor sensível de A é 300 cal/°C.
Calor sensível de B (utilizando dados do gráfico):
E o calor sensível de B é 100 cal/°C.
Agora vamos descobrir o calor específico das substâncias:
Ca = 2,0 cal/g.ºC
Cb = 1,0 cal/g.°C
Colocando na equação:
-150.2.(Teq - 60) = 100.1,0.(Teq - 40)
Teq = 55ºC
Lembrando que, a quantidade de calor da substância A é negativa porque a substância cede calor à substância B até que entrem em equilíbrio.
Alternativa correta, A.

Deixe um comentário