Questões Sobre Calorimetria - Física - 2º ano do ensino médio
Questão 91

- A) 11
- B) 55
- C) 66
- D) 108
A alternativa correta é letra B
Do enunciado temos que no início o volume de água no interior do filtro era de 6 L, com isso, podemos calcular a sua massa inicial. Lembre-se que:
d = m/V => m = d*V
Observe também que o volume inicialmente está em litros, e por conveniência vamos deixá-los em cm³.
1 L = 1 dm³ = (10 cm)³ = 1000 cm³
m = (1 g*cm-3)(6 L) = (1 g*cm-3)(6000 cm³) = 6000 g = 6 kg
Agora, que sabemos a massa inicial podemos elaborar a resolução do nosso problema. Pelo princípio de conservação de energia, considerando o sistema fechado, temos que não há perdas de energia, e assim a energia inicial deve ser igual a energia final, de forma equivalente, a energia final menos a energia inicial deve ser igual a zero.
Ef - Ei = 0
Como sabemos que as energias envolvidas diz respeito, a variação de calor na água e na evaporação de uma porção da mesma, temos:
ΔQ + Qev = 0 (1)
Donde ΔQ é a variação de calor da água no filtro e Qev é o calor associado a evaporação de parte da água, que é dado pela seguinte expressão:
Qev = m'Le
Donde Qev é o calor associado a evaporação, m' é a massa da água que evaporou, e Le é o calor latente de vaporização da água.
Lembre-se também que:
ΔQ = mcΔT
Donde ΔQ é o variação de calor, m é a massa da substância, c é o calor específico e ΔT é a variação de temperatura (note que a variação de temperatura na escala Celsius e Kelvin é a mesma).
Substituindo tais expressões em (1) temos:
mcΔT + m'Le = 0
Substituindo os valores conhecidos (note que 6 kg = 6000 g) na expressão acima temos:
(6000 g)(1 cal.g-1.°C-1)( -5 °C) + m'(540 cal.g-1) = 0
ΔT = -5 °C se deve ao fato da água do filtro ter sido resfriada, ou seja, a temperatura inicial era maior que a temperatura final.
=> -30000 cal + m'(540 cal.g-1) = 0 => m'(540 cal.g-1) = 30000 cal
=> m' = (30000 cal)/(540 cal.g-1) = 55,56 g
Alternativa B)
d = m/V => m = d*V
Observe também que o volume inicialmente está em litros, e por conveniência vamos deixá-los em cm³.
1 L = 1 dm³ = (10 cm)³ = 1000 cm³
m = (1 g*cm-3)(6 L) = (1 g*cm-3)(6000 cm³) = 6000 g = 6 kg
Agora, que sabemos a massa inicial podemos elaborar a resolução do nosso problema. Pelo princípio de conservação de energia, considerando o sistema fechado, temos que não há perdas de energia, e assim a energia inicial deve ser igual a energia final, de forma equivalente, a energia final menos a energia inicial deve ser igual a zero.
Ef - Ei = 0
Como sabemos que as energias envolvidas diz respeito, a variação de calor na água e na evaporação de uma porção da mesma, temos:
ΔQ + Qev = 0 (1)
Donde ΔQ é a variação de calor da água no filtro e Qev é o calor associado a evaporação de parte da água, que é dado pela seguinte expressão:
Qev = m'Le
Donde Qev é o calor associado a evaporação, m' é a massa da água que evaporou, e Le é o calor latente de vaporização da água.
Lembre-se também que:
ΔQ = mcΔT
Donde ΔQ é o variação de calor, m é a massa da substância, c é o calor específico e ΔT é a variação de temperatura (note que a variação de temperatura na escala Celsius e Kelvin é a mesma).
Substituindo tais expressões em (1) temos:
mcΔT + m'Le = 0
Substituindo os valores conhecidos (note que 6 kg = 6000 g) na expressão acima temos:
(6000 g)(1 cal.g-1.°C-1)( -5 °C) + m'(540 cal.g-1) = 0
ΔT = -5 °C se deve ao fato da água do filtro ter sido resfriada, ou seja, a temperatura inicial era maior que a temperatura final.
=> -30000 cal + m'(540 cal.g-1) = 0 => m'(540 cal.g-1) = 30000 cal
=> m' = (30000 cal)/(540 cal.g-1) = 55,56 g
Alternativa B)
Questão 92
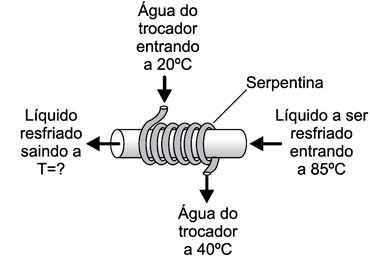
Quando a temperatura de saída da água da serpentina for 40 ºC, será possível estimar que a água da tubulação principal esteja saindo a uma temperatura T de, aproximadamente,
- A) 75 ºC
- B) 65 ºC
- C) 55 ºC
- D) 45 ºC
FAZER COMENTÁRIO- E) 35 ºC
A alternativa correta é letra C
A estratégia para a resolução da questão é perceber que o sistema pode ser tratado como sendo isolado, assim, a soma dos calores totais é zero (princípio da conservação de energia). Dessa forma, como a água da serpentina é aquecida, esperamos que a água na tubulação seja resfriada, o que está de acordo com o enunciado. Chamando ms a massa de água na serpentina, mp a massa de água na tubulação principal e C o calor específico da água, equacionando, temos:Como o fluxo de água na serpentina e na tubulação principal são conhecidos (18 litros/minuto e 12 litros/minuto, respectivamente), supondo que a densidade da água seja de 1kg/litro, para um tempo t qualquer, as massas de água serão:Cancelando os calores específicos e o tempo, chegamos que T= 55º C, que é a alternativa C.Questão 93
 Num dia frio, o ar externo, que está a uma temperatura de 5°C, é lançado para o interior da cabine, a 30°C, a uma taxa de 1,5L/s. Determine a potência térmica aproximada, em watts, absorvida pelo ar nessa troca de calor.FAZER COMENTÁRIO
Num dia frio, o ar externo, que está a uma temperatura de 5°C, é lançado para o interior da cabine, a 30°C, a uma taxa de 1,5L/s. Determine a potência térmica aproximada, em watts, absorvida pelo ar nessa troca de calor.FAZER COMENTÁRIO- A) 20
- B) 25
- C) 45
- D) 60
A alternativa correta é letra C
O ar necessita absorver uma certa quantidade de calor para aumentar sua temperatura. Logo, temos que usar a seguinte fórmula:
ΔQ = mcΔT (1)
Donde ΔQ é a variação do calor, m é massa, c é o calor específico e ΔT é a variação da temperatura.
Mas, note que não sabemos a massa de ar, porém temos uma informação com respeito a taxa com que tal transferência ocorre em L/s. Sendo assim podemos usar a relação entre densidade, massa e volume, para descobrir a nossa variável de interesse. Lembre-se que:
ρ = m/V => m = ρ*V (2)
Donde ρ é a densidade, m é a massa e V é o volume.
Sabemos que a potência é uma medida que relaciona a variação da energia em um dado tempo, ou melhor dizendo, a razão entre eles:
P = ΔQ/Δt
Donde P é a potência, ΔQ é variação do calor e Δt é o intervalo de tempo.
Logo, dividindo ambos os lados da equação (1) por Δt, e substituindo uma expressão equivalente a massa, encontrado em (2), temos:
ΔQ/Δt = ρ*VcΔT/Δt => P = ρ*cΔT(V/Δt)
Substituindo os valores conhecidos na expressão acima temos:
P = (1,2 kg/m³)(0,24 cal.g-1.°C-1)(30 °C - 5 °C)(1,5 L/s)
Lembre-se que:
1 L = 1 dm³ = (0,1 m)³ = 10-3 m³
1,5*(1 L) = 1,5*(10-3 m³) = 1,5*10-3 m³
1 cal = 4,2 J
0,24 cal = 0,24*(4,2 J) = 1,008 J
1000 g = 1 kg
1,2 kg = 1,2*(1000 g) = 1200 g
Logo,
P = (1200 g/m³)(1,008 J.g-1.°C-1)(25 °C)(1,5*10-3 m³/s) = 45,36 W ≈ 45 W
Alternativa C)94) O ar dentro de um automóvel fechado tem massa de 2,6 kg e calor específico de 720 J/kg ⋅ ºC. Considere que o motorista perde calor a uma taxa constante de 120 joules por segundo e que o aquecimento do ar confinado se deva exclusivamente ao calor emanado pelo motorista. Quanto tempo levará para a temperatura variar de 2,4 ºC a 37 ºC?
FAZER COMENTÁRIO- A) 540 s
- B) 480 s
- C) 420 s
- D) 360 s
- E) 300 s
A alternativa correta é letra A
O calor absorvido pelo ar pode ser calculado através da Quantidade de Calor representada abaixo :Q=mcΔT = 2,6 . 720 . 34,6 = 64771 J . Como 120 J são perdidos pelo motorista a cada segundo, conclue-se que para 64771 J o tempo será cerca de 540 s. Alternativa A.95) Foi realizada uma experiência em que se utilizava uma lâmpada de incandescência para, ao mesmo tempo, aquecer 100 g de água e 100 g de areia. Sabe-se que, aproximadamente, 1 cal = 4 J e que o calor específico da água é de 1 cal/g ºC e o da areia é 0,2 cal/g ºC. Durante 1 hora, a água e a areia receberam a mesma quantidade de energia da lâmpada, 3,6 kJ, e verificou-se que a água variou sua temperatura em 8 ºC e a areia em 30 ºC. Podemos afirmar que a água e a areia, durante essa hora, perderam, respectivamente, a quantidade de energia para o meio, em kJ, igual a
- A) 0,4 e 3,0.
- B) 2,4 e 3,6.
- C) 0,4 e 1,2.
- D) 1,2 e 0,4.
FAZER COMENTÁRIO- E) 3,6 e 2,4.
A alternativa correta é letra C
Para o cálculo do calor dissipado para o meio, tanto no aquecimento da água quanto no aquecimento da areia, deve-se, primeiramente, calcular qual a quantidade de calor efetivamente gasta no aquecimento descrito no enunciado.Para a água, tem-se que:Para a areia:Como a lâmpada fornece a mesma quantidade de energia para os dois aquecimentos (3,6 J), calcula-se a energia dissipada pela subtração da energia fornecida e da energia utilizada no aquecimento:96) Para realizar um experimento no litoral, um cientista precisa de 8 litros de água a 80ºC. Como não dispõe de um termômetro, decide misturar uma porção de água a 0ºC com outra a 100ºC. Ele obtém água a 0ºC a partir de uma mistura, em equilíbrio térmico, de água líquida com gelo fundente, e água a 100ºC, a partir de água em ebulição. Considerando que haja troca de calor apenas entre as duas porções de água, os volumes, em litros, de água a 0 ºC e de água a 100 ºC que o cientista deve misturar para obter água a 80 ºC são iguais, respectivamente, a
FAZER COMENTÁRIO- A) 1,6 e 6,4.
- B) 3,2 e 4,8.
- C) 4,0 e 4,0.
- D) 2,4 e 5,6.
- E) 5,2 e 2,8.
A alternativa correta é letra A
Queremos 8 litros de água a 80ºC. Para isso vamos misturar v litros de água a 0ºC com (8-v) litros de água a 100ºC [conforme o enunciado, vamos considerar que apenas as duas partes líquidas trocam calor].
A fórmula fundamental da Calorimetria é
onde Q é a quantidade de calor, m e c são, respectivamente, a massa e o calor específico da substância, e Δt é a variação da temperatura.
Temos que v litros vão esquentar de 0ºC para 80ºC e (8-v) litros vão esfriar de 100ºC para 80ºC, portanto
Usando a fórmula da densidade
obtemos
A densidade d e o calor específico são não nulos, então
Questão 97
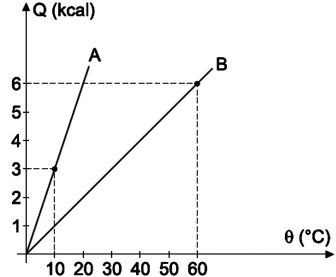 Misturando-se as duas substâncias: A (mA= 150 g e θA = 60 °C) e B (mB = 100 g e θB = 40 °C), a temperatura final de equilíbrio será:
Misturando-se as duas substâncias: A (mA= 150 g e θA = 60 °C) e B (mB = 100 g e θB = 40 °C), a temperatura final de equilíbrio será:- A) 55 °C.
- B) 50 °C.
- C) 45 °C.
- D) 60 °C.
FAZER COMENTÁRIO- E) 40 °C.
A alternativa correta é letra A
A quantidade de calor, é dada pela equação:Quando ocorre o equilíbrio térmico, as quantidades de calor finais são iguais, logo, só precisamos igualar as duas equações das substância A e B:Agora vamos resolver as equações para encontrar o calor específico (c) de A e de B.Calor sensível de A (utilizando dados do gráfico):Logo, o calor sensível de A é 300 cal/°C.Calor sensível de B (utilizando dados do gráfico):E o calor sensível de B é 100 cal/°C.Agora vamos descobrir o calor específico das substâncias:Ca = 2,0 cal/g.ºCCb = 1,0 cal/g.°CColocando na equação:-150.2.(Teq - 60) = 100.1,0.(Teq - 40)Teq = 55ºCLembrando que, a quantidade de calor da substância A é negativa porque a substância cede calor à substância B até que entrem em equilíbrio.Alternativa correta, A.98) Uma cozinheira, moradora de uma cidade praiana, não dispunha de um termômetro e necessitava obter água a uma temperatura de 60 ºC. Resolveu, então, misturar água fervendo com água proveniente de um pedaço de gelo que estava derretendo. Considere o sistema isolado, ou seja, que a troca de calor só se estabeleceu entre as quantidades de água misturadas e, ainda, que a cozinheira usou a mesma xícara nas suas medições. A cozinheira só chegaria ao seu objetivo se tivesse misturado uma xícara da água a 0 ºC com
- A) três xícaras de água fervendo.
- B) duas xícaras e meia de água fervendo.
- C) duas xícaras de água fervendo.
- D) uma xícara e meia de água fervendo.
FAZER COMENTÁRIO- E) meia xícara de água fervendo.
A alternativa correta é letra D
Sabemos queSupondo que a cozinheira misture n xícaras de massa M de água quente na xícara (de massa também M) de água fria, teremos queOnde Δθf e Δθq representam as variações de temperatura sofridas respectivamente pela água fria e pela água quente até chegar à temperatura de 60 ºC. Como a cidade é praiana, esperamos que as temperaturas de ebulição e de fusão da água sejam respectivamente 100 e 0 ºC. Substituindo na equação, teremosA cozinheira precisará misturar uma xícara e meia de água fervendo na água fria para obter a temperatura desejada.99) A evaporação da água é um dos mecanismos que promove a manutenção da temperatura corporal. Assinale a alternativa em que o fato descrito NÃO é explicado por esse mecanismo.
FAZER COMENTÁRIO- A) Banho de imersão na água fria após uma sauna.
- B) Cães ofegantes e com a língua para fora em dias quentes.
- C) Mãos molhadas e colocadas à frente de um ventilador em funcionamento.
- D) Transpiração de atletas durante a prática de atividades físicas.
A alternativa correta é letra A
Vamos analisar cada uma das alternativas e assim verificar a sua veracidade.
A alternativa B) diz respeito aos cães que colocam a língua para fora quando estão ofegantes. Neste momento, a saliva pode evaporar e assim tentar equilibrar a temperatura do animal, visto que este cansaço se origina de alguma atividade que tem como consequência uma elevação da temperatura corporal. Logo, essa alternativa É explicada por esse mecanismo.
A alternativa C) diz respeito as mãos molhadas colocadas a frente de um ventilador. O vento tem uma importante função no momento de espalhar as gotículas de água, e com isso facilitar a evaporação. Logo, essa alternativa É explicada por esse mecanismo.
A alternativa D) se refere ao suor dos atletas quando fazem atividade física. O fato da agitação do indivíduo provoca uma elevação da temperatura interna, para resfriar o corpo o atleta começa a suar, este que evapora e completa o resfriamento. Logo, essa alternativa É explicada por esse mecanismo.
Por fim, temos que a única alternativa que corresponde a um fato que não é explicado por esse mecanismo é o banho de imersão na água fria após uma sauna. Isto porque neste momento a expectativa é baixar a temperatura corporal por meio de algo mais direto e não pela evaporação da água, mas transferir calor para ela sem fazê-la evaporar.
Alternativa A)Continua após a publicidade..100) Um antigo, mas eficiente, método de se obter água a alguns graus Celsius abaixo da temperatura ambiente, é colocá-la dentro de uma moringa feita de barro cozido. Esse material é poroso à água, que atravessa muito lentamente as paredes da moringa e ao tocá-la, percebe-se que sua superfície externa está úmida. Com relação a esse processo de resfriamento da água, pode-se afirmar que ele acontece porque
- A) o calor específico do barro é maior que o calor específico da água.
- B) a temperatura da moringa é maior que a temperatura ambiente.
- C) a evaporação da água das paredes externas da moringa retira calor da água presente no seu interior.
- D) a condutividade térmica da água é maior do que a condutividade térmica do barro.
FAZER COMENTÁRIO- E) as paredes da moringa isolam, termicamente, a água contida em seu interior, do meio ambiente.
« Anterior 1 … 8 9 10 11 12 … 14 Próximo »A alternativa correta é letra C
Como é afirmado que a água do interior da moringa fica a uma temperatura abaixo da temperatura ambiente ocorre uma transferência de calor da parte interna para a externa(resfriamento).
Também é afirmado que a parte externa fica úmida.
Logo, podemos afirmar:
Erradas:
A-Não podemos afirmar, e não tem relação com o processo de resfriamento
B-Afirma o contrário do que foi dito no enunciado
D-Não podemos afirmar, e não tem relação com o processo de resfriamento
E-Se isolarem a água inserida não seria possível trocas de calor, afirmando o contrario do enunciado
Alternativa correta e que explica o fenômeno é a Letra C - B) a temperatura da moringa é maior que a temperatura ambiente.
- B) duas xícaras e meia de água fervendo.
- B) 50 °C.
- B) 2,4 e 3,6.
- B) 65 ºC
