Questões Sobre Calorimetria - Física - 2º ano do ensino médio
41) Quatro blocos de gelo idênticos, todos à mesma temperatura inicial, são colocados em um ambiente com temperatura controlada e mantida constante em 20oC, nas seguintes condições: • bloco 1, sem nenhum envoltório; • bloco 2, enrolado em uma folha de papel alumínio; • bloco 3, enrolado em uma folha de jornal; • bloco 4, enrolado em um tecido grosso de lã. É CORRETO afirmar que, nessas condições, o bloco de gelo que vai derreter mais lentamente é o
- A) 1.
- B) 2.
- C) 3.
- D) 4.
A alternativa correta é letra D
Vamos analisar cada material, descrevendo sua condutibilidade térmica, e com isso vai ficar claro o caso em que o gelo derrete mais lentamente.
O bloco 1 vai derreter normalmente já que não existe um intermediário nas trocas de calor.
O bloco 2 que é enrolado em papel alumínio vai derreter um pouco mais devagar, já que o alumínio apesar de bom condutor térmico ainda é um intermediário no processo, e nada se compara a ausência de tal para o derretimento ser mais rápido.
O bloco 3 vai derreter ainda mais devagar, já que estará enrolado em um jornal, que vai isolar consideravelmente o gelo do calor externo, mas é claro que em um dado momento o gelo vai começar a derreter.
Já o bloco 4 é aquele que vai demorar mais para derreter, isto porque a lã é um excelente isolante térmico, isto quer dizer que ela tende a manter a temperatura interna do corpo, dificultando e muito o seu contato com o ambiente externo. Até por isso usamos blusas de lã e não de alumínio.
Alternativa D).
O bloco 1 vai derreter normalmente já que não existe um intermediário nas trocas de calor.
O bloco 2 que é enrolado em papel alumínio vai derreter um pouco mais devagar, já que o alumínio apesar de bom condutor térmico ainda é um intermediário no processo, e nada se compara a ausência de tal para o derretimento ser mais rápido.
O bloco 3 vai derreter ainda mais devagar, já que estará enrolado em um jornal, que vai isolar consideravelmente o gelo do calor externo, mas é claro que em um dado momento o gelo vai começar a derreter.
Já o bloco 4 é aquele que vai demorar mais para derreter, isto porque a lã é um excelente isolante térmico, isto quer dizer que ela tende a manter a temperatura interna do corpo, dificultando e muito o seu contato com o ambiente externo. Até por isso usamos blusas de lã e não de alumínio.
Alternativa D).
42) Uma panela de ferro, de massa igual a 800 g, tem calor específico igual a 0,16 cal, e outra panela de alumínio, de massa igual a 200 g, tem calor específico igual a 0,34 cal/g.°C. Com os dados referentes a essas panelas, a capacidade térmica da panela de ferro e da panela de alumínio, em cal/°C são respectivamente:
- A) 68 e 128
- B) 128 e 68
- C) 78 e 138
- D) 138 e 78
- E) 138 e 68
A alternativa correta é letra B
A Capacidade Térmica é dada por : C = m.c .
Sendo :
C - Capacidade Térmica
m - massa
c - calor específico
A Capacidade Térmica Cf da panela de ferro é :
Cf= 800 . 0,16 = 128 cal/ºC
A Capacidade Térmica Ca da panela de alumínio é :
Ca= 200 . 0,34 = 68 cal/ºC
Alternativa correta, letra B.
43) Certos povos nômades que vivem no deserto, onde as temperaturas durante o dia podem chegar a 50 ºC, usam roupas de lã branca, para se protegerem do intenso calor da atmosfera. Essa atitude pode parecer-nos estranha, pois, no Brasil, usamos a lã para nos proteger do frio. O procedimento dos povos do deserto pode, contudo, se explicar pelo fato de que:
- A) a lã é naturalmente quente (acima de 50 º
- B) e, no deserto, ajuda a esfriar os corpos das pessoas, enquanto o branco é uma “cor fria”, ajudando a esfriá-los ainda mais.
- C) a lã é um bom isolante térmico, impedindo que calor de fora chegue aos corpos das pessoas, e o branco absorve bem a luz em todas as cores, evitando que luz do sol os aqueça ainda mais.
- D) a lã é um bom isolante térmico, impedindo que calor de fora chegue aos corpos das pessoas, e o branco reflete bem a luz em todas as cores, evitando que a luz do sol os aqueça ainda mais.
- E) a lã é naturalmente quente (embora esteja abaixo de 50 º
A alternativa correta é letra C
A Capacidade Térmica da lã é alta ( ela é um excelente isolante térmico), ou seja, necessita de grandes quantidades de calor para que sua temperatura varie. Além disso, a cor branca da lã tem baixa absorvidade e reflete a luz. A alternativa que expressa corretamente essas ideias é a letra C.
Questão 44

- A) 3,8 x 1015W.
- B) 4,6 x 1014W.
- C) 2,1 x 1013W.
- D) 1,2 x 1012W.
- E) 1,1 x 1011W.
A alternativa correta é letra B
Para resolver este problema precisamos descobrir a quantidade de calor envolvida no processo citado, e para isso vamos utilizar a seguinte equação:
Q = mLV
Donde Q é o calor, m é a massa e LV é o calor latente de vaporização.
Mas, não sabemos a massa, contudo temos informações com respeito ao volume de água gerado neste processo, considerando as informações no enunciado e que não há uma absorção por parte do solo, ou perda de água no processo, temos que será gerado uma camada de água sobre o terreno de 1,5 cm de altura, com um raio de 660 km, neste caso temos um cilindro, que tem volume calculado a partir da seguinte fórmula:
V = πr²h
Donde V é o volume, r é o raio e h é a altura.
Com isso, e usando a fórmula de densidade, temos:
ρ = m/V => m = ρV = ρπr²h
Donde m é a massa, V é o volume e ρ é a densidade.
Q = mLV = ρπr²hLV = (10³ kg/m³)(3)(660 km)²(1,5 cm)(2*106 J/kg)
Lembrando que 1 cm = 0,01 m e 1 km = 10³ m
Q=(10³ kg/m³)(3)(660*10³ m)²(0,015 m)(2*106 J/kg)
Q = 3,9204*1019 J
Como queremos descobrir a potência relacionada a tal fenômeno, devemos usar a seguinte fórmula:
P = Q/Δt
Donde P é a potência, Q é o calor e Δt é o tempo decorrido (1 dia).
P = (3,9204*1019 J)/(8,6*104 s) ≈ 4,6*1014 W
Alternativa B)
Q = mLV
Donde Q é o calor, m é a massa e LV é o calor latente de vaporização.
Mas, não sabemos a massa, contudo temos informações com respeito ao volume de água gerado neste processo, considerando as informações no enunciado e que não há uma absorção por parte do solo, ou perda de água no processo, temos que será gerado uma camada de água sobre o terreno de 1,5 cm de altura, com um raio de 660 km, neste caso temos um cilindro, que tem volume calculado a partir da seguinte fórmula:
V = πr²h
Donde V é o volume, r é o raio e h é a altura.
Com isso, e usando a fórmula de densidade, temos:
ρ = m/V => m = ρV = ρπr²h
Donde m é a massa, V é o volume e ρ é a densidade.
Q = mLV = ρπr²hLV = (10³ kg/m³)(3)(660 km)²(1,5 cm)(2*106 J/kg)
Lembrando que 1 cm = 0,01 m e 1 km = 10³ m
Q=(10³ kg/m³)(3)(660*10³ m)²(0,015 m)(2*106 J/kg)
Q = 3,9204*1019 J
Como queremos descobrir a potência relacionada a tal fenômeno, devemos usar a seguinte fórmula:
P = Q/Δt
Donde P é a potência, Q é o calor e Δt é o tempo decorrido (1 dia).
P = (3,9204*1019 J)/(8,6*104 s) ≈ 4,6*1014 W
Alternativa B)
45) Sabe-se que, na mecânica newtoniana, um corpo isolado de forças externas e em repouso em relação a um determinado referencial inercial não possui energia. Ele só adquire energia se uma força externa lhe conferir energia cinética ou potencial. Já na Teoria da Relatividade, massa e energia são equivalentes. Dessa forma, um corpo em repouso, cuja massa de repouso é m0 , possui uma energia de repouso, dada por m0C2, onde C é a velocidade da Luz. Suponha que você dispõe de um equipamento capaz de transformar a massa de um corpo em energia. Sabendo-se que o calor latente de fusão do gelo é Lf = 80 cal/g e aproximando 1 cal = 4,2 J, o valor aproximado de massa, em gramas, necessário para transformar um “Iceberg” de massa igual a 27,0 mil toneladas de gelo que se encontra a 0° C em água a 0° C é
- A) 0,1.
- B) 1,0.
- C) 10,0.
FAZER COMENTÁRIO- D) 0,01.
A alternativa correta é letra A
A energia em forma de calor necessária para derreter tal Iceberg, é dada por:
Em termos de energia de repouso, podemos escrever:
onde m0 seria a quantidade de massa correspondente à tal energia. Portanto, alternativa A.46)
FAZER COMENTÁRIO- A) 100
- B) 200
- C) 540
- D) 780
A alternativa correta é letra B
Sabemos que a potência é uma medida cujo objetivo é mensurar a rapidez com que é executa um trabalho, ou de forma equivalente, a rapidez com que ocorre transferências de energia.
Com isso,
P = ΔQ/Δt
P é a potência, ΔQ é a variação da energia (calor), e Δt é o tempo decorrido.
O fato da potência ser constante, quer dizer que ela é a mesma nos dois momentos do gráfico, de 0 a 10 min e de 10 a 54 min.
De 0 a 10 minutos temos que a variação de calor é:
ΔQ = mcΔT
Donde ΔQ é a variação de calor, m é a massa, c é o calor específico e ΔT é a variação de temperatura.
Logo,
P = mcΔT/Δt
De 10 a 54 minutos temos que o calor é:
Q = mLv
Donde Q é o calor, m é a massa e Lv é o calor de vaporização.
E assim, temos:
P' = mLv/Δt'
Mas, note que P' = P, como já discutido acima, então:
mLv/Δt' = mcΔT/Δt
Dividindo ambos os lados por m:
Lv/Δt' = cΔT/Δt => Lv = Δt'cΔT/Δt
Δt' = 54 min - 10 min = 44 min
Δt = 10 min - 0 min = 10 min
ΔT = 78 °C - 0 °C = 78 °C
Lv = (44 min)(0,58 cal/g.°C)(78 °C)/(10 min)≈ 200 cal/g
Alternativa B)47) A enfermeira de um posto de saúde resolveu ferver 1,0 litro de água para ter uma pequena reserva de água esterilizada. Atarefada, ela esqueceu a água a ferver e quando a guardou verificou que restaram 950 mL. Sabe-se que a densidade da água é 1,0 · 103 kg/m3, o calor latente de vaporização da água é 2,3 · 106 J/kg e supõe-se desprezível a massa de água que evaporou ou possa ter saltado para fora do recipiente durante a fervura. Pode-se afirmar que a energia desperdiçada na transformação da água em vapor foi aproximadamente de:
- A) 25 000 J.
- B) 115 000 J.
- C) 230 000 J.
- D) 330 000 J.
FAZER COMENTÁRIO- E) 460 000 J.
A alternativa correta é letra B
Calculando a massa de água que evaporou:Onde d= densidade em kg/m³, m= massa em kg, V= Volume em m³.Conforme a equação de calor latente temos:Onde Q= calor em joules, m= massa em kg e L= calor latente em J/kg.Questão 48
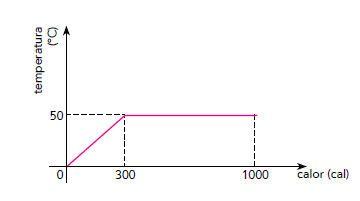 O calor latente de fusão dessa substância, em cal/g, é igual a:FAZER COMENTÁRIO
O calor latente de fusão dessa substância, em cal/g, é igual a:FAZER COMENTÁRIO- A) 70.
- B) 80.
- C) 90.
- D) 100.
A alternativa correta é letra A
Para calcular o calor latente de fusão dessa substância devemos analisar desde o ponto em que começa a mudança de fase (300 cal, 50 °C) até o ponto em que toda a substância já mudou de fase (1000 cal, 50 °C).
Sendo assim temos:Q = mLF
Qf - Qi =mLF
LF = (Qf - Qi)/m = (1000 cal - 300 cal)/(10 g) = 70 cal/gAlternativa A)Questão 49
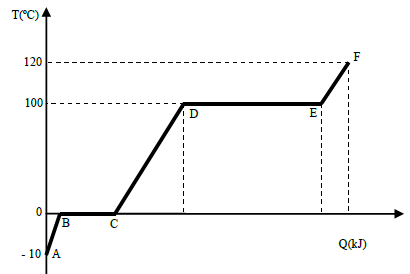 Sabemos que, por meio de gráficos desse tipo, é possível obter os valores do calor específico e do calor latente das substâncias estudadas. Assinale a alternativa que fornece corretamente o intervalo em que se pode obter o valor do calor latente de vaporização desse líquido.FAZER COMENTÁRIO
Sabemos que, por meio de gráficos desse tipo, é possível obter os valores do calor específico e do calor latente das substâncias estudadas. Assinale a alternativa que fornece corretamente o intervalo em que se pode obter o valor do calor latente de vaporização desse líquido.FAZER COMENTÁRIO- A) AB.
- B) BD.
- C) DE.
- D) CD.
- E) EF.
A alternativa correta é letra C
O calor latente de uma substância é o valor associado com a sua mudança de fase, neste momento a substância deixa de aumentar sua temperatura, e com a inserção de calor no sistema (uma dada quantidade) ela muda de fase.
Como a temperatura deve ser constante, temos dois possíveis candidatos a calor latente de vaporização BC e DE. Mas, a quantidade esperada não pode se referir a BC, pois ela está em uma temperatura menor que DE, o calor latente de vaporização deve estar na maior faixa de temperatura. Logo, temos que o intervalo correto para o calor latente de vaporização é DE.
Alternativa C)Continua após a publicidade..50) Qualquer dos seus leitores que tenha a ventura de residir em meio ao romântico cenário do País de Gales ou da Escócia poderia, não tenho dúvida, confirmar meus experimentos medindo a temperatura no topo e na base de uma cascata. Se minhas observações estão corretas, uma queda de 817 pés deve gerar um grau de calor, e a temperatura do rio Niágara deve subir cerca de um quinto de grau por causa de sua queda de 160 pés.
- A) 5,0 e 1,0.
- B) 1,0 e 0,20.
- C) 0,60 e 0,12.
- D) 0,30 e 0,060.
FAZER COMENTÁRIO- E) 0,10 e 0,020.
« Anterior 1 … 3 4 5 6 7 … 14 Próximo »A alternativa correta é letra C
Considerando que o trabalho do peso durante a queda será convertido integralmente em calor para aumentar a temperatura da água, temos:Wp = Q ⇒ mgh = mcΔT ⇒ 10.250 = 4200.ΔT⇒ ΔT = 0,6 °CSendo esse valor equivalente ao "1 grau de calor" que a temperatura da água subiu, então "1/5 de grau" equivale a:0,6 / 5 = 0,12 °C - B) 1,0 e 0,20.
- B) 115 000 J.
- B) 1,0.
