Questões Sobre Cinética Química - Química - 2º ano do ensino médio
51) Na reação de dissociação térmica do HI(g), a velocidade de reação é proporcional ao quadrado da concentração molar do HI. Se triplicarmos a concentração do HI, a velocidade da reação:
- A) aumentará 6 vezes.
- B) aumentará 9 vezes.
- C) diminuirá 6 vezes.
- D) diminuirá 9 vezes.
FAZER COMENTÁRIO- E) diminuirá 3 vezes
A alternativa correta é letra B
Primeiramente, considerando a equação da velocidade de reação, tem-se o seguinte:v = k . [HI]2Triplicando a concentração de HI, tem-se:v2 = k. [3 HI]2v2 = 9. k. [HI]Assim, dividindo v2 por v1, encontra-se que v2 é 9 vezes maior que v1.Portanto, a resposta correta é a alternativa B.52) Seja a reação: X → Y + Z. A variação na concentração de X em função do tempo é:
- A) 0,1 mol/L.min.
- B) 0,3 mol/L.min.
- C) 0,5 mol/L.min.
- D) 1,0 mol/L.min.
- E) 2 mol/L. min.
FAZER COMENTÁRIOA alternativa correta é letra A
Conforme mostra a fórmula, a velocidade média da reação é a seguinte:O sinal negativo indica que é a velocidade de consumo do reagente X.Portanto, a resposta correta é a alternativa A.Questão 53
O gráfico a seguir representa a variação das concentrações das substâncias X, Y e Z durante a reação em que elas tomam parte. A equação que representa a reação é:
A equação que representa a reação é:- A) X + Z ↔Y
- B) X + Y ↔Z
- C) X ↔ Y + Z
- D) Y ↔ X + Z
FAZER COMENTÁRIO- E) Z ↔ X + Y
A alternativa correta é letra E
Como é notado pelo gráfico disponibilizado, nota-se que a espécie Z tem sua concentração diminuída ao correr do tempo, indicando que é consumida no decorrer da reação. Já as espécies X e Y aumentam de acordo com o tempo, indicando que são geradas. Assim, uma possível reação entre as três espécies é da seguinte forma:Z como reagente e X e Y como produtos.Portanto, a resposta correta é a opção "E".54) Decorridos 15 segundos do início da difusão dos vapores, verificou-se a formação do anel de cloreto de amônio a 59,4 cm da extremidade que contém o algodão com amônia e a 40,6 cm da extremidade que contém o algodão com ácido clorídrico.
- A) 1,75.
- B) 1,46.
- C) 0,96.
FAZER COMENTÁRIO- D) 0,74.
A alternativa correta é letra B
Sabendo-se que a distância de difusão do gás NH3 foi de 59,4 e que a do gás HCl foi de 40,6, em um mesmo período de tempo (15 segundos), a razão entre suas velocidades médias será a razão entre suas distâncias percorridas. Assim: .
Portanto, a resposta correta é a alternativa B.Questão 55
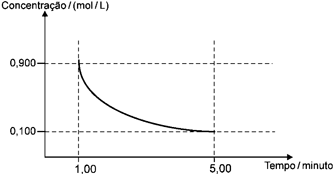
Considerando-se as informações desse gráfico, é CORRETO afirmar que, no intervalo entre 1 e 5 minutos, a velocidade média de consumo desse reagente é de:- A) 0,200 (mol /
- B) / min.
- C) 0,167 (mol /
- D) / min.
FAZER COMENTÁRIO- E) 0,225 (mol /
A alternativa correta é letra A
A velocidade média de consumo de um reagente é dada pela razão entre a variação molar do composto e o tempo gasto (assumindo volume constante), ou seja:O sinal negativo indica consumo do componente.Portanto, a resposta correta é a alternativa A.Questão 56
Pode-se detectar a presença de iodetos em águas-mães de salinas, por meio da reação representada pela equaçãoH2O2(aq) + 2 H+(aq) + 2I–(aq) → 2H2O(l) + I2(aq)Os seguintes gráficos, mostrando a velocidade da reação em função da concentração dos reagentes, foram construídos com os dados coletados em vários experimentos:– variando a concentração de H2O2 e mantendo constantes as de H+ e I–;– variando a concentração de H+ e mantendo constantes as de H2O2 e I–;– variando a concentração de I- e mantendo constantesas de H2O2 e H+. Com base na análise dos gráficos, afirma-se que a velocidade da reaçãoI. depende apenas da concentração de H+.II. é diretamente proporcional à concentração de H2O2.III. independe da concentração de H+.IV. é inversamente proporcional à concentração de I–.É correto o que se afirma apenas em:Com base na análise dos gráficos, afirma-se que a velocidade da reaçãoI. depende apenas da concentração de H+.II. é diretamente proporcional à concentração de H2O2.III. independe da concentração de H+.IV. é inversamente proporcional à concentração de I–.É correto o que se afirma apenas em:
Com base na análise dos gráficos, afirma-se que a velocidade da reaçãoI. depende apenas da concentração de H+.II. é diretamente proporcional à concentração de H2O2.III. independe da concentração de H+.IV. é inversamente proporcional à concentração de I–.É correto o que se afirma apenas em:Com base na análise dos gráficos, afirma-se que a velocidade da reaçãoI. depende apenas da concentração de H+.II. é diretamente proporcional à concentração de H2O2.III. independe da concentração de H+.IV. é inversamente proporcional à concentração de I–.É correto o que se afirma apenas em:- A) I
- B) III
- C) IV
- D) II e III
FAZER COMENTÁRIO- E) II, III e IV
A alternativa correta é letra D
Analisando o primeiro e último gráfico, em que houve o aumento de H2O2 e I-, respectivamente, nota-se que a velocidade aumentou de maneira proporcional.Já quando variou-se somente a concentração de H+, não ocorreu mudanças com a velocidade, indicando que ela não depende dos íons H+.Portanto, somente os itens II e III estão corretos.Assim, a resposta correta é a alternativa D.Questão 57
2NH3 ⇒ N2 + 3H2A tabela abaixo indica a variação na concentração de reagente em função do tempo. Qual é a velocidade média de consumo do reagente nas duas primeiras horas de reação?
Qual é a velocidade média de consumo do reagente nas duas primeiras horas de reação?- A) 4,0 mol L-1h-1
- B) 2,0 mol L-1h-1
- C) 10 km h-1
- D) 1,0 mol L-1h-1
FAZER COMENTÁRIO- E) 2,3 mol h-1
A alternativa correta é letra B
A velocidade média de consumo da amônia (reagente da reação), é dada pela razão entre a variação da quantidade molar de NH3 no tempo decorrido de duas horas.Ou seja:Sendo que o sinal negativo indica apenas que se trata de consumo do reagente.Portanto, a resposta correta é a alternativa B.Questão 58
2 SO2 + O2 → 2 SO3.
Na tabela, temos a variação da massa do SO2 em função do tempo. Assinale a alternativa que indica o valor da velocidade média da reação no intervalo de 0 minuto a 8 minutos.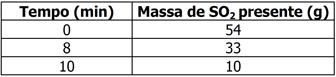
- A) 2,500 g/min.
- B) 2,600 g/min.
- C) 2,625 g/min.
- D) 2,700 g/min.
FAZER COMENTÁRIO- E) 2,725 g/min.
A alternativa correta é letra C
A velocidade média de consumo da amônia (reagente da reação), é dada pela razão entre a variação da quantidade molar de SO2 no tempo decorrido de 0 a 8 minutos.Ou seja:Sendo que o sinal negativo indica apenas que se trata de consumo do reagente.Portanto, a resposta correta é a alternativa C.59) Em determinada experiência, a reação de formação de água está ocorrendo com o consumo de 4 mols de oxigênio por minuto. Consequentemente, a velocidade de consumo de hidrogênio é de:
- A) 2 mol/min
- B) 4 mol/min
- C) 8 mol/min
- D) 12mol/min
FAZER COMENTÁRIO- E) 16 mol/min
A alternativa correta é letra C
A reação de formação da água é dada pela equação seguinte:O2 (g) + 2H2(g) → 2H2O (g)Assim, se a velocidade de consumo de O2 é 4 mols/min, a velocidade de consumo de H2 deve ser o dobro devido aos coeficientes estequiométricos da reação, dessa forma, a velocidade será 8 mols/min.Portanto, a resposta correta é a alternativa C.Continua após a publicidade..60) A platina é um metal nobre, encontrada livre na natureza na forma de pepitas, e é muito empregada na produção de catalisadores, que são utilizados para
FAZER COMENTÁRIO- A) acelerar a formação de compostos gasosos, somente.
- B) aumentar a velocidade de reações químicas específicas.
- C) retardar a produção de compostos indesejáveis, somente.
- D) controlar o deslocamento de uma reação química específica.
- E) promover a decomposição sólida de reações químicas somente.
A alternativa correta é letra B
Alternativa correta: B
O catalisador não participa de uma reação, ele vai proporcionar a ocorrência dela em um tempo menor do que em condições normais ela ocorreria e isso é possível através da diminuição da energia de ativação e aumento da velocidade da reação. - B) 4 mol/min
- B) 2,600 g/min.
- B) 2,0 mol L-1h-1
- B) III
- B) 1,46.
- B) X + Y ↔Z
- B) 0,3 mol/L.min.
- B) aumentará 9 vezes.
