Continua após a publicidade..
Considere os seguintes dados sobre potenciais padrão de eletrodo:
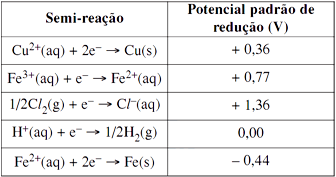
Se uma lâmina de cobre puro for mergulhada em uma solução ácida de cloreto de ferro (III), a 1 mol/L nas condições-padrão, haverá, num primeiro momento,
- A) dissolução do cobre da lâmina
- B) formação de cloro gasoso
- C) liberação de hidrogênio gasoso
- D) depósito de ferro metálico
- E) formação de mais íons cloreto
Resposta:
A alternativa correta é letra A
As semi-reações, que ocorrem do cobre puro em uma solução ácida de cloreto de ferro(III), são as seguintes:
Cu(s) → Cu2+(aq) + 2e– Eoxi = – 0,36V
2Fe3+(aq) + 2e– → 2Fe2+(aq) Ered = +0,77V
–––––––––––––––––––––––––––––––––––––––––––––
Cu(s) + 2Fe3+(aq) → Cu2+(aq) + 2Fe2+(aq) ΔE = + 0,41V
Cu(s) → Cu2+(aq) + 2e– Eoxi = – 0,36V
2Fe3+(aq) + 2e– → 2Fe2+(aq) Ered = +0,77V
–––––––––––––––––––––––––––––––––––––––––––––
Cu(s) + 2Fe3+(aq) → Cu2+(aq) + 2Fe2+(aq) ΔE = + 0,41V
Durante este processo, o potencial utilizado foi positivo, ou seja, ΔE > 0, indicando que a reação é espontânea.
Como o processo é espontâneo, a lâmina de cobre sofre oxidação (perda de elétrons) e o produto gerado desta oxidação (Cu2+) é dissolvido na solução ácida de cloreto de ferro (III). Portanto, a alternativa correta é a letra A.

Deixe um comentário