Continua após a publicidade..
Pode-se montar um circuito elétrico com um limão, uma fita de magnésio, um pedaço de fio de cobre e um relógio digital, como mostrado na figura.
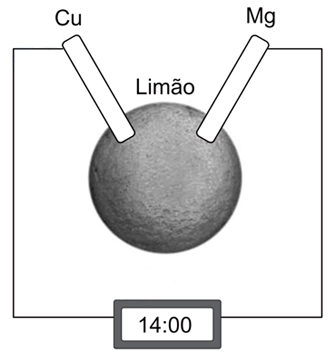
O suco ácido do limão faz o contato entre a fita de magnésio e o fio de cobre, e a corrente elétrica produzida é capaz de acionar o relógio.
Dados:
Com respeito a esse circuito, pode-se afirmar que:
- A) se o fio de cobre for substituído por um eletrodo condutor de grafite, o relógio não funcionará.
- B) no eletrodo de magnésio ocorre a semi-reaçãoMg(s) → Mg2+ + 2e–.
- C) no eletrodo de cobre ocorre a semi-reaçãoCu2+ + 2e– → Cu(s).
- D) o fluxo de elétrons pelo circuito é proveniente do eletrodo de cobre.
- E) a reação global que ocorre na pilha éCu2+ + Mg(s) → Cu(s) + Mg2+.
Resposta:
A alternativa correta é letra B
O cobre nessa pilha servirá apenas de eletrodo suporte, não participará da reação, ou seja não fornecerá íons para a solução nem, tão pouco, será reduzido
Precisamos analisar os dados contidos na tabela:
A pilha formada será entre o Magnésio e o Hidrogênio. O Magnésio, com menor potencial de redução, será oxidado:
Mg(s) → Mg 2+ + 2e-
Enquanto que o Hidrogênio será reduzido:
2H+ + 2 e- →H2 (g)
A equação global da pilha será:
2H+ + Mg (s) → H2 (g) + Mg 2+
Resposta B

Deixe um comentário