Continua após a publicidade..
Ácido cítrico reage com hidróxido de sódio segundo a equação:
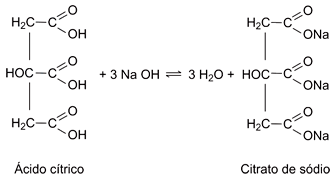
Considere que a acidez de um certo suco de laranja provenha apenas do ácido cítrico. Uma alíquota de 5,0 mL desse suco foi titulada com NaOH 0,1 mol/L, consumindo-se 6,0 mL da solução básica para completa neutralização da amostra analisada. Levando em conta estas informações e a equação química apresentada, é correto afirmar que a concentração de ácido cítrico no referido suco, em mol/L, é:
- A) 2,0.10–4
- B) 6,0.10–4
- C) 1,0.10–2
- D) 1,2.10–2
- E) 4,0.10–2
Resposta:
A alternativa correta é letra E
Pela equação química apresentada, tem-se que a razão molar de NaOH : Ácido Cítrico é igual a 3:1.
Em 6,0mL da solução de NaOH, tem-se uma quantidade molar igual a 6,0.10-4 mol. Dessa forma, adotando a razão molar entre o ácido e a base, chega-se que a quantidade molar de ácido cítrico é igual a 2,0.10-4 mol.
Assim, pode-se dizer que a concentração de ácido cítrico no suco é de:
Portanto, a resposta correta é a alterntativa E.

Deixe um comentário