Continua após a publicidade..
Em uma das primeiras classificações periódicas, os elementos químicos eram organizados em grupos de três, denominados tríades. Os elementos de cada tríade apresentam propriedades químicas semelhantes, e a massa atômica do elemento central equivale aproximadamente à média aritmética das massas atômicas dos outros dois. Observe as tríades a seguir:
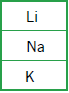
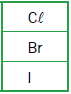
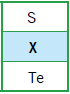
Com base nos critérios desta classificação, a letra X corresponde ao seguinte elemento químico:
- A) O.
- B) As.
- C) Se.
- D) Po.
Resposta:
A alternativa correta é letra C
A tríade que contém o elemento X, as massas atômicas do enxofre (S) e do telúrio (Te) são iguais a 32 e a 127,5, respectivamente.
A média aritmética dessas duas massas equivale a:
A média aritmética dessas duas massas equivale a:
32+127,5/2 = 79,5
Os elementos químicos cujas massas atômicas mais se aproximam de 79,75 são o selênio (Se), com massa igual a 79, e o bromo (Br), com massa igual a 80. Entre esses dois elementos, porém, o selênio é aquele que apresenta propriedades químicas semelhantes ao enxofre e ao telúrio, sendo sua configuração eletrônica da camada de valência igual a ns2np4. Logo, considerando os critérios dessa antiga classificação periódica, a letra X corresponde ao Selênio (Se).

Deixe um comentário