Continua após a publicidade..
Baterias de íon-lítio empregam o lítio na forma iônica, que está presente no eletrólito pela dissolução de sais de lítio em solventes não aquosos. Durante o processo de descarga da bateria, os íons lítio deslocam-se do interior da estrutura que compõe o anodo (grafite) até a estrutura que compõe o catodo (Co02), enquanto os elétrons se movem através do circuito externo (Fig. 31).
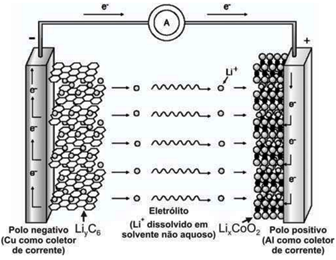
Figura 31: Circuito externo
Neste processo, o cobalto sofre uma alteração representada pela equação a seguir.
Com base no enunciado, assinale a alternativa correta.
- A) Durante a descarga, o número de oxidação do cobalto aumenta.
- B) O cobalto recebe elétrons, para haver a recarga da bateria.
- C) No catodo, o cobalto é reduzido durante a descarga.
- D) O íon de lítio se desloca para o catodo, durante a descarga, devido à atração magnética.
- E) O solvente utilizado entre os polos deve ser um líquido orgânico apolar.
Resposta:
A alternativa correta é letra C
Análise das alternativas:
a) Incorreta.Drante a a descarga o número do cobalto passa de 4+ para 3+.
b) Incorreta. O cobalto recebe elétrons na descarga e perde elétrons na recarga.
c) Correta. O número de oxidação do cobalto diminui,consequentemente ele sofre redução.
d) Incorreta. O íon de lítio se desloca para o catôdo durante a descarga, devido a atração eletrostática.
e) Incorreta.O solvente utilizando entre os polos deve ser um líquido polar pois o Li+ seria solúvel nesse sistema.
a) Incorreta.Drante a a descarga o número do cobalto passa de 4+ para 3+.
b) Incorreta. O cobalto recebe elétrons na descarga e perde elétrons na recarga.
c) Correta. O número de oxidação do cobalto diminui,consequentemente ele sofre redução.
d) Incorreta. O íon de lítio se desloca para o catôdo durante a descarga, devido a atração eletrostática.
e) Incorreta.O solvente utilizando entre os polos deve ser um líquido polar pois o Li+ seria solúvel nesse sistema.

Deixe um comentário