Continua após a publicidade..
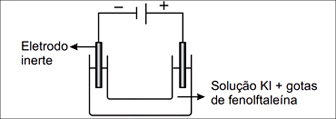
A uma solução aquosa contendo KI suficiente para tornar o meio condutor, foram adicionadas algumas gotas do indicador fenolftaleína. A solução resultante foi eletrolisada com eletrodos inertes, no dispositivo esquematizado a seguir.
São fornecidos os potenciais padrão de redução das espécies químicas presentes na solução, que podem sofrer óxido-redução no processo.
Com base nesses dados, pode-se prever que, durante a eletrólise da solução, haverá desprendimento de gás
- A) em ambos os eletrodos, e aparecimento de cor vermelha apenas ao redor do eletrodo negativo.
- B) em ambos os eletrodos, e aparecimento de cor vermelha apenas ao redor do eletrodo positivo.
- C) em ambos os eletrodos, e aparecimento de cor vermelha também ao redor dos dois eletrodos.
- D) somente do eletrodo positivo, e deposição de potássio metálico ao redor do eletrodo negativo.
- E) somente do eletrodo negativo, e aparecimento de cor vermelha apenas ao redor do mesmo eletrodo.
Resposta:
A alternativa correta é letra E
Tomar cuidado com as definições:
redução → eletrodo negativo → cátodo
oxidação →eletrodo positivo → ânodo
As reações que ocorrerão na pilha serão:
redução - cátodo
2H2O(l) + 2e-→ H2(g) + 2OH-(aq)
oxidação - ânodo
2I-(aq) → I2 + 2 e-
Reação geral
2H2O + 2I- → H2(g) + I2
No eletrodo negativo (cátodo) há o despreendimento de gás hidrogênio liberado pela reação, além do aparecimento da cor vermelha devido aos íons OH- em formação na solução

Deixe um comentário