Um gás ideal sofre uma expansão isotérmica, seguida de uma compressão adiabática. A variação total da energia interna do gás poderia ser nula se, dentre as opções abaixo, a transformação seguinte fosse uma
- A) compressão isocórica
- B) expansão isocórica
- C) expansão isobárica
- D) compressão isobárica
- E) compressão isotérmica
Resposta:
A alternativa correta é letra D) compressão isobárica
Gabarito: LETRA D.
Como o enunciado menciona, o gás ideal sofre primeiro uma expansão isotérmica. Em um diagrama PxV, essa transformação poderia ter o seguinte formato:
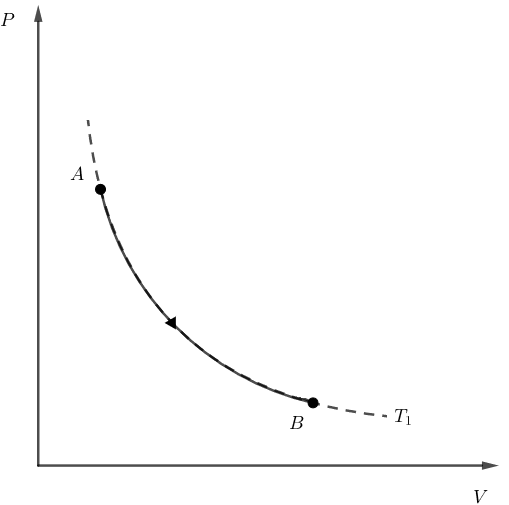
Ou seja, o processo A rightarrow B ocorre sobre uma isoterma.
Em seguida, o gás sofre uma compressão adiabática. Lembrando que, em uma compressão adiabática, ocorre uma diminuição de volume sem troca de calor, ou seja, Q = 0, então, de acordo com a primeira lei da termodinâmica, temos que:
Delta U_{B rightarrow C} = Q_{B rightarrow C} - W_{B rightarrow C}
Delta U_{B rightarrow C} = 0 - W_{B rightarrow C}
Delta U_{B rightarrow C} = - W_{B rightarrow C}
Como o gás sofre uma compressão, temos que W_{B rightarrow C} lt 0. Então, da equação acima, temos que Delta U_{B rightarrow C} gt 0, ou seja, a temperatura do gás aumenta, pois sabemos que Delta U = propto Delta T.
Assim, o diagrama PxV poderia ter o seguinte formato:
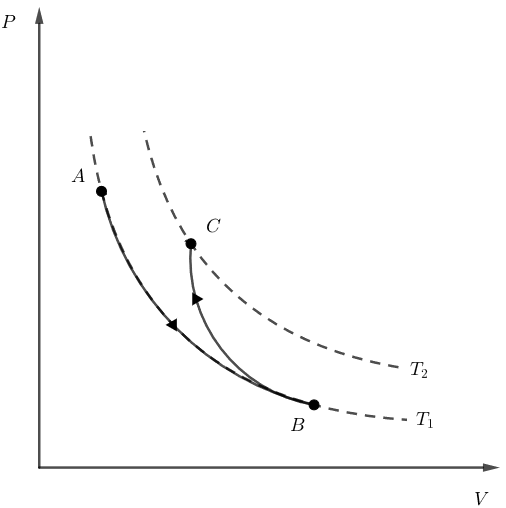
Agora, note que, para que a variação total da energia interna do gás seja nula, é necessário que o gás retorne ao ponto inicial, pois a energia interna é uma variável de estado, ou seja, o cálculo de sua variação depende apenas dos pontos inicial e final.
Assim, vamos analisar cada uma das alternativas:
a) compressão isocórica INCORRETA.
Em uma transformação isocórica, não há variação de volume. Logo, uma compressão (diminuição de volume) não é isocórica. Alternativa incorreta.
b) expansão isocórica INCORRETA.
Em uma transformação de expansão, há aumento de volume. Logo, essa transformação não é isocórica. Alternativa incorreta.
c) expansão isobárica INCORRETA.
Em uma transformação isobárica, não há variação de pressão. Assim, deveríamos ter P_A = P_C. Em um diagrama PxV, esse caso teria o seguinte formato:
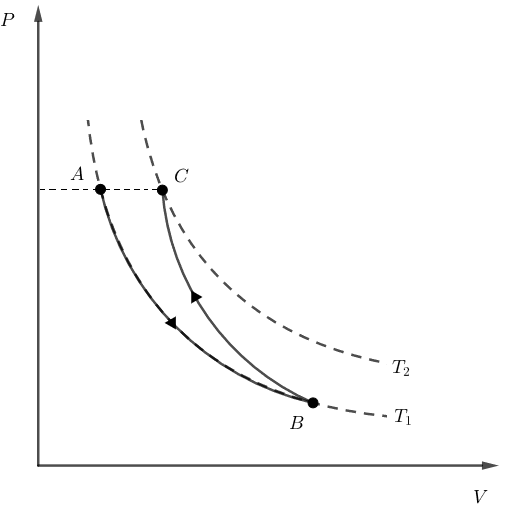
Note que, para que volte ao estado inicial A, o gás deveria sofrer uma compressão isobárica, e não uma expansão. Alternativa incorreta.
d) compressão isobárica CORRETA.
Como vimos na alternativa anterior, ao sofrer uma compressão isobárica, o gás poderia retornar para o estado inicial, como nos mostra o diagrama a seguir:
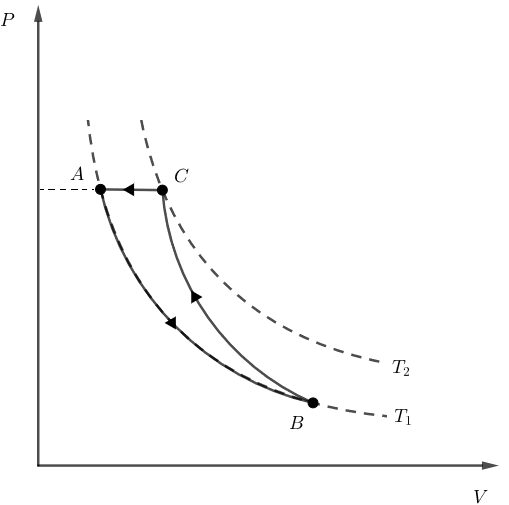
Assim, não haveria variação da energia interna total do gás. Logo, a alternativa está correta.
e) compressão isotérmica INCORRETA.
Como o gás deve retornar à temperatura inicial, ou seja, deve haver uma diminuição de temperatura, a transformação não pode ser isotérmica. Alternativa incorreta.
Portanto, a resposta correta é a alternativa (d).

Deixe um comentário