O gráfico abaixo indica o comportamento térmico de 10 g de uma substância que, ao receber calor de uma fonte, passa integralmente da fase sólida para a fase líquida.
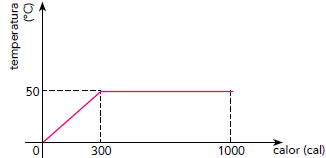
O calor latente de fusão dessa substância, em cal/g, é igual a:
- A) 70
- B) 80
- C) 90
- D) 100
Resposta:
A alternativa correta é letra A) 70
Gabarito: LETRA A.
Sabemos que, durante a mudança de fase, a temperatura da substância não varia.
Assim, observando o gráfico do enunciado, podemos afirmar que a substância inicia o processo de mudança de fase quando a quantidade de calor é 300 cal e passa integralmente da fase sólida para a fase líquida quando a quantidade de calor é 1000 cal, visto que a temperatura é mantida a 50° C.
Dessa forma, podemos afirmar que a quantidade de calor recebida durante a mudança de fase é dada por:
Q = 1000 - 300
Q = 700 , cal
Então, sendo m e L a massa e o calor latente de fusão da substância, respectivamente, temos que:
Q = m L
Logo,
L = dfrac { Q } { m }
L = dfrac { 700 , cal } { 10 , g }
L = 70 , cal/g
Portanto, a resposta correta é a alternativa (a).

Deixe um comentário