Durante um processo físico, a informação mais importante é a relativa à variação da entropia, e não a do seu valor absoluto. No século XIX, Clausius determinou que a variação da entropia de um sistema, em um processo reversível e à temperatura T, em Kelvin, é dada por DeltaS = DeltaQ/T, em que DeltaQ é a quantidade de calor adicionado. Com relação a esse conceito, considere a situação em que 30 g de gelo, inicialmente a 0 ºC, transforma-se em água a 0 ºC. Considere, ainda, que o calor latente de fusão do gelo seja 80 cal/g.
Com base nessas informações, julgue o próximo item.
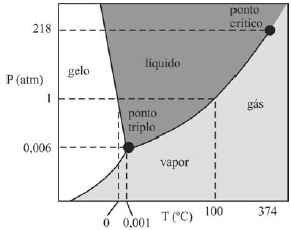
A figura a seguir ilustra uma possível representação do diagrama de fase da água, na qual consta o ponto triplo, região em que ocorrem, simultaneamente, os estados gasoso, líquido e sólido.
- A) Certo
- B) Errado
Resposta:
A resposta certa é A) Certo.
Para entender por que essa é a resposta certa, vamos analisar o problema. Temos 30 g de gelo a 0°C que se transformam em água a 0°C. Isso significa que houve uma mudança de fase do gelo para a água, e para isso, é necessário fornecer calor ao sistema. O calor fornecido é conhecido como calor latente de fusão, que no caso do gelo é de 80 cal/g.
Como a entropia é uma grandeza que mede a desordem ou a aleatoriedade de um sistema, durante a mudança de fase do gelo para a água, a entropia do sistema aumenta, pois as moléculas passam de um estado mais ordenado (sólido) para um estado mais desordenado (líquido). Essa variação de entropia é dada pela fórmula: ΔS = ΔQ / T, em que ΔQ é a quantidade de calor fornecida ao sistema e T é a temperatura em Kelvin.
No caso em questão, como a temperatura é de 0°C (ou 273 K), a variação de entropia pode ser calculada como: ΔS = 80 cal/g * 30 g / 273 K = 87,97 J/K. Ou seja, a variação de entropia do sistema é de aproximadamente 87,97 J/K.
Portanto, como a variação de entropia é uma grandeza importante para descrever o sistema, e não seu valor absoluto, a afirmativa está correta.
É importante notar que o diagrama de fase da água, apresentado na figura, mostra a região em que os estados gasoso, líquido e sólido coexistem, conhecida como ponto triplo. No entanto, isso não é relevante para a resolução do problema.

Deixe um comentário