No diagrama P x V da figura, A, B e C representam transformações possíveis de um gás entre os estados I e II.
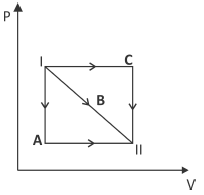
Com relação à variação
Δ∪ da energia interna do gás e ao trabalho W por ele realizado, entre esses estados, é correto afirmar que
- A) Δ∪_A=Δ∪_B=Δ∪_c e W_c>W_B>W_A
- B) Δ∪_A>Δ∪_c>Δ∪_B e W_c=W_A
- C) Δ∪_A<Δ∪_B<Δ∪_c e W_c>W_B>W_A
- D) Δ∪_A=Δ∪_B=Δ∪_c e W_c=W_A>W_B
- E)
Δ∪_A>Δ∪_B>Δ∪_c e
W_c=W_B=W_A
Resposta:
Resposta: A) $ΔU_A = ΔU_B = ΔU_c$ e $W_c > W_B > W_A$
A resposta correta para essa questão é a alternativa A. Isso ocorre porque, (ΔU) é a variação da energia interna do gás, entre os estados I e II. Como a variação da energia interna é a mesma para as transformações A, B e C, temos que $ΔU_A = ΔU_B = ΔU_c$.
Já para o trabalho (W) realizado pelo gás, temos que $W_c > W_B > W_A$. Isso ocorre porque o trabalho realizado é diretamente proporcional à área abaixo da curva no diagrama P x V. Como a área da transformação C é maior que a área da transformação B, e esta é maior que a área da transformação A, temos que o trabalho realizado pela transformação C é maior que o trabalho realizado pela transformação B, e este é maior que o trabalho realizado pela transformação A.
Portanto, a alternativa A é a correta, pois atende às condições estabelecidas para a variação da energia interna e para o trabalho realizado pelo gás.

Deixe um comentário