Um gás ideal monoatômico realiza as transformações ABCD indicadas no gráfico Pressão x Volume a seguir.
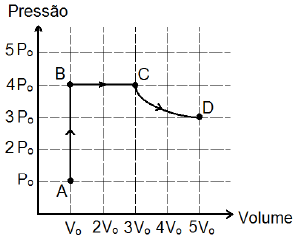
Em relação às temperaturas absolutas T_A, T_B, T_C e T_D respectivamente nos pontos A, B, C e D, é correta a relação
- A) T_A < T_B < T_C < T_D.
- B) T_A < T_B < T_C = T_D.
- C) T_A < T_B = T_C = T_D.
- D) T_A = T_B < T_C < T_D.
Resposta:
A alternativa correta é letra A) T_A < T_B < T_C < T_D.
Gabarito: LETRA A.
De acordo com a lei dos gases ideais, podemos escrever:
dfrac { P_A V_A } { T_A } = dfrac { P_B V_B } { T_B }
Logo,
T_B = dfrac { P_B V_B } { P_A V_A } cdot T_A
Da figura do enunciado, temos que P_A = P_0, P_B = 4 P_0 e V_A = V_B = V_0. Substituindo esse valores na equação acima, temos:
T_B = dfrac { 4cancel {P_0} cancel {V_0} } { cancel {P_0} cancel {V_0} } cdot T_A
T_B = 4 T_A
Logo,
T_A lt T_B
Analogamente para os pontos B e C, temos:
T_C = dfrac { P_C V_C } { P_B V_B } cdot T_B
Da figura do enunciado, temos que P_C = P_B = 4P_0 e V_C = 3 V_0. Substituindo esse valores na equação acima, temos:
T_C = dfrac { cancel {4 P_0} 3 cancel {V_0} } { cancel { 4P_0} cancel {V_0} } cdot T_B
T_C = 3 T_B
Logo,
T_A lt T_B lt T_C
Analogamente para os pontos C e D, temos:
T_D = dfrac { P_D V_D } { P_C V_C } cdot T_C
Da figura do enunciado, temos que P_D = 3P_0 e V_D = 5V_0. Substituindo esse valores na equação acima, temos:
T_D = dfrac { cancel 3 cancel {P_0} 5cancel {V_0} } { 4cancel {P_0} cancel 3 cancel {V_0} } cdot T_C
T_D = dfrac 54 cdot T_C
Logo,
T_A lt T_B lt T_C lt T_D
Portanto, a resposta correta é a alternativa (a).

Deixe um comentário