Muitos metais () em água, dependendo do pH da solução, formam hidróxidos () insolúveis.111111111111
Esse comportamento pode ser descrito pela equação (I), que relaciona o valor de pH com o logaritmo da concentração do metal (log []), para uma dada temperatura, em que
é a constante do produto de solubilidade do hidróxido do metal.
Equação (I): log[] = log (
) +14n – n (pH)
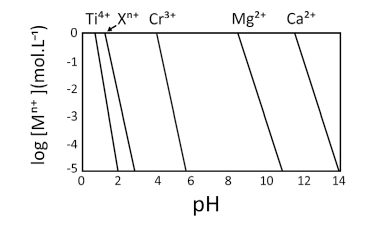
O comportamento da equação (I) é representado no gráfico, no qual as linhas mostram o valor de pH e log [] em que se inicia a precipitação de cada um dos metais. Em condições mais alcalinas do que a apresentada na linha de cada metal, será observada a espécie insolúvel como hidróxido e, em condições mais ácidas do que a apresentada na linha, será observada a espécie em sua forma solúvel.
a) Pinte, no gráfico da folha de respostas, a região onde o se encontra na forma solúvel e o
se encontra na forma de
insolúvel.
b) As linhas que representam e
possuem a mesma inclinação, mas diferem da inclinação daslinhas que representam
e
, que possuem a mesma inclinação entre si. Indique a carga n de
e justifique com base na equação (I).
c) Indique qual das espécies tem maior valor de :
ou
. Justifique com base nas informações dadas
Resposta:
a)
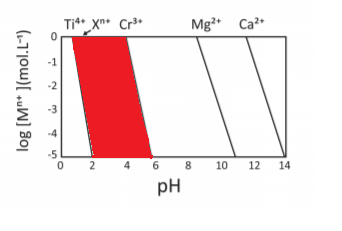
b)
Analisando a equação 1:
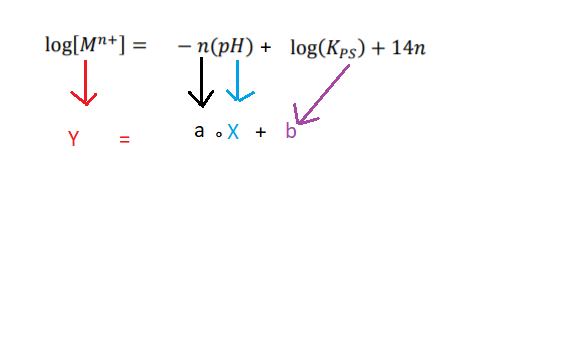
A inclinação da reta (a) é n ( carga do metal) , logo metais que possuem a mesma carga possuem a mesma inclinação, por iso a carga de X é +3.
c)´´b´´ está relacionada com o kps, onde eixo X corta a reta, então a reta maior b possuí o composto com maior Kps no caso o hidróxido de cálcio.

Deixe um comentário