O experimento conhecido como “chuva de ouro” consiste na recristalização, à temperatura ambiente, de iodeto de chumbo (). A formação desse sal pode ocorrer a partir da mistura entre nitrato de chumbo () e iodeto de potássio (). Outro produto dessa reação é o nitrato de potássio () em solução aquosa. Tanto o quanto o são sais brancos solúveis em água à temperatura ambiente, enquanto o é um sal amarelo intenso e pouco solúvel nessa temperatura, precipitando como uma chuva dourada.11111112222222

Em um laboratório, o mesmo experimento foi realizado em dois frascos. Em ambos, 100 mL de solução 0,1 de
e 100 mL de solução 0,2
de
foram misturados. Ao primeiro frasco foi também adicionado 20 mL de água destilada, enquanto ao segundo frasco foi adicionado 20 mL de solução 0,1
de iodeto de sódio (
).
A tabela a seguir apresenta os dados de solubilidade dos produtos da reação em diferentes temperaturas.

Responda aos itens a seguir considerando os dados do enunciado e o equilíbrio químico de solubilidade do iodeto de chumbo:
(s) ⇌
(aq) +
(aq)
a) Indique se o procedimento do segundo frasco favorece ou inibe a formação de mais sólido amarelo.
b) Para separar o precipitado da solução do primeiro frasco e obter o sólido e seco, foi recomendado que, após a precipitação, fosse realizada uma filtração em funil com papel de filtro, seguida de lavagem do precipitado com água para se retirar o
formado e, na sequência, esse precipitado fosse colocado para secar. Nesse caso, para se obter a maior quantidade do
, é mais recomendado o uso de água fria (4 °C) ou quente (80 °C)? Justifique.
c) Encontre a constante do produto de solubilidade () do iodeto de chumbo a 32 °C.
Resposta:
- O procedimento feito no segundo frasco favorece a formação do sólido amarelo,pois a solução de iodeto de sódio fornece íons I- ao meio:
NaI(aq)→Na+(aq) + I-(aq)
Esses íons deslocam o equilíbrio químico no sentido de formação do sólido PbI2(s).
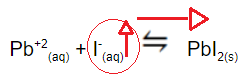
- Com o objetivo de aumentar o rendimento do processo para obter a maior quantidade de precipitado possível deve-se utilizar a água fria a 4ºC já que a solubilidade é menor como indicado na tabela, visando reduzir a perda de precipitado por solubilização durante a lavagem.
- Inicialmente vamos calcular a relação da solubilidade S com o Kps do iodeto de chumbo.
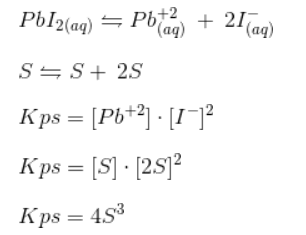
S é a solubilidade em mol/L , usando a fórmula n=m/mm , podemos transformar a concentração de g/L para mol/L:



Deixe um comentário