Prova de Química da UECE 2016 Resolvida
Questão 1
Atente aos seguintes compostos:
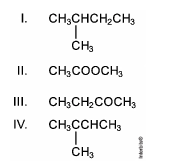
Considerando as reações dos compostos orgânicos acima, assinale a afirmação verdadeira.
- A) Há possibilidade de obter cinco diferentes substâncias monocloradas a partir de I.
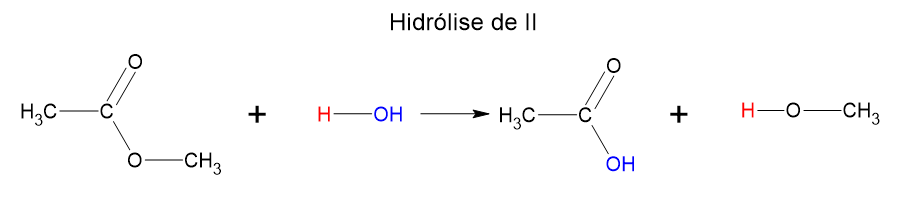
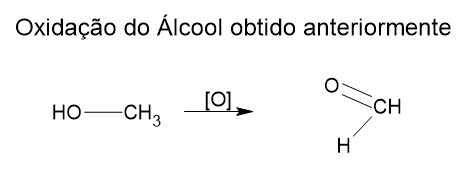
- B) A oxidação do álcool, obtido a partir da hidrólise de II, leva à formação do metanal.
- C) A substância III, em condições brandas, pode ser oxidada por uma solução neutra de KMnO4.
- D) Na oxidação enérgica, feita a quente com o composto IV, ocorre a formação de aldeído e ácido carboxílico.
A alternativa correta é letra B)
a) Incorreto. Há possibilidade de obter cinco diferentes substâncias monocloradas a partir de I.
São quatro diferentes substâncias monocloradas a partir de I:
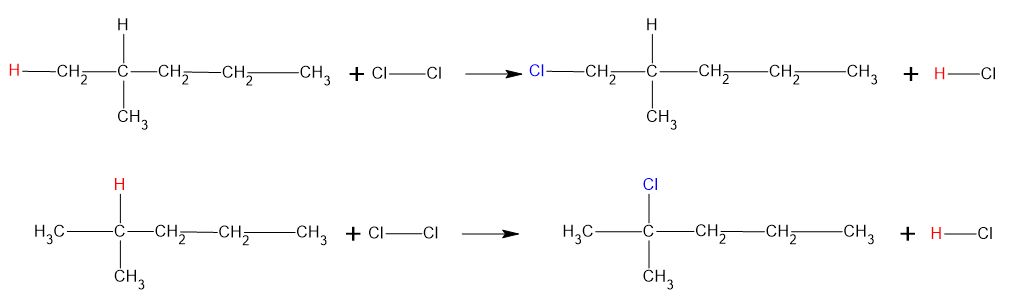
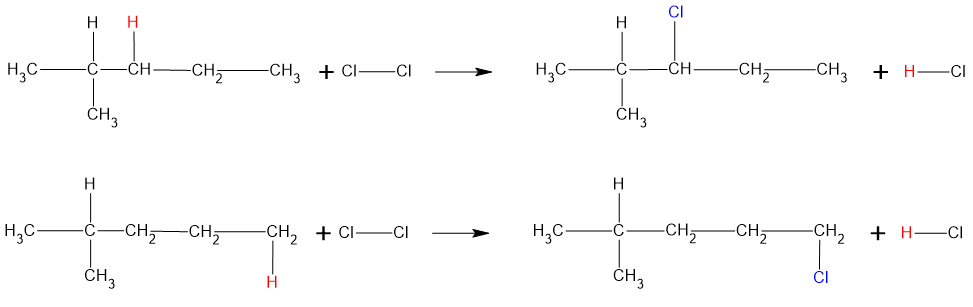
b) Correto. A oxidação do álcool, obtido a partir da hidrólise de II, leva à formação do metanal.
c) Incorreto. A substância III, em condições brandas, pode ser oxidada por uma solução neutra de KMnO4.
A oxidação de cetonas precisa de meio ácido e aquecimento (condição enérgica), não podendo então ser condição branda e solução neutra.
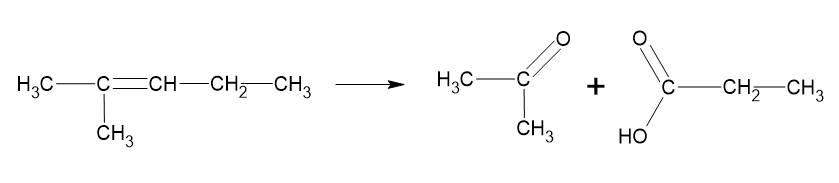
d) Incorreto. Na oxidação enérgica, feita a quente com o composto IV, ocorre a formação de aldeído e ácido carboxílico.
Um dos carbonos da dupla é um carbono terciário, produzindo uma cetona. Enquanto o outro carbono é secundário, produzindo um ácido carboxílico.
2) No laboratório de Química foi realizada uma experiência, cujo procedimento foi o seguinte:
- A) A vitamina C promove a oxidação do iodo a iodeto de hidrogênio.
- B) A descoloração da solução ocorre porque a vitamina C promove a redução do iodeto de hidrogênio a iodo.
- C) A reação química da vitamina C com a solução de lugol é:
- C) C6H8O6 + 2 HI → C6H6O6 + I2 + 2 H2
- D) Na reação química, a vitamina C atua como redutor.
A alternativa correta é letra D)
Método do Íon-elétron
1) Balanceios elementos que não sejam O e H
2) Balancei os O com H2O
3) Balancei os H com H+
4) Balancei cargas com e-
__________________________________________
a) A vitamina C promove a oxidação do iodo a iodeto de hidrogênio. ❌
O nox variou de 0 para -1 o iodo reduziu
b) A descoloração da solução ocorre porque a vitamina C promove a redução do iodeto de hidrogênio a iodo. ❌
Falsa, a redução é de iodo a iodeto de hidrogênio como pode ser verificado na reação montada acima
c) A reação química da vitamina C com a solução de lugol é: ❌
Falsa, como vimos na reação montada acima
d) Na reação química, a vitamina C atua como redutor. ✔️
Verdadeiro, o nox variou de 0 para -1 o iodo reduziu
a vitamina C é o agente redutor
3) O fermento é responsável pelo aumento do volume de um bolo, que acontece assim: a temperatura alta faz com que o fermento libere gás carbônico; esse gás se expande e faz o bolo crescer. Quando adicionado na massa, o fermento sofre uma transformação química a partir da reação entre bicarbonato de sódio e fosfato di-hidrogenado de cálcio:
- A) Ca2(PO4)3 + 4Na2HPO4 + 8CO2 + 8H2O
- B) Ca3(PO4)2 + 4NaHPO4 + 8CO2 + 8H2O
- C) Ca3(PO4) + 4Na2HPO4 + 8CO2 + 8H2O
- D) Ca3(PO4)2 + 4Na2HPO4 + 8CO2 + 8H2O
A alternativa correta é letra D)
[D]
Teremos a seguinte reação química:
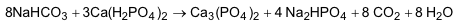
Questão 4
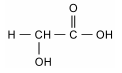
Atente ao que se diz a respeito dessa substância:
I. Essa substância é um éster.
II. Libera H+ quando se encontra em solução aquosa.
III. Uma diminuição da concentração de H+ leva também a uma diminuição do pH.
IV. Na reação de ionização, essa substância se transforma na seguinte espécie:
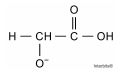
É correto o que se afirma somente em
- A) I e III.
- B) II.
- C) I e IV.
- D) II, III e IV.
A alternativa correta é letra B)

5) (Uece 2016) Os químico alemães Fritz Haber (1868-1934) e Carl Bosch (1874-1940) desenvolveram, em 1909, um processo de produção de amônia, matéria-prima para a fabricação de explosivos utilizados durante a Primeira Guerra Mundial. De acordo com o processo Haber, a obtenção da amônia se faz através da reação:
- A) quebrar as ligações entre os átomos de hidrogênio.
- B) quebrar as ligações entre os átomos de nitrogênio.
- C) melhorar, simultaneamente, o rendimento da amônia e a velocidade da reação.
- D) reorganizar a estrutura na molécula da amônia.
A alternativa correta é letra B)
6) (Uece 2016) O Prêmio Nobel de Química de 2015 foi para três pesquisadores que descobriram mecanismos biomoleculares naturais que reparam erros no DNA (ácido desoxirribonucleico), que contém as informações para o desenvolvimento e o funcionamento dos seres vivos. O DNA é relativamente instável e sua composição pode ser danificada por diversos fatores. Os pesquisadores Lindahl, Sancar e Modrich descobriram mecanismos que existem em praticamente todos os seres vivos e servem como “caixas de ferramentas” naturais para corrigir esses defeitos que surgem espontaneamente.
- Sua cadeia principal é formada por bases halogenadas e resíduos de açúcar dispostos alternadamente.É um longo polímero de unidades simples (monômeros) de nucleotídeos, cuja cadeia principal é formada por moléculas de açúcares e fosfato.Os três filamentos que compõem a sua estrutura enrolam-se, um sobre o outro, formando uma tripla hélice, semelhante a um espiral de caderno, podendo ter milhares de nucleotídeos.É um composto orgânico constituído por uma desoxirribose e um grupo nitrogenado.
A alternativa correta é letra B)
None7) (Uece 2016) Josiah Willard Gibbs (1839-1903) foi um pesquisador norte-americano que contribuiu para a determinação da energia livre de um sistema termodinâmico através de uma lei que é associada ao seu nome. Em se tratando de energia livre e de entropia, analise as seguintes proposições:
- A) I e II.
- B) III e IV.
- C) I, III e V.
- D) II, IV e V.
A alternativa correta é letra D)

8) (Uece 2016) Em um laboratório de Química, foi realizada uma experiência, adotando-se o seguinte procedimento:
- A) A equação química da reação do tubo de ensaio que contém o hidróxido de sódio é
- B) A equação química da reação do tubo de ensaio que contém o ácido clorídrico é
- C) O gás liberado nos dois tubos de ensaio após a adição de alumínio é o O2.
- D) Por essa experiência, pode-se afirmar acertadamente que o emprego do ácido muriático (ácido clorídrico comercial) deve ser indicado para a limpeza de uma escada de alumínio.
2 Al(s) + 2 NaOH(aq) + 2 H2O(l) → 2 NaAlO2(aq) + 3 H2(g)
2 Al(s) + 6 HCl(aq) → 2 AlH3 (aq) + 3 Cl2(g)
A alternativa correta é letra A)
B) Reações entre metais não-nobres sempre formam hidrogênio e sal:
4 Al + 6 HCl 2 Al2Cl3 + 3 H2
C) Em ambos é liberado H2.
D) Falso, pois o ácido ira corroer a escada.
Nesse caso, resta a letra A como resposta.
A) O alumínio possui caráter anfótero e pode reagir tanto com ácidos como com bases. Com bases, o alumínio reage formando um sal de aluminato e gás hidrogênio.
Há outros metais que reagem com base também liberando H2, o estanho, o chumbo e zinco.
9) (Uece 2016) Os clorofluorcarbonos, descobertos por Thomas Midgley Jr. (1899-1944), não são tóxicos, nem reativos, nem explosivos e foram bastante utilizados em extintores, refrigerantes, propelentes de aerossol e, posteriormente, como agente refrigerante em geladeiras e aparelhos de ar condicionado. Tais gases, no entanto, estão causando a destruição da camada de ozônio. No que diz respeito a clorofluorcarbonos e ozônio, assinale a afirmação verdadeira.
- A) Os CFCs também produzem chuva ácida e o efeito estufa.
- B) Na estratosfera, são decompostos pela radiação infravermelha e liberam cloro, que ataca o ozônio produzindo monóxido de cloro e oxigênio.
- C) Na troposfera, grandes quantidades de ozônio acarretam poluição atmosférica.
- D) Aumentos na radiação infravermelha podem aumentar o ozônio na estratosfera, acarretando o aquecimento global.
A alternativa correta é letra C)
a) [Errada] Os CFCs também produzem chuva ácida e o efeito estufa.
O principal efeito dos CFCs é a destruição da camada de ozônio, não sendo associado ao efeito estufa ou chuva ácida.
b) [Errada] Na estratosfera, são decompostos pela radiação infravermelha e liberam cloro, que ataca o ozônio produzindo monóxido de cloro e oxigênio.
A radiação que decompõe o CFC é a radiação ultravioleta (UV) e não a infravermelha.
c) [Correta] Na troposfera, grandes quantidades de ozônio acarretam poluição atmosférica.
O Ozônio (O3) presente na estratosfera é um agente poluidor. Podendo causar a oxidação de óxidos de enxofre acarretando um agravamento da chuva ácida por ser um poderoso agente oxidante.
d) [Errada] Aumentos na radiação infravermelha podem aumentar o ozônio na estratosfera, acarretando o aquecimento global.
A radiação infravermelha não produz o Ozônio, o correto seria a radiação UV.
Questão 10
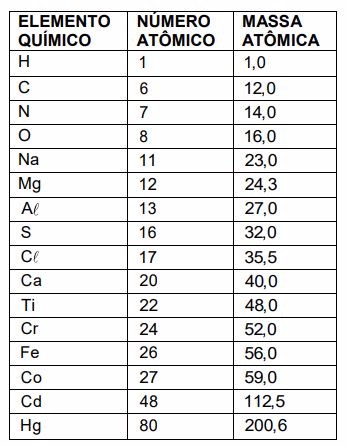
A titulação é um procedimento laboratorial que permite determinar a concentração desconhecida de uma substância a partir de uma substância de concentração conhecida. Em uma titulação representada pela equação: 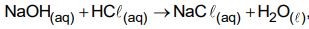 , equipamento usado para adicionar cuidadosamente o volume adequado da solução de NaOH é denominado
, equipamento usado para adicionar cuidadosamente o volume adequado da solução de NaOH é denominado
- A) pipeta graduada.
- B) proveta.
- C) bureta.
- D) pipeta volumétrica.
A alternativa correta é letra C)
O equipamento utilizado para mensurar constantemente a quantidade de base (NaOH) adicionada ao meio reacional é a bureta, que está representada esquematicamente abaixo: