Continua após a publicidade..
O benzeno, um importante solvente para a indústria química, é obtido industrialmente pela destilação do petróleo. Contudo, também pode ser sintetizado pela trimerização do acetileno catalisada por ferro metálico sob altas temperaturas, conforme a equação química:1
3C2H2(g)  C6H6(ℓ)
C6H6(ℓ)
A energia envolvida nesse processo pode ser calculada indiretamente pela variação de entalpia das reações de combustão das substâncias participantes, nas mesmas condições experimentais:
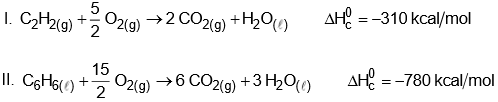
A variação de entalpia do processo de trimerização, em kcal, para a formação de um mol de benzeno é mais próxima de
- A) - 1090
- B) - 150
- C) - 50
- D) + 157
- E) + 470
Resposta:
A alternativa correta é letra B)
Pela estequiometria das reações I e II, temos que a variação de entalpia é 3I – II.
3 C2H2 (g) + 15/2 O2 (g) → 6 CO2 (g) + 3 H2O (l) ΔHo =3.(-310) = -930 kcal
6 CO2 (g) + 3 H2O (l) → C6H6 (l) + 15/2 O2 (g) ΔHo = +780 kcal
ΔHo = 3I – II = 3.(-310) – (-780) = -930+780 = -150
LETRA B

Deixe um comentário