A respeito das características estruturais dos aminoácidos, substâncias orgânicas que constituem as proteínas, julgue o seguinte item.
Para formar peptídeos, os aminoácidos se unem por meio de ligações peptídicas que se estabelecem entre o grupo amino e o grupo R de dois aminoácidos diferentes.
- A) Certo
- B) Errado
Resposta:
A alternativa correta é letra B) Errado
Gabarito da banca: ERRADO.
Entendimento: ERRADO.
Acompanhe a análise:
Estamos falando de peptídeos, que é o encadeamento organizado de aminoácidos.
Para as provas de concurso mais exigentes, considero importante aprofundar a explicação. Assim, lembre-se que uma ligação peptídica é formada por uma extremidade aminoterminal, uma extremidade carbonoterminal e uma cadeia lateral (R). A cadeia lateral pode ser: alifática (apolar), aromática, hidrofílica, ácida (carga negativa), básica (carga positiva). Veja o esquema:
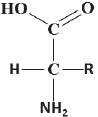
A ligação peptídica forma-se entre o átomo de carbono (C) do grupo carboxílico e o átomo de nitrogênio do grupo amina, e essa ligação se dá pela eliminação de água. Os peptídeos formam-se, portanto, por reação de polimerização de condensação de aminoácidos. Por que condensação? Lembro que reações de condensação são as que ocorrem com liberação de molécula de água.
Os aminoácidos são ligados em sequência através de ligações peptídicas. Como são muitos aminoácidos ligados, as ligações peptídicas formam cadeias polipeptídicas. Para seu estudo, considere importante que a ligação peptídica tem duas características: primeiro, ela é rígida e planar; segundo, a conformação trans reduz choques estéricos entre os grupos R da cadeia lateral. Sobre essa segunda característica, merece sua atenção que a configuração trans se dá pela rotação da cadeia lateral e da extremidade carbonoterminal em torno do grupo amina. Como resultado da rotação, ocorre o enovelamento da proteína.

Deixe um comentário