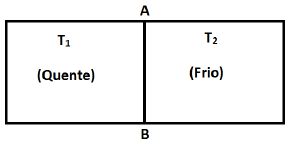
A figura ao lado mostra um sistema composto por um recipiente, separado em dois compartimentos de mesmo volume. Os dois compartimentos contêm massas iguais do mesmo gás, 0,6 gramas em cada um, e o calor específico a volume constante (cv) do gás é 0,18 cal/g°C. Inicialmente, o gás quente está a 67 °C, e o gás frio a 20 °C. Não existe fluxo de calor, exceto, lentamente, através da partição AB.
Sobre a variação da entropia, afirma-se que
I. a variação da entropia do gás no recipiente quente é negativa.
II. a variação da entropia do gás no recipiente frio é positiva.
III. como a variação da entropia do gás em cada recipiente possui o mesmo valor absoluto, a variação da energia total do universo é nula.
IV. a entropia total do universo aumentou como resultado desse processo.
Está(ão) correta(s) apenas a(s) afirmação(ões)
- A) III.
- B) I e II.
- C) I, II e III.
- D) I, II e IV.
Resposta:
A resposta correta é a letra D) I, II e IV.
Vamos analisar cada afirmação para entender por que essa é a resposta correta:
I. A variação da entropia do gás no recipiente quente é negativa.
Isso é verdade porque, quando o gás quente se expande e perde calor, sua entropia diminui.
II. A variação da entropia do gás no recipiente frio é positiva.
Isso também é verdade porque, quando o gás frio absorve calor e se expande, sua entropia aumenta.
III. Como a variação da entropia do gás em cada recipiente possui o mesmo valor absoluto, a variação da energia total do universo é nula.
Essa afirmação é falsa. Embora as variações de entropia sejam iguais em magnitude, elas têm sinais opostos (uma é positiva e a outra é negativa). Portanto, a variação total da entropia do universo não é nula.
IV. A entropia total do universo aumentou como resultado desse processo.
Isso é verdade porque, embora a entropia do gás quente tenha diminuído, a entropia do gás frio aumentou mais. Portanto, a entropia total do universo aumentou.
Portanto, as afirmações I, II e IV são verdadeiras, e a resposta correta é a letra D) I, II e IV.

Deixe um comentário