A figura representa o gráfico da pressão versus a temperatura do processo cíclico ABCA sofrido por um gás ideal monoatômico.
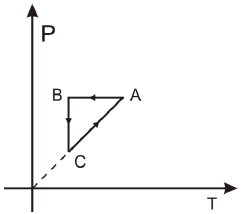
O gráfico pressão versus volume equivalente as transformações ABCA é:
- A)
- B)
- C)
- D)
Resposta:
A resposta certa é a letra D). O gráfico de pressão versus volume é caracterizado por uma isoterma (processo A), uma adiabata (processo BC) e outra isoterma (processo CA). Isso ocorre porque o gás ideal monoatômico sofre expansão isoterma (A), compressão adiabática (B) e compressão isoterma (C).
Na transformação A, a temperatura é constante, portanto, a isoterma é uma linha horizontal no gráfico de pressão versus volume. Já na transformação BC, a entalpia do gás aumenta, pois a temperatura aumenta durante a compressão adiabática, portanto, a adiabata é uma linha inclinada no gráfico de pressão versus volume. Finalmente, na transformação CA, a temperatura é novamente constante, portanto, a isoterma é outra linha horizontal no gráfico de pressão versus volume.
O gráfico de pressão versus temperatura é caracterizado por uma linha reta que passa pela origem, pois a pressão é diretamente proporcional à temperatura em um gás ideal monoatômico. Portanto, apenas a opção D) apresenta o gráfico correto de pressão versus temperatura para o processo cíclico ABCA.
É importante notar que o gráfico de pressão versus volume também pode ser utilizado para analisar o processo cíclico ABCA. Nesse caso, o gráfico apresentaria uma isoterma (A), uma adiabata (B) e outra isoterma (C). No entanto, como a questão pede o gráfico de pressão versus temperatura, a resposta certa é a opção D).





Deixe um comentário