Certa quantidade de gás sofre três transformações sucessivas, A rightarrow B, B rightarrow C e C rightarrow A, conforme o diagrama p-V apresentado na figura abaixo.
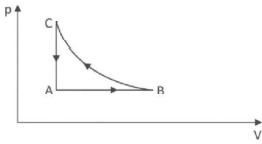
A respeito dessas transformações, afirmou-se o seguinte:
I. O trabalho total realizado no ciclo ABCA é nulo.
II. A energia interna do gás no estado C é maior que no estado A.
III. Durante a transformação A rightarrow B, o gás recebe calor e realiza trabalho.
Está correto apenas o que se afirma em
- A) I.
- B) II.
- C) III.
- D) I e II.
- E) II e III.
Note e adote: o gás deve ser tratado como ideal; a transformação B rightarrow C é isotérmica .
Resposta:
A alternativa correta é letra E) II e III.
Note e adote:
o gás deve ser tratado como ideal;
a transformação B rightarrow C é isotérmica .
Os gases realizam trabalho W de compressão ou expansão, conforme a seguinte expressão:
W = - PcdotDelta{V}
Então, notamos que o trabalho de um gás é função do produto da pressão pelo volume do gás. Sendo assim, a afirmação I de que o trabalho realizado no ciclo ABCA é nulo é FALSA.
O primeiro princípio da termodinâmica afirma que a quantidade de calor (Q) fornecida a um sistema é igual ao trabalho realizado pelo gás (tau) mais a variação da energia interna (Delta U) sofrida por ele.
Q=tau + Delta U
A energia interna de um gás depende exclusivamente de sua temperatura. Calculando a temperatura do gás nos dois estados através da equação de Clapeyron, teremos:
frac{pcdot V}{T}=ncdot R ,,, implies ,,, T=dfrac{pcdot V}{ncdot R}
Do ponto C para o ponto A ocorre uma transformação isovolumétrica. Pela equação de Clapeyron, nessa condição tanto a pressão quanto a temperatura diminuem de C para A. Logo, podemos afirmar que se a temperatura em C é maior do que em A, então a energia interna do gás em C também é maior do que em A. Assertiva II é verdadeira.
De A rightarrow B o gás passa por uma transformação isobárica. Pela equação de Clapeyron, como o volume do gás aumenta, a temperatura também aumenta. Logo, ocorrerá aumenta da energia interna do gás e a realização de trabalho pelo gás.
tau>0
Delta U>0 e
Q>0
E assim, confirmamos que de A rightarrow B o gás recebe calor (Q>0) e realiza trabalho (tau>0). Assertiva III é verdadeira.
Gabarito: E

Deixe um comentário