Considere o diagrama de fases do CO2 esboçado na figura abaixo.
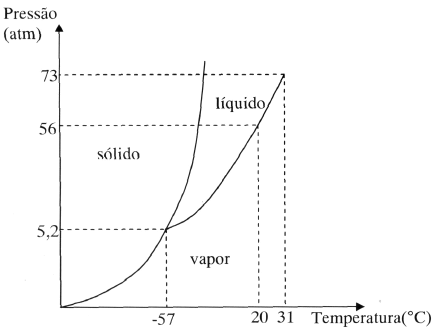
Uma dada quantidade de CO2, inicialmente à pressão de 1 atm e temperatura de 15 ºC, é submetida às seguintes transformações: uma transformação isotérmica até a pressão de 60 atm, seguida de uma redução isobárica da temperatura até –70 ºC e, posteriormente, uma redução de isotérmica de pressão até 6 atm.
É CORRETO afirmar que, nessas transformações, o CO2 irá passar, sequencialmente, pelas seguintes fases:
- A) vapor, sólido, líquido e vapor.
- B) vapor, líquido, sólido e vapor.
- C) vapor, líquido e sólido.
- D) líquido e sólido.
Resposta:
A resposta correta é a letra C) vapor, líquido e sólido.
Para entender por que essa é a resposta correta, vamos analisar as transformações sofridas pelo CO2 nas condições dadas.
Inicialmente, o CO2 encontra-se a uma pressão de 1 atm e temperatura de 15°C. Em seguida, é submetido a uma transformação isotérmica até a pressão de 60 atm. Nessa etapa, o CO2 está no estado de vapor.
Em seguida, ocorre uma redução isobárica da temperatura até -70°C. Nessa etapa, o CO2 condensa e passa para o estado líquido.
Por último, ocorre uma redução isotérmica da pressão até 6 atm. Nessa etapa, o CO2 pode passar para o estado sólido, uma vez que se encontra abaixo da curva de fusão do diagrama de fases.
Portanto, durante essas transformações, o CO2 passou sequencialmente pelos estados de vapor, líquido e sólido, o que corrobora a alternativa C) como a resposta correta.

Deixe um comentário