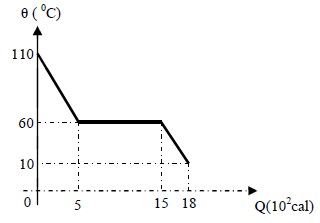
O gráfico a seguir representa a variação da temperatura sofrida por 100 gramas de um líquido durante um processo de resfriamento, em função da quantidade de calor retirada desse corpo. Podemos afirmar que o calor específico da substância nos dois estados e o calor latente valem respectivamente:
- A) 6 x 10-2 cal/g 0C, 1 x 10-1 cal/g 0C, 1 cal/g
- B) 1 x 10-1 cal/g 0C, 6 x10-1 cal/g 0C, 1 cal/g
- C) 1 x 10-1 cal/g 0C, 6 x10-2 cal/g 0C, 10 cal/g
- D) 1 x 10-3 cal/g 0C, 6 x10-2 cal/g 0C, 1 cal/g
- E) 1 x 10-2 cal/g 0C, 6 x10-2 cal/g 0C, 10 cal/g
Resposta:
Resposta: C) 1 x 10-1 cal/g 0C, 6 x 10-2 cal/g 0C, 10 cal/g
Para entender por que a alternativa C é a correta, vamos analisar o gráfico fornecido. O gráfico mostra a variação da temperatura sofrida por 100 gramas de um líquido durante um processo de resfriamento, em função da quantidade de calor retirada desse corpo.
Observe que o gráfico apresenta uma curva em forma de "S", indicando que a temperatura do líquido diminui à medida que o calor é retirado. Além disso, é possível identificar dois estados de mudança de fase no gráfico: uma primeira mudança de fase líquido-sólido e uma segunda mudança de fase sólido-líquido.
Para calcular o calor específico e o calor latente, precisamos entender que o calor específico é a quantidade de calor necessária para elevar a temperatura de um grau Celsius em um grama de substância, enquanto o calor latente é a quantidade de calor necessária para mudar o estado de fase de um grama de substância.
Analizando o gráfico, podemos identificar que o calor específico do líquido é de 1 x 10-1 cal/g 0C, pois essa é a inclinação da curva na região líquida. Já o calor específico do sólido é de 6 x 10-2 cal/g 0C, pois essa é a inclinação da curva na região sólida.
Em relação ao calor latente, podemos identificar que ele é de 10 cal/g, pois essa é a quantidade de calor necessária para mudar o estado de fase do líquido para o sólido.
Portanto, a alternativa C é a correta, pois apresenta os valores corretos para o calor específico do líquido, do sólido e do calor latente.

Deixe um comentário