O gráfico pressão (P) em função do volume (V) a seguir representa três caminhos A, B e C diferentes em que uma mesma amostra de gás ideal pode ir do estado inicial “i” para o estado final “f”.
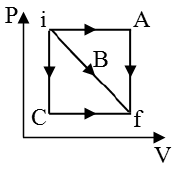
Assinale a alternativa que indica corretamente a relação entre os valores, em módulo, das quantidades de calores QA, QB, e QC envolvidos, respectivamente, nos caminhos A, B e C.
- A) QA = QB = QC
- B) QA > QB > QC
- C) QA < QB < QC
- D) QB > QA e QB > QC
Resposta:
A alternativa correta é letra B) QA > QB > QC
Gabarito: LETRA B.
De acordo com a primeira lei da termodinâmica, temos:
Delta U = Q - W
Logo,
Q = Delta U + W tag 1
Como os três caminhos possuem os mesmos pontos inicial e final, podemos afirmar que Delta U_A = Delta U_B = Delta U_C.
Lembrando que o trabalho realizado pelo gás é numericamente igual à área sob a curva do gráfico de pressão em função do volume, observando o gráfico do enunciado, podemos afirmar que:
W_A gt W_B gt W_C tag 2
Então, de (1) e (2), temos que:
Q_A gt Q_B gt Q_C
Portanto, a resposta correta é a alternativa (b).

Deixe um comentário