Questões Sobre Termologia - Física - concurso
991) O mês de agosto de 2011 foi de umidade relativa do ar muito baixa, atingindo valores abaixo de 15%, que é considerada uma situação de desertos, onde os dias são muito quentes, e as noites são frias.
- A) alto calor específico.
- B) baixa capacidade térmica.
- C) alta condutividade térmica.
- D) alta densidade.
A alternativa correta é letra A) alto calor específico.
Gabarito: LETRA A.
A umidade relativa do ar é importante para reduzir as diferenças de temperatura devido ao alto calor específico da água. O calor específico é a quantidade de calor necessária para elevar a temperatura de uma substância em uma quantidade determinada. Isso significa que a água pode absorver uma quantidade considerável de calor antes de sua temperatura aumentar significativamente.
Quando o ar possui uma umidade relativa adequada, a água presente no ar absorve o calor do ambiente durante o dia, quando há maior exposição solar, evitando que a temperatura aumente drasticamente. À noite, essa água libera gradualmente o calor, ajudando a manter as temperaturas mais altas e reduzindo as diferenças de temperatura entre o dia e a noite. Nesse caso, a água atua como um regulador térmico, moderando as variações extremas de temperatura.
Portanto, a resposta correta é a alternativa (a).
992) Numa aula de laboratório em Barbacena, cidade cuja altitude média é de 1 160 m, um professor de Física pediu a seus alunos que observassem a água que fervia numa vasilha sem tampa.
- A) os três alunos.
- B) Carolina e Sílvia.
- C) apenas Sílvia.
- D) Daniel e Sílvia.
A alternativa correta é letra B) Carolina e Sílvia.
Gabarito: LETRA B.
Vamos analisar cada uma das afirmações:
Daniel: A água está fervendo a 100ºC. INCORRETA.
A temperatura de ebulição da água varia de acordo com a pressão atmosférica. Em altitudes elevadas como Barbacena, a pressão atmosférica é menor do que ao nível do mar, o que faz com que a temperatura de ebulição da água seja menor do que 100ºC. Ou seja, a água está fervendo a uma temperatura abaixo de 100ºC em Barbacena.
Sílvia: Enquanto a água está fervendo, a temperatura da água não muda. CORRETA.
Quando a água está fervendo, sua temperatura permanece constante durante esse processo. Isso ocorre porque toda a energia térmica fornecida está sendo utilizada para romper as ligações intermoleculares e transformar a água do estado líquido para o estado gasoso (vapor de água).
Carolina: A água está passando do estado líquido para o gasoso. CORRETA.
Quando a água está fervendo, ela está passando do estado líquido para o estado gasoso (vapor de água). Esse processo é conhecido como ebulição ou fervura.
Portanto, a resposta correta é a alternativa (b).
993) Um professor explica à sua turma que, quando se fornece calor a uma amostra de gelo a 0 ºC, a temperatura do gelo não se altera. Em vez disso, ocorre a fusão do gelo. Este é um exemplo de mudança de fase. Em seguida, solicita à turma a resolução da seguinte questão: quantas calorias precisam ser fornecidas a 100 gramas de gelo a –10 ºC para que este se funda e se transforme em água líquida na temperatura de 40 ºC, considerando calor específico da água = 1,00 frac{kcal}{kg.K}, calor específico do gelo a -10 ºC = 0,49 frac{kcal}{kg.K} e calor latente de fusão do gelo = 80,0 frac{kcal}{kg.K} ?
- A) 4,90 kcal.
- B) 6,25 kcal.
- C) 12,49 kcal.
- D) 40,00 kcal.
- E) 62,50 kcal.
The correct answer is C) . To understand why,<|begin_of_text|>2019-07-15,22:30
Let's break down the problem step by step:
First, we need to calculate the energy required to raise the temperature of the 100 g of ice from -10°C to 0°C. We can use the specific heat capacity of ice, which is 0.49 kcal/kg°C. The temperature change is 10°C, so:
Q = mcΔT = 100 g × 0.49 kcal/kg°C × 10°C = 49 kcal
Next, we need to calculate the energy required to melt the 100 g of ice at 0°C. The latent heat of fusion of ice is 80 kcal/kg, so:
Q = mL = 100 g × 80 kcal/kg = 8000 kcal
Finally, we need to calculate the energy required to raise the temperature of the resulting 100 g of water from 0°C to 40°C. We can use the specific heat capacity of water, which is 1 kcal/kg°C. The temperature change is 40°C, so:
Q = mcΔT = 100 g × 1 kcal/kg°C × 40°C = 4000 kcal
Adding up the energies required for each step, we get:
Total energy = 49 kcal + 8000 kcal + 4000 kcal = 12,049 kcal ≈ 12,49 kcal
Therefore, the correct answer is C) 12,49 kcal.
994) Talvez a cidade mais fria do mundo seja Oymyakon, na Sibéria, onde a temperatura chega aos incríveis 213 K nos piores dias de inverno.
- A) − 32 ºC
- B) − 60 ºC
- C) − 100 ºC
- D) − 213 ºC
- E) − 273 ºC
A alternativa correta é letra B) − 60 ºC
Pessoal, precisamos passar de Kelvin para Celsius.
Basicamente é o sentido inverso do que estamos acostumados.
Sem delongas,
T_K = T_C + 273
T_C = 213 - 273 = - 60 ºC
Gabarito: LETRA B.
995) Considerando o calor específico da água igual a 1 cal/g ºC, qual a quantidade de calor necessária para elevar a temperatura de 20 g de água da temperatura inicial de 10 ºC para a temperatura final de 45 ºC?
- A) 35 cal
- B) 150 cal
- C) 200 cal
- D) 350 cal
- E) 700 cal
A alternativa correta é letra E) 700 cal
Pessoal, clássica questão de aplicação de
Q = m c Delta T
Q = 20 times 1 times (45 - 10) = 700 , cal
Reparem que não precisamos sequer fazer transformação de unidades.
As dimensões já estavam nas unidades necessárias (olhar para a unidade de c).
Gabarito: LETRA E.
996) Um recipiente de alumínio está totalmente cheio com 350 cm3 de glicerina.
- A) 0,119
- B) 0,154
- C) 3,5
- D) 7
- E) 10
A alternativa correta é letra C) 3,5
Pessoal, reparem que a questão pede a variação volumétrica da glicerina.
Os dados do alumínio foram fornecidos apenas para gerar confusão.
Delta L = L_0 alpha Delta T
Delta L = 350 times 5 times 10^{-4} times (40 - 20) = 3,5 , cm^3
Gabarito: LETRA C.
997) Um tanque contendo um fluido incompressível é agitado por um equipamento que entrega 2.500 kJ de trabalho.
- A) 750
- B) 1.750
- C) 2.500
- D) 3.250
- E) 3.500
A alternativa correta é letra D) 3.250
Pessoal, aqui sem muito segredo.
Temos a aplicação direta de
Delta U = Q - W
750 = Q - 2.500
Q = 3.250 , kJ
Gabarito: LETRA D.
Questão 998
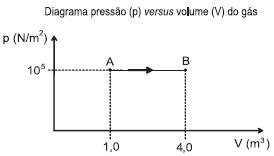
De acordo com a primeira lei da termodinâmica, a energia interna do gás sofre um(a)
- A) aumento de 2 x 105 J
- B) diminuição de 2 x 105 J
- C) aumento de 3 x 105 J
- D) diminuição de 3 x 105 J
- E) aumento de 5 x 105 J
A alternativa correta é letra A) aumento de 2 x 105 J
Pessoal, clássica aplicação de
Delta U = Q - W
Delta U = 5 times 10^5 - 10^5 times (4 - 1)
Delta U = 2 tiems 10^5 , J
Gabarito: LETRA A.
Questão 999
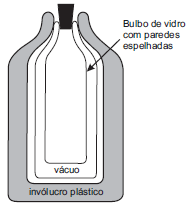
Certas características da garrafa térmica são responsáveis pela redução das trocas de calor entre o interior e o exterior da garrafa.
A transferência de calor por convecção e por radiação são reduzidas, respectivamente, por causa do
- A) invólucro de plástico e do vácuo entre as paredes de vidro
- B) espelhamento das paredes de vidro e do vácuo entre as paredes de vidro
- C) espelhamento das paredes de vidro e do invólucro de plástico
- D) vácuo entre as paredes de vidro e do invólucro de plástico
- E) vácuo entre as paredes de vidro e do espelhamento das paredes de vidro
A alternativa correta é letra E) vácuo entre as paredes de vidro e do espelhamento das paredes de vidro
Pessoal, reparem que a questão pede o que é preciso fazer para reduzir convecção e radiação respectivamente.
A convecção é a transferência de calor por meio fluido (líquido ou gasoso).
A radiação, por sua vez, é a transferência de calor que ocorre por qualquer meio (até mesmo vácuo).
O vácuo reduz a convecção, visto que para que esta ocorra é necessário um meio fluido.
A radiação, como ocorre em qualquer meio, precisa ser refletida ("devolvida").
Logo,
Gabarito: LETRA E.
1000) Uma expedição de pesquisa chega a um local ermo. Os pesquisadores descobrem que levaram o termômetro errado para medir a temperatura ambiente. Ele havia sido graduado em uma escala X que, em água fervente a 1 atm, indica 80 °X e que, em gelo fundente a 1 atm, indica 30 °X.
- A) 10
- B) 20
- C) 30
- D) 40
- E) 50
A alternativa correta é letra B) 20
Pessoal, fazendo a interpolação, teremos
dfrac{100 - C}{80 - 40} = dfrac{100-0}{80-30}
No lado DIREITO, reparem que temos a temperatura de ebulição e congelamento em Celsius no numerador e a temperatura de ebulição e congelamento em X no denominador.
Já no lado ESQUERDO, temos a interpolação com Ebulição nas duas escalas bem como a temperatura pedida.
dfrac{100-C}{40} = dfrac{100}{50}
C = 20 °C
Gabarito: LETRA B.
