Questões Sobre Termologia - Física - concurso
1061) Com relação à calorimetria, assinale a opção INCORRETA.
- A) Para uma dada pressão, cada substância possui uma temperatura fixa de fusão e outra temperatura fixa de vaporização.
- B) Para uma mesma substância a uma determinada pressão, a temperatura de solidificação coincide com a de fusão, bem como a temperatura de liquefação coincide com a de vaporização.
- C) Se um cubo de gelo está em fusão, pode-se afirmar que a temperatura permanece constante e ocorre absorção de calor.
- D) A capacidade térmica é uma propriedade da substância, e o calor específico é uma propriedade do corpo.
- E) Quando um cubo de gelo é aquecido de 0ºC a 100ºC, a água se contrai e depois se dilata.
A alternativa correta é letra D) A capacidade térmica é uma propriedade da substância, e o calor específico é uma propriedade do corpo.
Vamos verificar afirmativa por afirmativa pessoal.
a) Para uma dada pressão, cada substância possui uma temperatura fixa de fusão e outra temperatura fixa de vaporização.
CORRETA. Realmente pessoal, as temperaturas de fusão e vaporização tem relação com a pressão. Quando a pressão aumenta, a temperatura de vaporização também aumenta, via de regra.
b) Para uma mesma substância a uma determinada pressão, a temperatura de solidificação coincide com a de fusão, bem como a temperatura de liquefação coincide com a de vaporização.
CORRETA. Um aumento de temperatura acima da temperatura de solidificação irá causar fusão e uma diminuição de temperatura causa solidificação. Na liquefação, o comportamento é análogo conforme sugere a questão.
c) Se um cubo de gelo está em fusão, pode-se afirmar que a temperatura permanece constante e ocorre absorção de calor.
CORRETA. A fusão da água (gelo) ocorre a temperatura constante pessoal.
d) A capacidade térmica é uma propriedade da substância, e o calor específico é uma propriedade do corpo.
INCORRETA. Pessoal, a questão trocou os conceitos. Capacidade térmica é propriedade do corpo e calor específico da substância.
e) Quando um cubo de gelo é aquecido de 0ºC a 100ºC, a água se contrai e depois se dilata.
CORRETA. Essa característica é própria da água. Entre 0 e 5 graus, a água se contrai com aquecimento ao invés de se expandir como os outros materiais. Após essa faixa, ela se dilata normalmente conforme esperado quando aumentamos a temperatura.
Gabarito: LETRA D.
Questão 1062
Analise a figura abaixo.
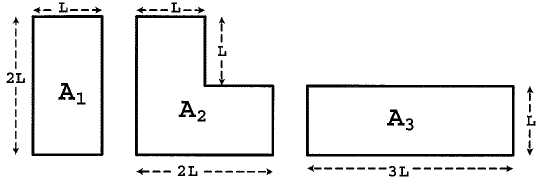
Três placas metálicas retangulares feitas do mesmo material possuem áreas A1, A2 e A3, cujas dimensões estão indicadas na figura acima. Considerando que elas sofrem um aumento de temperatura de mesmo valor, pode-se afirmar que o aumento das áreas das placas, triangle,A_1, triangle,A_2,,e,triangle,A_3 se relacionam por:
- A) triangle,A_1 = triangle,A_2 = triangle,A_3
- B) triangle,A_1 = triangle,A_2,e,triangle,A_1 <triangle,A_3
- C) triangle,A_3 < triangle,A_1< triangle,A_2
- D) triangle,A_1 < triangle,A_2,e,triangle,A_2 = triangle,A_3
- E) triangle,A_2 > triangle,A_3 > triangle,A_1
A alternativa correta é letra D) triangle,A_1 < triangle,A_2,e,triangle,A_2 = triangle,A_3
Pessoal, vamos calcular a área de cada uma delas.
A_1 = 2L times L = 2L^2
A_2 = L times L + L times 2L = 3 L^2
A_3 = 3L^2
Agora, pessoal, reparem que o aumento de área é dado por
Delta A = A alpha Delta T
Como os materiais são os mesmos e a variação de temperatura também, temos que a única influência que diferencia cada dilatação será a área de cada material.
Percebam que elas são diretamente proporcional, quanto maior a área inicial maior a dilatação.
Logo, a primeira área é a que menos vai aumentar e a segunda terá um mesmo aumento que a terceira (visto terem a mesma área 3L2),
triangle,A_1 < triangle,A_2,e,triangle,A_2 = triangle,A_3
Gabarito: LETRA D.
1063) Calor intenso e permanência de temperaturas elevadas por vários dias refletem-se necessariamente na expansão do consumo residencial de energia elétrica. Considere um consumo médio residencial de 160 kWh por mês. No Rio de Janeiro, onde o consumo cresceu aproximadamente 16%, a temperatura máxima na capital chegou a ficar, em média, no início do verão, 7 °C acima da esperada. Considere que o calor específico da água é 4,2 J/g °C. Os 16% de energia a mais consumida no período de um mês em um domicílio seriam suficientes para aquecer de 7 °C aproximadamente quantos quilogramas de água?
- A) 0,87⋅103.
- B) 3,1⋅103.
- C) 3,7⋅103.
- D) 23⋅103.
A alternativa correta é letra B) 3,1⋅103.
Gabarito: LETRA B.
Primeiro, vamos calcular os 16% de energia a mais consumida no período de um mês em um domicílio cujo consumo médio residencial é de 160 kWh por mês:
E_{adicional} = 16% cdot E_{médio}
E_{adicional} = 0,16 cdot 160
E_{adicional} = 25,6 , kWh
E_{adicional} = 25,6 times 10^3 , Wh
Agora, vamos converter essa energia de kWh para joules, lembrando que 1 , Wh = 3,6 times 10^3 , J:
E_{adicional} = 25,6 times 10^3 cdot 3,6 times 10^3 , J
E_{adicional} approx 9,21 times 10^7 , J
Então, vamos calcular a massa de água que pode ser aquecida utilizando essa energia adicional consumida. Usaremos o calor específico da água (4,2 J/g °C) e a variação de temperatura (7 °C):
Q = mc Delta T
A energia adicional é transferida na forma de calor. Logo,
E = mc Delta T
m = dfrac { E }{c Delta T}
Substituindo os valores, temos:
m = dfrac { 9,21 times 10^7 cancel J }{ 4,2 dfrac { cancel J } { g cancel{°C} } cdot 7 cancel{°C} }
m approx 3,1 times 10^6 , g
m approx 3,1 times 10^3 , kg
Portanto, a resposta correta é a alternativa (b).
1064) Satélites artificiais, como os usados em transmissão de TV, têm sistemas eletrônicos instalados e que se aquecem por efeito Joule. Além disso, as partes do satélite que estejam voltadas para o sol estão expostas a temperaturas em torno de 300 K, enquanto as partes sombreadas ficam em um ambiente de 2,7 K. A geração de calor por efeito Joule e essas diferenças de temperatura exigem um projeto muito sofisticado no tocante à dissipação de calor. Considerando que o satélite esteja fora da atmosfera terrestre, onde não haja um meio condutor de calor para o ambiente, podese afirmar corretamente que a principal forma de dissipação de calor do satélite é
- A) difusão.
- B) irradiação.
- C) condução.
- D) convecção.
A alternativa correta é letra B) irradiação.
Gabarito: LETRA B.
As formas de dissipação de calor são os processos pelos quais um corpo ou sistema transfere energia térmica para o ambiente, buscando atingir um equilíbrio térmico. Dentre elas, podemos destacar três principais formas:
1. Condução: É a transferência de calor que ocorre em meios materiais (sólidos, líquidos ou gases) através de colisões entre partículas. Em sólidos, a condução é mais eficiente, pois as partículas estão mais próximas umas das outras. Nos fluidos (líquidos e gases), a condução é menos eficiente.
2. Convecção: A convecção ocorre em fluidos (líquidos e gases) e envolve o movimento das massas do fluido. O calor é transferido quando o fluido quente, que se torna menos denso, sobe e o fluido mais frio, que se torna mais denso, desce. Esse processo forma correntes de convecção que transferem calor.
3. Irradiação: É a forma de transferência de calor através de ondas eletromagnéticas (radiação térmica). Todos os objetos com temperatura acima do zero absoluto emitem radiação térmica. A irradiação não requer um meio material para transferir o calor e é efetiva mesmo no vácuo.
Assim, podemos afirmar que a principal forma de dissipação de calor do satélite fora da atmosfera terrestre é a irradiação, já que não há um meio material para transferir o calor no vácuo do espaço.
Portanto, a resposta correta é a alternativa (b).
1065) A massa de oxigênio (O_2) que está contido num recipiente ideal de volume igual a 40,18 dm^3 , sob pressão de 5 atm e temperatura de 77º C , é igual a:
- A) 112 g
- B) 184 g
- C) 224 g
- D) 312 g
A alternativa correta é a letra C) 224 g.
Vamos calcular a massa de oxigênio (O2) contida no recipiente ideal de volume igual a 40,18 dm³, sob pressão de 5 atm e temperatura de 77°C.
Primeiramente, vamos utilizar a equação de estado dos gases ideais:
$PV = nRT$
Onde:
- $P$ é a pressão do gás (5 atm)
- $V$ é o volume do recipiente (40,18 dm³)
- $n$ é o número de moles do gás
- $R$ é a constante universal dos gases ($R = 0,082 atm.L / (mol.K)$)
- $T$ é a temperatura em Kelvin (350 K)
Agora, podemos rearranjar a equação para encontrar o número de moles do gás:
$n = frac{PV}{RT}$
Substituindo os valores, temos:
$n = frac{(5 atm)(40,18 dm^3)}{(0,082 atm.L / (mol.K))(350 K)} = 7,0 mol$
Para encontrar a massa do oxigênio, multiplicamos o número de moles pelo peso molecular do oxigênio:
$m = nM = (7,0 mol)(32 g/mol) = 224 g$
Portanto, a massa de oxigênio contida no recipiente é igual a 224 g.
Questão 1066
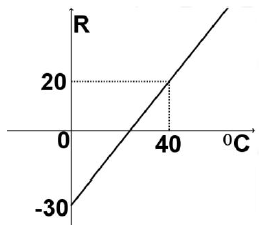
- A) 250
- B) 260
- C) 265
- D) 270
A temperatura de fusão do estanho é de 232°C. Para encontrar a temperatura equivalente na escala R, podemos analisar o gráfico fornecido.
O gráfico apresenta uma relação direta entre as escalas de temperatura R e Celsius. Podemos observar que a temperatura de 0°C é igual a 491,7 R e a temperatura de 100°C é igual a 671,7 R.
Para encontrar a temperatura de 232°C na escala R, podemos usar a fórmula de conversão:
TR = 491,7 + (TC - 0) × (671,7 - 491,7) / (100 - 0)
Onde TR é a temperatura em R e TC é a temperatura em Celsius.
Substituindo os valores, obtemos:
TR = 491,7 + (232 - 0) × (671,7 - 491,7) / (100 - 0)
TR ≈ 260 R
Portanto, a temperatura de fusão do estanho na escala R é de aproximadamente 260 R.
A alternativa correta é a letra B) 260.
Questão 1067
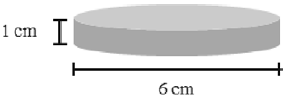
Sabendo que o paciente se encontra à temperatura de 38 °C, assinale a opção que apresenta corretamente o acréscimo sofrido pelo raio da peça, em micrômetros, ao entrar em equilíbrio térmico com o paciente.
- A) 10,8
- B) 16,2
- C) 21,6
- D) 5,4
- E) 8,1
A alternativa correta é letra A) 10,8
Quando a campânula do estetoscópio atingir o equilíbrio térmico no contato com o paciente, a peça também estará a temperatura de 38 °C. A expressão que define a variação no volume de um corpo é dada por:
Delta{V}=V_0cdot gamma cdot Delta{theta}tag 1
Onde V_0 é o volume inicial, gamma é é o coeficiente de dilatação volumétrica e Delta{theta} é a variação de temperatura.
No entanto, prezados alunos, não precisaremos calcular a variação de volume da peça. Por que não? Porque o enunciado solicita o acréscimo sofrido pelo raio da peça. E sabemos que o raio é uma dimensão linear. Portanto, deveremos obter o coeficiente de dilatação linear a partir do coeficiente de dilatação volumétrica. Vejamos então a expressão para a variação linear do material:
Delta{L}=L_0cdot alpha cdot Delta{theta}tag 2
Onde alpha é coeficiente de dilatação linear. No entanto:
alpha=frac{gamma}{3}
alpha=frac{60times10^{-6}}{3}
alpha=20times10^{-6}
Agora iremos aplicar a equação 2 para o cálculo da variação linear no comprimento do raio:
Delta{L}=3times10^{-2}times 20times10^{-6}times (38 -20)
Delta{L}=60times10^{-8}times 18
Delta{L}=1.080times10^{-8}
Delta{L}=10,8times10^{-6}
Delta{L}=10,8mu,m
Analisando as alternativas, o gabarito é a letra A.
Gabarito: Letra A.
Questão 1068
O bisturi elétrico atua como um terminal carregado.
O tecido atua como um resistor que fecha o circuito e permite a passagem de corrente, que aquece a região. A corrente varia de acordo com o tecido, a região, entre outros fatores. Abaixo, está representada a variação da corrente que percorre um trecho de tecido durante 8 segundos.
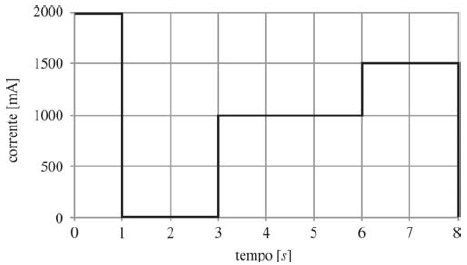
Considere que a região do tecido percorrida pela corrente, no primeiro segundo, tenha massa de 50 g e calor específico constante e igual a 1,25 J·g-1·K-1. Assumindo-se que toda a energia tenha sido convertida em calor e que não tenha havido perdas para os tecidos vizinhos, o aumento de temperatura nessa região foi de
- A) 42,5 K.
- B) 53,1 K.
- C) 64,0 K.
- D) 24,0 K.
- E) 33,0 K.
A alternativa correta é letra C) 64,0 K.
A quantidade de calor fornecida ou recebida por um corpo é definida pela seguinte expressão:
Q=mcdot ccdot Delta{theta}tag 1
Onde c é o valor específico do corpo que recebe o calor e Delta{theta} é a variação de temperatura. Como o tecido está recebendo calor, a variação de temperatura será positiva.
Conforme a questão de número 1837928, a energia transferida ao tecido durante o primeiro segundo foi de:
E= 4cdot 10^3times1=4cdot 10^3,J
Então, usaremos a equação (1) para calcular a elevação de temperatura do tecido:
4cdot 10^3=50cdot 1,25cdot Delta{theta}
4cdot 10^3=62,5cdot Delta{theta}
boxed{Delta{theta}=64,K}
Logo, concluímos que o nosso gabarito é a letra C.
Gabarito: C
1069) Em um calorímetro (instrumento utilizado em laboratórios de física para estudar trocas de calor), inicialmente com 150g água (calor específico 1,0 frac{cal}{g.ºC}) a uma temperatura de 10 , é colocado um bloco metálico homogêneo, de 200g, e com temperatura de 90 . Considerando que a temperatura de equilíbrio atingida é de 30 . e desprezando a capacidade térmica do calorímetro, qual o calor específico do metal que constitui o bloco?
- A) 0,15 frac{cal}{g.ºC}
- B) 0,25 frac{cal}{g.ºC}
- C) 0,5frac{cal}{g.ºC}
- D) 0,75frac{cal}{g.ºC}
Resposta: B) 0,25 cal/g°C
Para encontrar o calor específico do metal que constitui o bloco, vamos utilizar a fórmula da troca de calor entre dois corpos: Q = mcΔT, onde Q é a quantidade de calor trocada, m é a massa do corpo, c é o calor específico do corpo e ΔT é a variação de temperatura.
No problema, temos dois corpos: a água e o bloco metálico. A água tem uma massa de 150g e uma temperatura inicial de 10°C. O bloco metálico tem uma massa de 200g e uma temperatura inicial de 90°C. Depois da troca de calor, a temperatura de equilíbrio é de 30°C.
Vamos considerar que a água perde calor e o bloco metálico ganha calor. A quantidade de calor perdida pela água é igual à quantidade de calor ganha pelo bloco metálico. Portanto, podemos escrever:
Q_água = -Q_bloco
Substituindo a fórmula da troca de calor, temos:
m_água * c_água * ΔT_água = -m_bloco * c_bloco * ΔT_bloco
Substituindo os valores dados, temos:
150g * 1,0 cal/g°C * (30°C - 10°C) = -200g * c_bloco * (30°C - 90°C)
Simplificando a equação, obtemos:
c_bloco = 0,25 cal/g°C
Portanto, o calor específico do metal que constitui o bloco é de 0,25 cal/g°C, que é a alternativa B.
1070) Em um calorímetro ideal (completamente adiabático) mistura-se 200 g de água (cH20 = 1 cal ⁄ Co) a 80o com 500 g de um material (cujo calor específico é 0,4 cal ⁄ Co) a 20o.
- A) 10o
- B) 20o
- C) 30o
- D) 40o
- E) 50o
Para resolver essa questão, vamos aplicar o conceito de mistura de calor entre dois corpos. Nesse caso, temos 200 g de água a 80°C e 500 g de um material desconhecido a 20°C. Quando misturamos esses dois corpos, eles alcançam um estado de equilíbrio térmico, onde a temperatura final é a mesma para ambos.
Para calcular a temperatura final, vamos utilizar a fórmula de mistura de calor:
$$Q_1 = -Q_2$$$$m_1 cdot c_1 cdot Delta T_1 = m_2 cdot c_2 cdot Delta T_2$$
Onde:
- $Q_1$ é a quantidade de calor perdida pela água;
- $Q_2$ é a quantidade de calor ganha pelo material;
- $m_1$ é a massa da água (200 g);
- $m_2$ é a massa do material (500 g);
- $c_1$ é o calor específico da água (1 cal/g°C);
- $c_2$ é o calor específico do material (0,4 cal/g°C);
- $Delta T_1$ é a variação de temperatura da água;
- $Delta T_2$ é a variação de temperatura do material;
Substituindo os valores, temos:
$$200 cdot 1 cdot (80 - T_f) = -500 cdot 0,4 cdot (T_f - 20)$$
Resolvendo a equação, encontramos:
$$T_f = 50°C$$
Portanto, a alternativa correta é a letra E) 50°C.
OBS: É importante notar que a temperatura final é inferior à temperatura inicial da água, pois o material absorveu calor da água, fazendo com que a temperatura final seja menor que 80°C.
