Questões Sobre Termologia - Física - concurso
Questão 1101
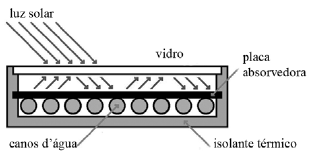
Considere que a intensidade da luz solar incidente seja igual a 500 W/m2 e que 60% dessa intensidade seja utilizada para aquecer a água. Considere, ainda, que a área da placa absorvedora seja de 2 m2 e que o coeficiente de dilatação linear do material que a compõe seja α = 20 × 10-6 ºC-1. Considere, por fim, que a água tenha máxima densidade à temperatura de 4 ºC e que c= 4.190 frac {J} {kg.K} seja o calor específico, considerado constante.
Com base nessas informações, julgue o item subsequente.
Considerando que a água esteja presa nos canos, é correto afirmar que a sua pressão aumentará quando a temperatura cair de 4 ºC para 3 ºC.
- A) Certo
- B) Errado
A alternativa correta é letra A) Certo
Quando a temperatura de um corpo cai, o comportamento comum é que seu volume diminua. Porém, a água se comporta de modo diferente no intervalo de 0 à 4ºC. Neste intervalo, a queda na temperatura provoca um aumento do volume, como a água esta presa nos canos a pressão aumentará.
Resposta: O item está CERTO
1102) Na termodinâmica, a parte do universo selecionada para a análise das mudanças de energia é denominada sistema, sendo a vizinhança o restante do universo. Alguns tipos particulares de transformações são considerados no estudo da termodinâmica, assim como o processo.
- A) fusotérmico
- B) ecotérmico
- C) coloritérmico
- D) exotérmico
- E) endotérmico
A alternativa correta é letra E) endotérmico
Resposta: Alternativa E
Processos exotérmicos são aqueles que liberam calor. O principal exemplo é a combustão.
Processos endotérmicos são aqueles que absorvem calor. Para que o gelo se funda é necessário que ele absorva calor, portanto, a fusão é um processo endotérmico.
1103) Uma chaleira contendo um litro de água à temperatura de 20 ºC é colocada no fogão para ferver. A temperatura de ebulição da água no local é de 100 ºC.
- A) 8 cal, 8 g
- B) 80 kcal, 10 g
- C) 100 kcal, 10 g
- D) 80 kcal, 8 g
- E) 80 kcal, 80 g
A alternativa correta é letra B) 80 kcal, 10 g
Pessoal, reparem nas alternativas que o erro estará nas casas decimais.
Um litro de água equivale a 1.000 g.
Logo,
Q = m c Delta T = 1.000 times 1 times (100-20) = 80 , kcal
A quantidade de massa requerida de gás é de 8 g para uma eficiência de 100%.
Para uma eficiência de 80, precisamos corrigir
m_{gas} = dfrac{8}{0,8} = 10 , g
Gabarito: LETRA B.
1104) Sobre um sistema termodinâmico realiza-se um trabalho de 100 J. Em seguida, o sistema perde 50 J de calor. Ao final desses processos, a variação de energia interna do sistema, em joules, é igual a:
- A) 50
- B) 150
- C) -50
- D) -150
- E) 100
A alternativa correta é letra A) 50
A primeira lei da termodinâmica diz que:
Q = W + Delta U,
sendo Q o calor, W o trabalho realizado e Delta U a variação da energia interna.
Notemos que foi realizado um trabalho sobre o sistema. Isso significa que W é negativo.
Além disso, o sistema perdeu calor. Portanto, Q é negativo.
Assim, substituindo os valores na equação, obtemos
-50 = Delta U + (-100)
100 - 50 = Delta U
Delta U = 50
1105) Em um laboratório aquece-se, uniformemente, uma chapa metálica com um furo no meio. Assinale a opção que representa o que acontece com o furo e a chapa após o aquecimento.
- A) O furo contrai e a chapa dilata.
- B) Nada acontece.
- C) O furo dilata e a chapa contrai.
- D) Furo e chapa contraem.
- E) O furo e a chapa dilatam.
A alternativa correta é letra E) O furo e a chapa dilatam.
Quando um corpo é aquecido, suas dimensões aumentam proporcionalmente à variação de temperatura.
Por essa razão, uma confusão comum é achar que o buraco no meio da placa diminuirá. Entretanto, é fundamental lembrar que a expansão provocada pelo aumento de temperatura mantém todas as proporções do corpo. Então, o raio do circulo interno deve aumentar. Vejamos em uma figura como a expansão ocorre:

Colocando as figuras antes e depois da expansão teremos:

Assim, concluímos que a chapa e o furo dilatam.
1106) Uma escala arbitrária X adota os valores -20 e 200 para os pontos do gelo e vapor de água. A temperatura na escala X que corresponde a 30°C é:
- A) 46
- B) 80
- C) 54
- D) 68
- E) 90
A alternativa correta é letra A) 46
(NOTA: a temperatura de 300^oC está ERRADA, deveria ser 30^oC)
Para estabelecermos a relação entre duas escalas de temperatura, devemos estabelecer a proporção entre os seguimentos em duas retas numeradas:

Então fazemos a proporção entre os segmentos:
frac{t -(-20)}{200 - (-20)} = frac{30 - 0}{100 - 0}
frac{t +20}{220} = frac{30}{100}
t +20 = frac{30.220}{100}
t +20 = 3.22
t = 66 - 46
t = 46^o X
1107) Uma certa quantidade de água encontra-se numa vasilha a 1ºC à pressão atmosférica quando é aquecida até atingir a temperatura de 6ºC. Nesta situação podemos afirmar, em relação ao volume, que ele:
- A) diminui.
- B) aumenta.
- C) aumenta e a seguir diminui.
- D) diminui e a seguir aumenta.
- E) aumenta, a seguir diminui e finalmente aumenta.
Resposta: D) diminui e a seguir aumenta.
Quando a água é aquecida, sua temperatura aumenta e, consequentemente, sua energia cinética também aumenta. Isso faz com que as moléculas de água sejam mais agitadas e ocupem mais espaço, fazendo com que o volume da água aumente.
Porém, há um fator que influencia nesse processo: a pressão atmosférica. Quando a água é aquecida, sua expansão é limitada pela pressão atmosférica, que não permite que o volume aumente indefinidamente. Isso faz com que, inicialmente, o volume da água diminua devido à compressão exercida pela pressão atmosférica.
À medida que a temperatura da água continua a aumentar, a expansão térmica se torna mais intensa e o volume da água começa a aumentar novamente. Portanto, a alternativa correta é D) diminui e a seguir aumenta.
Explicação:
A expansão térmica é um fenômeno comum em muitos materiais, incluindo a água. Quando um material é aquecido, as suas moléculas ganham energia cinética e se movimentam mais rapidamente, ocupando mais espaço. Isso faz com que o volume do material aumente.
No entanto, quando se trata de um líquido como a água, a pressão atmosférica também desempenha um papel importante. A pressão atmosférica é a força exercida pela atmosfera sobre a superfície da Terra e, consequentemente, sobre o líquido. Quando a água é aquecida, a pressão atmosférica tenta comprimir o líquido, reduzindo seu volume.
Portanto, ao analisar a questão, é importante considerar tanto a expansão térmica quanto a pressão atmosférica. Isso explica por que a alternativa correta é D) diminui e a seguir aumenta.
1108) Sabendo que o calor de fusão do gelo é 80 cal/g, que o calor específico do gelo é 0,5 cal/gºC e que o calor específico da água líquida é 1,0 cal/gºC, calcular a energia necessária para transformar 100 gramas de gelo a – 10 ºC em água a 10 ºC.
- A) 7500 cal
- B) 6000 cal
- C) 6500 cal
- D) 8500 cal
- E) 9500 cal
Resposta: 9500 cal
Para calcular a energia necessária para transformar 100 gramas de gelo a –10°C em água a 10°C, precisamos considerar as seguintes etapas:
1. Aumento de temperatura do gelo de –10°C para 0°C:
Q₁ = m × c × ΔT
Q₁ = 100 g × 0,5 cal/g°C × 10°C = 500 cal
2. Fusão do gelo a 0°C:
Q₂ = m × L
Q₂ = 100 g × 80 cal/g = 8000 cal
3. Aumento de temperatura da água de 0°C para 10°C:
Q₃ = m × c × ΔT
Q₃ = 100 g × 1,0 cal/g°C × 10°C = 1000 cal
A energia total necessária é a soma das energias necessárias para cada etapa:
Q-total = Q₁ + Q₂ + Q₃ = 500 cal + 8000 cal + 1000 cal = 9500 cal
Portanto, a alternativa correta é a letra E) 9500 cal.
1109) Um turista estrangeiro em visita a Cidade do Natal observou um termômetro em via pública que marcava uma temperatura de 35 °C. Sabendo se que em seu país de origem as temperaturas são medidas na escala Fahrenheit (F), o valor marcado no termômetro corresponde à
- A) 98 F.
- B) 95 F.
- C) 100 F.
- D) 102 F.
A alternativa correta é letra B) 95 F.
Para converter temperaturas da escala Celsius para Fahrenheit (e vice-versa) utilizamos a seguinte equação:
frac{C}{5} = frac{F - 32}{9}
A questão nos pergunta qual será a temperatura em Fahrenheit dado que em Celsius o termômetro marcada 35 °C. Vamos então substituir esse valor na equação e determinar sua equivalente em Fahrenheit.
frac{35}{5} = frac{F - 32}{9}
7 cdot 9 = F - 32
F = 95
Portanto, 35 °C equivalem a 95 F.
Questão 1110
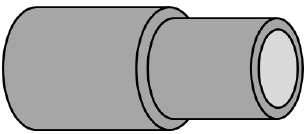
I. Passar água fria na superfície interna do cano de dentro e água quente na superfície externa do cano de fora.
II. Passar água fria tanto na superfície interna do cano de dentro quanto na superfície externa do cano de fora.
III. Passar água quente na superfície interna do cano de dentro e água fria na superfície externa do cano de fora.
IV. Passar água quente tanto na superfície interna do cano de dentro quanto na superfície externa do cano de fora.
verifica-se que está(ão) correto(s) apenas
- A) I.
- B) I e III.
- C) I e IV.
- D) II e III.
- E) II e IV.
Agora, vamos analisar a questão sobre termologia e encontrar a resposta correta.
A questão apresenta quatro opções para separar os canos de cobre encaixados. As opções são:
- I. Passar água fria na superfície interna do cano de dentro e água quente na superfície externa do cano de fora.
- II. Passar água fria tanto na superfície interna do cano de dentro quanto na superfície externa do cano de fora.
- III. Passar água quente na superfície interna do cano de dentro e água fria na superfície externa do cano de fora.
- IV. Passar água quente tanto na superfície interna do cano de dentro quanto na superfície externa do cano de fora.
Agora, vamos analisar cada opção e entender por que apenas uma delas é correta.
A opção I é a única que apresenta uma variação de temperatura entre a superfície interna e externa dos canos. Isso faz com que o cano de dentro se contraia e o cano de fora se expanda, o que possibilita a separação dos canos.
As outras opções não apresentam essa variação de temperatura, portanto, não possibilitam a separação dos canos.
Portanto, a resposta correta é a letra A, que corresponde à opção I.
Em resumo, a dilatação térmica dos materiais é a chave para separar os canos de cobre encaixados. A opção I é a única que explora essa propriedade, fazendo com que os canos se separem.
