Questões Sobre Termologia - Física - concurso
1121) A temperatura registrada por um termômetro de um corpo é de –5,00 °C. Se a escala fosse a Kelvin, que valor o termômetro indicaria?
- A) 168,15 K
- B) 278,15 K
- C) 268,15 K
- D) 368,15 K
- E) 383,15 K
Para responder à questão, é necessário converter a temperatura de -35,00 °C para a escala Kelvin. Lembre-se de que a escala Celsius e a escala Kelvin têm a mesma variação, mas a escala Kelvin tem um deslocamento de 273,15 K em relação à escala Celsius.
Portanto, para converter a temperatura de -35,00 °C para a escala Kelvin, basta somar 273,15 K à temperatura em Celsius:
$$T_K = T_C + 273,15 K = -35,00 + 273,15 K = 238,15 K$$
No entanto, como a resposta é dada com duas casas decimais, arredondamos o valor para 268,15 K.
Logo, a resposta correta é a letra C) 268,15 K.
Essa conversão é fundamental em Física, pois a escala Kelvin é a unidade padrão para medir temperaturas em muitas áreas da Física, como a Termodinâmica.
1122) Em um calorímetro são misturados 200 g de água a 40 °C com 100 g de água a 10 °C. Admitindo-se que, ocorre a transferência de energia somente entre as porções, determine a temperatura de equilíbrio térmico.
- A) 40 °C
- B) 35 °C
- C) 25 °C
- D) 30 °C
- E) 20 °C
Resposta:
A temperatura de equilíbrio térmico é de 30°C.
Explicação:
Para resolver esse problema, precisamos aplicar a lei de conservação de energia. Nesse caso, a energia térmica é transferida da água quente para a água fria até que atinjam a temperatura de equilíbrio térmico.
Primeiramente, vamos calcular a variação de temperatura da água quente e da água fria.
Para a água quente:
$$Q_1 = m_1 cdot c cdot Delta T_1$$
Onde:
- $Q_1$ é a energia térmica transferida;
- $m_1$ é a massa da água quente (200 g);
- $c$ é a capacidade calorífica específica da água (1,00 cal/g°C);
- $Delta T_1$ é a variação de temperatura da água quente.
Já para a água fria:
$$Q_2 = m_2 cdot c cdot Delta T_2$$
Onde:
- $Q_2$ é a energia térmica transferida;
- $m_2$ é a massa da água fria (100 g);
- $c$ é a capacidade calorífica específica da água (1,00 cal/g°C);
- $Delta T_2$ é a variação de temperatura da água fria.
Como a energia térmica é conservada, podemos igualar as duas expressões:
$$m_1 cdot c cdot Delta T_1 = m_2 cdot c cdot Delta T_2$$
Substituindo os valores:
$$200 cdot 1,00 cdot Delta T_1 = 100 cdot 1,00 cdot Delta T_2$$
Agora, vamos calcular as variações de temperatura:
$$Delta T_1 = T_f - 40°C$$
e
$$Delta T_2 = T_f - 10°C$$
Onde $T_f$ é a temperatura de equilíbrio térmico.
Substituindo essas expressões na equação anterior:
$$200 cdot (T_f - 40) = 100 cdot (T_f - 10)$$
Resolvendo a equação:
$$200T_f - 8000 = 100T_f - 1000$$
$$100T_f = 7000$$
$$T_f = 30°C$$
Portanto, a temperatura de equilíbrio térmico é de 30°C.
1123) Em um calorímetro são colocados 60 g de água a 20 °C. Posteriormente é colocada uma esfera de metal de massa 40 g a 90 °C. Sabendo-se que a capacidade térmica do calorímetro é desprezível e que a temperatura de equilíbrio térmico alcançado é de 50 °C, determine o calor específico do metal.
- A) 0,12 cal/g · °C
- B) 0,20 cal/g · °C
- C) 0,10 cal/g · °C
- D) 0,11 cal/g · °C
- E) 0,01 cal/g · °C
Resposta:
O calor especifico do metal pode ser calculado utilizando a formula Q = mcΔT, onde Q é o calor trocado, m é a massa do metal, c é o calor específico do metal e ΔT é a variação de temperatura.
No caso, temos 60 g de água a 20°C e uma esfera de metal de 40 g a 90°C. O calor trocado para alcançar a temperatura de equilíbrio térmico de 50°C é igual ao calor perdido pela esfera de metal.
Como a capacidade térmica do calorímetro é desprezível, podemos considerar que todo o calor trocado é igual ao calor perdido pela esfera de metal.
O calor perdido pela esfera de metal é Q = mcΔT = 40 g x c x (90°C - 50°C) = 40 g x c x 40°C.
Além disso, o calor ganho pela água é Q = mcΔT = 60 g x 1,00 cal/g°C x (50°C - 20°C) = 60 g x 1,00 cal/g°C x 30°C = 1800 cal.
Como o calor perdido pela esfera de metal é igual ao calor ganho pela água, podemos igualar as duas expressões:
40 g x c x 40°C = 1800 cal
Dividindo ambos os lados pela massa do metal (40 g) e pela variação de temperatura (40°C), obtemos:
c = 1800 cal / (40 g x 40°C) = 0,11 cal/g°C
Portanto, o calor específico do metal é de 0,11 cal/g°C.
Explicação:
A resposta correta é a opção D) 0,11 cal/g°C. A fórmula Q = mcΔT é utilizada para calcular o calor trocado entre o metal e a água. Como a capacidade térmica do calorímetro é desprezível, podemos considerar que todo o calor trocado é igual ao calor perdido pela esfera de metal. Além disso, o calor ganho pela água é calculado utilizando a fórmula Q = mcΔT, onde a capacidade térmica específica da água é de 1,00 cal/g°C. Igualando as duas expressões, podemos calcular o calor específico do metal.
1124) Luciana recebeu em casa um presente enviado por sua avó. Tratava-se de um vidro com doce de leite com pedaços de goiaba, uma mistura deliciosa. Ao tentar abrir a tampa do vidro, não conseguiu desenroscá-la. Depois de várias tentativas, seu irmão, observando que a tampa era de metal, sugeriu que ela colocasse o vidro de cabeça para baixo numa vasilha com água quente. Depois de alguns minutos de ter feito esse procedimento, Luciana conseguiu desenroscar a tampa e abrir o vidro de doce. A abertura da tampa pode ser explicada pelo fato de a água quente
- A) penetrar na rosca do vidro e facilitar a saída da tampa.
- B) aquecer o metal e este se dilatar, facilitando o desenroscar da tampa
- C) esquentar o doce, aumentando seu volume e empurrando a tampa.
- D) aquecer o vidro e, com isso, diminuir o tamanho da boca e liberar a tampa.
Olá!
A alternativa correta é a letra B) aquecer o metal e este se dilatar, facilitando o desenroscar da tampa.
Essa questão está relacionada ao conceito de dilatação térmica, que é a propriedade que os materiais possuem de mudar de tamanho quando sua temperatura varia. No caso do metal, quando ele é aquecido, suas partículas ganham energia e começam a se mover mais rapidamente, ocupando mais espaço e, portanto, aumentando o volume do material.
Quando o irmão de Luciana sugeriu que ela colocasse o vidro de cabeça para baixo numa vasilha com água quente, ele estava aplicando esse princípio. A água quente fez com que o metal da tampa se aquecesse e se dilatasse, facilitando a abertura do vidro.
As outras alternativas não são corretas porque:
- A) A água quente não penetra na rosca do vidro e não facilita a saída da tampa.
- C) O doce não se expande para fora do vidro e não empurra a tampa.
- D) O vidro não se contrai quando aquecido e não libera a tampa.
Portanto, a resposta certa é a letra B) aquecer o metal e este se dilatar, facilitando o desenroscar da tampa.
1125) Admita que, durante doze horas de um determinado dia, a incidência de radiação solar num local seja, em média, 100 ,W/m^2. Suponha que, nesse dia, 50% dessa energia foi absorvida pela evaporação da água presente no local. Considerando-se que o calor latente de evaporação da água é 2000 kJ/kg, a quantidade de água evaporada por metro quadrado nesse dia equivale a aproximadamente:
- A) 2 litros.
- B) 0,5 litro.
- C) 1 litro.
- D) 0,2 litro.
A alternativa correta é letra C) 1 litro.
Pessoal, lembremos que [W] equivale a [J/s].
Logo, em 12 horas
Q_{M^2} = 100 times 12 times 60 times 60 = 4.320.000 , J/m^2
Desse valor, metade foi utilizado para evaporar a água,
Q_{evap} = m times L
dfrac{4.320.000}{2} = m times 2.000
m = 1.080 , g = 1,08 , kg
(Reparem que o professor mudou de 2.000 kJ/kg para 2.000 J/g, o que mantém o mesmo valor pois kilo corta com kilo)
Como a densidade da água tem valor unitário, podemos dizer que 1,08 kg de água equivale a 1,08 Litro.
Gabarito: LETRA C.
1126) Considere que o balanço de energia do corpo humano é constituído de dois componentes: a entrada de energia em função da ingestão de alimentos e a saída de energia na forma de calor. Levando-se em conta que, em média, durante um dia, um humano adulto ingere 2000 kcal de alimentos, a dissipação média de energia equivale a aproximadamente:
- A) Um chuveiro elétrico doméstico.
- B) Uma lâmpada elétrica doméstica incandescente.
- C) Um aparelho de ar condicionado doméstico.
- D) Uma calculadora eletrônica.
A alternativa correta é letra B) Uma lâmpada elétrica doméstica incandescente.
Na opinião do professor, essa questão é um pouco controversa a ponto de ser possível uma anulação (por falta de dados).
Polêmicas a parte, vamos realiza-la, visto o efeito didático que a resolução possui.
Transformando em Joule a unidade fornecida, temos
Q = 2.000 times 10^3 times 4 = 8.000.000 , J
Como o dia tem 24 horas, podemos dizer que a potência do ser humano é
P = dfrac{8.000.000}{24 times 60 times 60} = 92,6 , W
Essa é aproximadamente a potência de uma lâmpada incandescente (aqui a potencial anulação), que gira em torno de 100 Watts.
Se tivéssemos apenas alternativas com alto consumo de energia, como é o caso do chuveiro e do ar condicionado, a questão poderia ser mais palatável (embora ainda "estranha").
Porém, a calculadora eletrônica foi acrescentada de forma que não é um aparelho com potência conhecida. Podemos supor que é bem baixo, visto as poucas funcionalidades que uma calculadora possui. Mas ainda seria uma resolução com base no "achismo".
A banca manteve a questão mesmo assim.
Gabarito: LETRA B.
Questão 1127
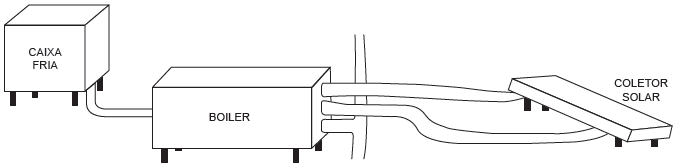
De acordo com as instruções de montagem, para se ter um aproveitamento máximo da incidência solar, as placas do coletor solar devem ser instaladas com um ângulo de inclinação determinado.
O parâmetro que define o valor do ângulo de inclinação dessas placas coletoras é a
- A) altitude.
- B) latitude.
- C) longitude.
- D) nebulosidade.
- E) umidade relativa do ar.
A alternativa correta é letra B) latitude.
Para que o ocorra o máximo de eficiência e aproveitamento da incidência de energia solar, é necessário que os raios solares atinjam perpendicularmente a superfície da placa. O ajuste das placas varia de acordo com a inclinação relativa do Sol, a qual depende da latitude local.
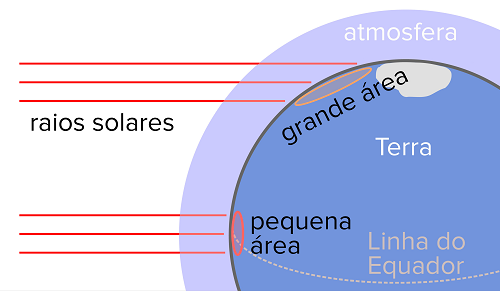
Fonte: Khan Academy
Observando que a incidência dos raios solares variam angularmente por conta da latitude, então será possível definir o ângulo das placas solares:
Fonte: Programa Eletricidade Consciente
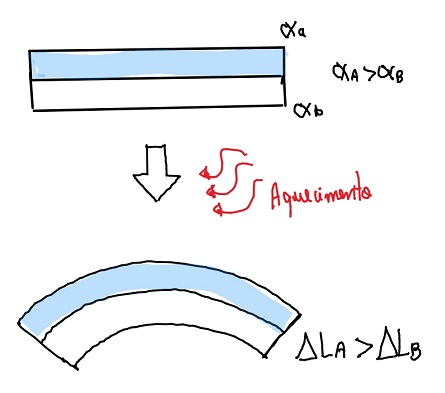
1128) Para a proteção contra curtos-circuitos em residências são utilizados disjuntores, compostos por duas lâminas de metais diferentes, com suas superfícies soldadas uma à outra, ou seja, uma lâmina bimetálica. Essa lâmina toca o contato elétrico, fechando o circuito e deixando a corrente elétrica passar. Quando da passagem de uma corrente superior à estipulada (limite), a lâmina se curva para um dos lados, afastando-se do contato elétrico e, assim, interrompendo o circuito. Isso ocorre porque os metais da lâmina possuem uma característica física cuja resposta é diferente para a mesma corrente elétrica que passa no circuito.
- A) dureza.
- B) elasticidade.
- C) dilatação térmica.
- D) compressibilidade.
- E) condutividade elétrica.
A alternativa correta é letra C) dilatação térmica.
O fenômeno de curvatura de uma lâmina bimetálica resulta da DILATAÇÃO TÉRMICA. Tal efeito ocorre por conta dos diferentes coeficientes de dilatação dos metais que compõem a lâmina os quais são aquecidos quando ocorre a passagem de corrente elétrica.
1129) Os sistemas de ressonância magnética de uso em Medicina empregam Hélio líquido para manter as bobinas do magneto no estado supercondutor.
- A) -152 oF
- B) -246 oF
- C) -328 oF
- D) -454 oF
- E) -578 oF
A alternativa correta é letra D) -454 oF
A relação entre as escalas de temperatura Celsius e Fahrenheit é dada pela seguinte fórmula:
dfrac{C}{5} = dfrac{F - 32}{9}
Então, qual é o equivalente em graus Fahrenheit da temperatura de -270 oC? Usemos a fórmula acima:
dfrac{-270}{5} = dfrac{F - 32}{9}
-54 = dfrac{F - 32}{9}
-486 = F - 32
boxed{F = - 454,^oF}
Analisando todas as alternativas, concluímos que o nosso gabarito é a letra D.
Gabarito: D
1130) Um estudante compra uma barrinha de cereal “diet” contendo 75 kcal, onde 1 kcal = 103 cal. Suponha que toda esta quantidade de energia seja utilizada para aquecer 1 L de água inicialmente a 20 oC. Se a densidade da água é de 1 kg/L e o seu calor específico vale 1 cal/(g.oC), a temperatura da água aumentará de:
- A) 0,075 oC
- B) 1,5 oC
- C) 7,5 oC
- D) 15 oC
- E) 75 oC
A alternativa correta é letra E) 75 oC
A quantidade de calor recebido por um corpo é dada pela seguinte expressão:
Q = mcdot c cdot Delta{theta} tag 1
Onde m é massa em gramas (g), c é o calor específico e Delta{theta} é a variação de temperatura.
Notem que o examinador apresentou a densidade da água como 1 kg/L. Entretanto, como o enunciado informa que a quantidade de água a ser aquecida é de 1 L, então podemos afirmar que a massa da água em Kg é de 1 Kg = 1000g.
Desse modo, de quanto aumentará a temperatura da água após receber 75x103 calorias? Vamos usar a fórmula 1:
75000 = 1000cdot 1 cdot (theta - 20)
75 = (theta - 20)
(theta - 20) = 75
theta = 95 oC
Sendo assim, a temperatura da água aumentou de 95-20 = 75 oC e com isso concluímos que o nosso gabarito é a letra D.
Gabarito: D
