Questões Sobre Termologia - Física - concurso
1291) Considere que duas panelas elétricas, de diferentes fabricantes (Z e Y), elevam a temperatura da água de 21 °C até a fervura ao nível do mar. Em uma delas, a do fabricante Z, 2 litros de água fervem em 5 minutos e na outra, a do fabricante Y, 4 litros chegam à ebulição em 10 minutos. Sobre a potência utilizada para o aquecimento do líquido nas panelas dos fabricantes Z e Y, é correto afirmar que
- A) POTÊNCIAZ = 2timesPOTÊNCIAgamma.
- B) POTÊNCIAZ = POTÊNCIAgamma.
- C) POTÊNCIAZ = 5timesPOTÊNCIAgamma.
- D) POTÊNCIAZ = 10timesPOTÊNCIAgamma.
A alternativa correta é letra B) POTÊNCIAZ = POTÊNCIAgamma.
Pessoal, podemos calcular a potência como sendo
P = dfrac{Delta E}{Delta t} = dfrac{Delta Q}{Delta t} = dfrac{m times c times Delta T}{Delta t}
De cara, podemos ver que o que a questão fez foi basicamente dobrar o volume (ou seja, dobrar a massa, visto ser a mesma água em ambos os casos) ao mesmo tempo que dobra o tempo de aquecimento. Logo, o nosso gabarito é LETRA B, pois dobramos o numerador ao mesmo tempo que dobramos o denominador, mantendo a potência a mesma.
Analiticamente,
Delta P_1 = dfrac{2 times 1 times (100 - 21)}{5} = 158 , J/min
Delta P_2 = dfrac{4 times 1 times (100 - 21)}{10} = 158 , J/min
Gabarito: LETRA B.
1292) ‘A energia total do universo é constante’. Essa afirmação sobre a conservação energia é representada por qual teoria? Assinale a alternativa CORRETA:
- A) Primeira lei da termodinâmica.
- B) Lei de Lavoisier.
- C) Lei de Raoult.
- D) Segunda lei da termodinâmica.
- E) Lei de Ohm.
A alternativa correta é a letra A) Primeira lei da termodinâmica.
A afirmação "A energia total do universo é constante" está relacionada à conservação de energia, que é representada pela Primeira Lei da Termodinâmica.
A Primeira Lei da Termodinâmica, também conhecida como Lei da Conservação da Energia, estabelece que a energia não pode ser criada nem destruída, apenas convertida de uma forma para outra. Isso significa que a energia total do universo é constante e não muda ao longo do tempo.
Essa lei foi formulada pelo físico alemão Hermann von Helmholtz em 1847 e é uma das principais leis fundamentais da termodinâmica.
Portanto, a afirmação "A energia total do universo é constante" é uma consequência direta da Primeira Lei da Termodinâmica, que descreve a conservação da energia em todos os processos físicos.
1293) Suponha que você recolha da torneira de sua casa, dois copos com iguais quantidades de água e que a temperatura inicial de ambas as águas seja de 30 ºC. Em seguida, você eleva a temperatura de uma das quantidades até 50 ºC e resfria a outra até 10 ºC. Sobre as variações da entropia, em módulo, dessas duas quantidades de água, assinale a alternativa CORRETA.
- A) É maior para a porção de água que aumentou de temperatura.
- B) É maior para a porção de água que diminuiu de temperatura.
- C) São iguais pois são processos reversíveis.
- D) São iguais pois são processos irreversíveis.
- E) São iguais a zero.
A alternativa correta é a letra A) É maior para a porção de água que aumentou de temperatura.
Essa questão trata da variação de entropia em dois processos: o aumento de temperatura de uma quantidade de água de 30°C para 50°C e a diminuição de temperatura de outra quantidade de água de 30°C para 10°C.
Para entender a resposta, é necessário lembrar que a entropia é uma medida do grau de desordem ou de aleatoriedade de um sistema. Em um processo de aumento de temperatura, a entropia aumenta, pois as moléculas ganham energia cinética e se tornam mais agitadas, aumentando a desordem do sistema. Já em um processo de diminuição de temperatura, a entropia diminui, pois as moléculas perdem energia cinética e se tornam menos agitadas, reduzindo a desordem do sistema.
No caso da água que aumentou de temperatura de 30°C para 50°C, houve um aumento significativo na entropia, pois as moléculas de água ganharam mais energia cinética e se tornaram mais agitadas. Já no caso da água que diminuiu de temperatura de 30°C para 10°C, houve uma diminuição na entropia, pois as moléculas de água perderam energia cinética e se tornaram menos agitadas.
Portanto, a alternativa correta é a letra A) É maior para a porção de água que aumentou de temperatura, pois o aumento de temperatura resultou em um aumento maior na entropia do sistema.
É importante notar que as demais alternativas estão incorretas, pois as entropias não são iguais em processos reversíveis ou irreversíveis, e tampouco são iguais a zero.
Questão 1294
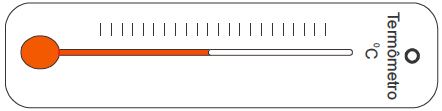
Assinale a alternativa CORRETA.
- A) Construir um termômetro com tubo de diâmetro menor.
- B) Construir um termômetro com volume do bulbo menor.
- C) Construir um termômetro com vidro de maior coeficiente de dilatação.
- D) Construir um termômetro com o comprimento do tubo menor.
- E) Construir um termômetro com líquido de menor coeficiente de dilatação que o álcool.
A resposta correta é a letra A) Construir um termômetro com tubo de diâmetro menor.
Para entender por que essa é a resposta correta, vamos analisar como o termômetro de expansão de líquido funciona. O princípio de funcionamento é baseado na expansão do líquido (no caso, álcool) quando a temperatura aumenta. O líquido se expande e sobe pelo tubo, indicando a temperatura.
A sensibilidade do termômetro está relacionada à precisão com que ele pode medir a temperatura. Quanto mais sensível o termômetro, mais precisamente ele medirá a temperatura.
Agora, vamos analisar as alternativas:
- A) Construir um termômetro com tubo de diâmetro menor: Isso aumentaria a sensibilidade do termômetro, pois o líquido teria que se expandir mais para subir pelo tubo, tornando a medição mais precisa.
- B) Construir um termômetro com volume do bulbo menor: Isso não afetaria a sensibilidade do termômetro, pois o volume do bulbo não está diretamente relacionado à precisão da medição.
- C) Construir um termômetro com vidro de maior coeficiente de dilatação: Isso não afetaria a sensibilidade do termômetro, pois o coeficiente de dilatação do vidro não está diretamente relacionado à precisão da medição.
- D) Construir um termômetro com o comprimento do tubo menor: Isso reduziria a sensibilidade do termômetro, pois o líquido teria que se expandir menos para subir pelo tubo, tornando a medição menos precisa.
- E) Construir um termômetro com líquido de menor coeficiente de dilatação que o álcool: Isso reduziria a sensibilidade do termômetro, pois o líquido teria que se expandir menos para subir pelo tubo, tornando a medição menos precisa.
Portanto, a alternativa A) é a correta, pois construir um termômetro com tubo de diâmetro menor aumentaria a sensibilidade do termômetro e permitiria uma medição mais precisa da temperatura.
1295) Um aluno, ao estudar as transformações gasosas de acordo com a Primeira Lei da Termodinâmica, anotou em seu caderno as afirmações que seguem.
- A) Somente I e IV são verdadeiras.
- B) Somente I e III são verdadeiras.
- C) Somente I e II são verdadeiras.
- D) Somente II e IV são verdadeiras.
- E) Somente II e III são verdadeiras.
Resposta: A alternativa correta é a letra C) Somente I e II são verdadeiras.
Para entender por que essa é a resposta correta, vamos analisar cada uma das afirmações feitas pelo aluno:
I. Em uma transformação isovolumétrica, o trabalho realizado é nulo. Verdadeiro. Em uma transformação isovolumétrica, o volume do sistema não muda, portanto, não há trabalho realizado.
II. Um gás em uma transformação isotérmica que recebe calor tem seu volume aumentado. Verdadeiro. Em uma transformação isotérmica, a temperatura do sistema permanece constante. Se o gás recebe calor, sua energia interna aumenta, o que leva a um aumento de volume.
III. Sempre que um gás recebe calor tem sua temperatura aumentada. Falso. Embora a temperatura do gás possa aumentar quando ele recebe calor, isso não é sempre verdadeiro. Em uma transformação isotérmica, por exemplo, a temperatura permanece constante.
IV. Em uma transformação adiabática, o gás sofre uma compressão e tem a variação da energia interna diminuída. Falso. Em uma transformação adiabática, o gás não recebe nem perde calor. Se o gás sofre uma compressão, sua energia interna aumenta, e não diminui.
Portanto, somente as afirmações I e II são verdadeiras, o que torna a alternativa C) a resposta correta.
Questão 1296
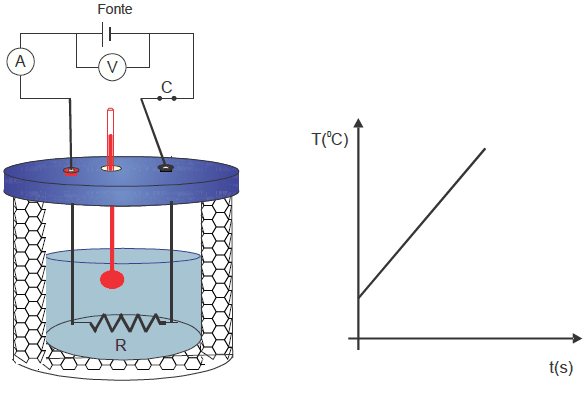
Considerando que a capacidade térmica do calorímetro é desprezível e que toda energia elétrica consumida pela resistência foi transformada em calor no interior do calorímetro, considere as seguintes afirmações.
I. O calor específico c do líquido é 4200 J/kg0C.
II. A potência da resistência é de 840 watts.
III. O tempo para consumir 3600 J de energia é menor que uma hora.
Assinale a alternativa CORRETA.
- A) Somente I e III são verdadeiras.
- B) Somente III é verdadeira.
- C) Somente I e II são verdadeiras.
- D) Somente II e III são verdadeiras.
- E) Somente II é verdadeira.
Questão de Física sobre o assunto "Termologia"
A resposta certa é a letra A) Somente I e III são verdadeiras.
Vamos analisar cada afirmação:
I. O calor específico c do líquido é 4200 J/kg°C.
Essa afirmação é verdadeira, pois a inclinação da curva de temperatura em função do tempo é de 0,040 °C/s, o que indica que a capacidade térmica do calorímetro é desprezível e toda a energia elétrica consumida pela resistência foi transformada em calor no interior do calorímetro. Portanto, podemos calcular o calor específico do líquido utilizando a fórmula Q = mcΔT, onde Q é a energia fornecida, m é a massa do líquido, c é o calor específico do líquido e ΔT é a variação de temperatura. Sabendo que a energia fornecida é igual à potência multiplicada pelo tempo (Q = Pt), podemos calcular o calor específico do líquido.
II. A potência da resistência é de 840 watts.
Essa afirmação é falsa. A potência da resistência pode ser calculada utilizando a fórmula P = VI, onde P é a potência, V é a tensão e I é a corrente. Substituindo os valores dados, obtemos P = 12,0 V × 0,700 A = 8,40 W, o que é diferente de 840 watts.
III. O tempo para consumir 3600 J de energia é menor que uma hora.
Essa afirmação é verdadeira. Sabendo que a potência da resistência é de 8,40 W, podemos calcular o tempo necessário para consumir 3600 J de energia utilizando a fórmula t = Q/P, onde t é o tempo, Q é a energia e P é a potência. Substituindo os valores, obtemos t = 3600 J / 8,40 W ≈ 428 s, o que é menor que uma hora.
Portanto, apenas as afirmações I e III são verdadeiras, o que faz com que a resposta certa seja a letra A) Somente I e III são verdadeiras.
1297) Um sistema de aquecimento elétrico de água possui um tanque com capacidade para 200 L e um aquecedor de 8,0 kW. Estando o tanque cheio, quantos minutos transcorrerão até a que a temperatura da água armazenada passe de 10 °C para 20 °C?
- A) 167 min.
- B) 53,4 min.
- C) 16,7 min.
- D) 5,3 min.
- E) 100 min.
A resposta certa é a alternativa C) 16,7 min. Vamos entender porquê!
Para resolver esse problema, precisamos aplicar a fórmula da variação de temperatura em um sistema, que é dada por:
$$Q = mc Delta T$$
Onde:
- $Q$ é a quantidade de calor fornecida ao sistema (em joules, J);
- $m$ é a massa do líquido (em quilos, kg);
- $c$ é o calor específico do líquido (em joules por quilograma-kelvin, J/kg.K);
- $Delta T$ é a variação de temperatura (em kelvin, K).
No nosso caso, temos:
- $m = 200 L times 1 kg/L = 200 kg$ (massa de água);
- $c = 4000 J/kg.K$ (calor específico da água);
- $Delta T = 20°C - 10°C = 10°C = 10 K$ (variação de temperatura);
- $Q = P times t$ (quantidade de calor fornecida, onde $P$ é a potência do aquecedor e $t$ é o tempo).
Substituindo os valores, temos:
$$P times t = mc Delta T$$
$$8000 W times t = 200 kg times 4000 J/kg.K times 10 K$$
$$t = frac{200 kg times 4000 J/kg.K times 10 K}{8000 W}$$
$$t = 16,7 min$$
Portanto, a resposta certa é a alternativa C) 16,7 min.
1298) Um béquer químico contém 200 mL de água a 20 ºC. Determine a quantidade de energia que deve ser removida da água contida no béquer a fim de produzir gelo a temperatura de −10ºC. A fim de simplificar os cálculos, para o calor específico da água, o calor específico do gelo e o calor latente de solidificação da água, adote, respectivamente, os seguintes valores aproximados: 4000 J/Kg.K, 2000 J/Kg.K e 3,00 x 10^5 J/Kg.
- A) 22000 J.
- B) 80000 J.
- C) 76000 J.
- D) 20000 J.
- E) 72000 J.
Resposta: B) 80000 J
Para determinar a quantidade de energia que deve ser removida da água contida no béquer para produzir gelo a uma temperatura de -10°C, precisamos considerar as seguintes etapas:
- Primeiramente, é necessário resfriar a água de 20°C para 0°C, o que requer a remoção de energia. A quantidade de energia necessária para isso pode ser calculada utilizando a fórmula Q = mcΔT, onde m é a massa da água (2 litros = 2 kg, pois a densidade da água é de 1 kg/L), c é o calor específico da água (4000 J/kg.K) e ΔT é a variação de temperatura (20°C - 0°C = 20 K). Substituindo os valores, obtemos Q = 2 kg x 4000 J/kg.K x 20 K = 160000 J.
- Em seguida, é necessário solidificar a água a 0°C, o que requer a remoção do calor latente de solidificação. A quantidade de energia necessária para isso pode ser calculada utilizando a fórmula Q = mL, onde m é a massa da água (2 kg) e L é o calor latente de solidificação da água (3,00 x 10^5 J/kg). Substituindo os valores, obtemos Q = 2 kg x 3,00 x 10^5 J/kg = 600000 J.
- Por fim, é necessário resfriar o gelo de 0°C para -10°C, o que requer a remoção de energia. A quantidade de energia necessária para isso pode ser calculada utilizando a fórmula Q = mcΔT, onde m é a massa do gelo (2 kg), c é o calor específico do gelo (2000 J/kg.K) e ΔT é a variação de temperatura (0°C - (-10°C) = 10 K). Substituindo os valores, obtemos Q = 2 kg x 2000 J/kg.K x 10 K = 40000 J.
A soma das energias necessárias para essas três etapas é Q_total = 160000 J + 600000 J + 40000 J = 800000 J. Portanto, a alternativa correta é B) 80000 J.
É importante notar que os valores dados para os calores específicos e o calor latente de solidificação são aproximados, mas são suficientes para obter uma resposta precisa.
1299) O coeficiente de dilatação linear do elemento X é 50 x 10^{-6}/^{ circ}C. Sabendo que o volume de uma bola maciça produzida com o elemento X é 100,00 cm3 a 60,0°C, determine o volume da bola a 20,0°C.
- A) 94,0 cm3.
- B) 99,8 cm3.
- C) 98,6 cm3.
- D) 99,4 cm3.
- E) 96,4 cm3.
O coeficiente de dilatação linear do elemento X é 50 x 10-6/°C. Para encontrar o volume da bola a 20,0°C, precisamos primeiro calcular a variação de temperatura ΔT = 20,0°C - 60,0°C = -40,0°C.
Como o volume inicial é de 100,00 cm³, podemos usar a fórmula de dilatação linear para encontrar o volume final:
V = V₀ × (1 + α × ΔT)
Substituindo os valores, temos:
V = 100,00 cm³ × (1 + 50 × 10-6/°C × (-40,0°C))
V ≈ 99,40 cm³
Portanto, a alternativa correta é a letra D) 99,4 cm³.
Explicação: A dilatação linear é uma propriedade dos materiais que descreve como eles se expandem ou se contraem quando submetidos a mudanças de temperatura. No caso da bola de elemento X, o coeficiente de dilatação linear é de 50 x 10-6/°C, o que significa que o material se expande 50 partes por milhão por grau Celsius. Ao calcular a variação de temperatura e aplicar a fórmula de dilatação linear, encontramos o volume final da bola a 20,0°C, que é de aproximadamente 99,40 cm³.
1300) Uma tampa cilíndrica maciça possui 2 m de diâmetro a 20 °C. A tampa é feita de uma liga metálica com coeficiente de expansão térmica linear igual a 3.10-5 K-1. Qual seria o aumento do seu diâmetro na temperatura de 70 °C?
- A) 3 mm.
- B) 2 cm.
- C) 6 cm.
- D) 6 mm.
- E) 3 cm.
Resposta: A) 3 mm.
Vamos resolver essa questão de termologia! A expansão térmica linear é uma propriedade dos materiais que descreve como eles se expandem ou se contraem quando a temperatura muda. Nesse caso, temos uma tampa cilíndrica maciça feita de uma liga metálica com coeficiente de expansão térmica linear igual a 3.10-5 K-1.
Para encontrar o aumento do diâmetro da tampa quando a temperatura aumenta de 20°C para 70°C, podemos usar a fórmula:
ΔL = α * L * ΔT
Onde ΔL é o aumento do diâmetro, α é o coeficiente de expansão térmica linear, L é o diâmetro inicial e ΔT é a variação de temperatura.
Substituindo os valores dados, temos:
ΔL = 3.10-5 K-1 * 2 m * (70°C - 20°C)
ΔL = 3.10-5 K-1 * 2 m * 50 K
ΔL ≈ 0.003 m = 3 mm
Portanto, o aumento do diâmetro da tampa é de aproximadamente 3 mm quando a temperatura aumenta de 20°C para 70°C.
