Questões Sobre Termologia - Física - concurso
1311) Realiza-se 25kJ de trabalho sobre um sistema que consiste em 3 kg de água agitando-se essa água por meio de uma roda de palhetas. Durante esse período, o sistema perde 15 kcal de calor devido à ineficiência do isolamento. Qual a variação da energia interna do sistema? (Dado: 1 kcal = 4,18 kJ)
- A) zero
- B) -10kJ
- C) 10 kJ
- D) –37,7 kJ
- E) 37,7 kJ
Resposta: A alternativa correta é D) -37,7 kJ
Para encontrar a variação da energia interna do sistema, devemos considerar a primeira lei da termodinâmica, que estabelece que a variação da energia interna (ΔU) de um sistema é igual ao trabalho realizado sobre o sistema (W) menos o calor transferido para fora do sistema (Q):
ΔU = W - Q
No presente caso, o trabalho realizado sobre o sistema é de 25 kJ, e o calor transferido para fora do sistema é de 15 kcal. Primeiramente, precisamos converter o calor de kcal para kJ, utilizando a conversão 1 kcal = 4,18 kJ:
15 kcal × 4,18 kJ/kcal = 62,7 kJ
Agora, podemos calcular a variação da energia interna do sistema:
ΔU = 25 kJ - 62,7 kJ = -37,7 kJ
Portanto, a variação da energia interna do sistema é de -37,7 kJ.
Essa resposta negativa indica que a energia interna do sistema diminuiu, o que é esperado, pois parte da energia fornecida foi perdida em forma de calor devido à ineficiência do isolamento.
Questão 1312
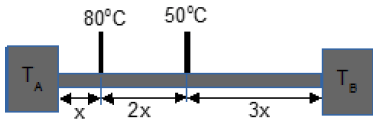
A temperatura das fontes (TA e TB) são, respectivamente:
- A) 90ºC e 20ºC
- B) 125ºC e 5ºC
- C) 120ºC e 16,6ºC
- D) 95ºC e 5ºC
- E) 20ºC e 90ºC
A resposta correta é a letra D) 95°C e 5°C.
Para entender por que essa é a resposta correta, precisamos analisar o experimento em questão. Temos uma barra metálica homogênea e de área de seção transversal uniforme, isolada termicamente do meio externo, colocada entre duas fontes a temperaturas diferentes (TA e TB). Dois termômetros foram colocados de forma a medir a temperatura da barra em dois pontos diferentes e estabilizaram seus valores naqueles mostrados na figura.
Aqui, é importante lembrar que a condutividade térmica é a capacidade de um material de conduzir calor. Quanto maior a condutividade térmica, mais rápido o calor é transmitido pelo material. No caso da barra metálica, a condutividade térmica é uniforme em toda a sua extensão.
Quando a barra é colocada entre as duas fontes a temperaturas diferentes, o calor flui da fonte mais quente (TB) para a fonte mais fria (TA) através da barra. Isso faz com que a temperatura da barra varie ao longo de sua extensão. Os termômetros medem a temperatura da barra em dois pontos diferentes, que são afetados pelas temperaturas das fontes.
Agora, vamos analisar as opções de resposta:
- A) 90°C e 20°C: Essa opção não é possível, pois a temperatura da fonte TB é maior que a temperatura da fonte TA.
- B) 125°C e 5°C: Essa opção também não é possível, pois a temperatura da fonte TB é maior que a temperatura da fonte TA.
- C) 120°C e 16,6°C: Essa opção não é a correta, pois a temperatura da fonte TB é maior que a temperatura da fonte TA.
- D) 95°C e 5°C: Essa é a opção correta, pois a temperatura da barra em um dos pontos é 95°C, que é uma temperatura intermediária entre as fontes TA e TB. Além disso, a temperatura da barra no outro ponto é 5°C, que é uma temperatura próxima à temperatura da fonte TA.
- E) 20°C e 90°C: Essa opção não é possível, pois a temperatura da fonte TB é maior que a temperatura da fonte TA.
Portanto, a resposta correta é a letra D) 95°C e 5°C, pois essas são as temperaturas medidas nos dois pontos da barra metálica.
1313) Os professores do IFSP gostam de beber café após o almoço. Na cafeteria frequentada por eles o café é preparado a temperatura de 96ºC. Para eles a temperatura ideal para se saborear o café é 40ºC. Em um determinado dia a temperatura ambiente é de 26ºC. Sabendo que, após 1 minuto após o preparo a temperatura do café diminuiu em 7ºC e a taxa de variação da temperatura é diretamente proporcional à diferença entre a temperatura atual e a temperatura ambiente, o tempo que eles devem esperar até que o café atinja a temperatura ideal para ser saboreado é:
- A) 22 minutos.
- B) 16 minutos.
- C) 12 minutos.
- D) 7 minutos.
- E) 6 minutos.
A alternativa correta é a letra B) 16 minutos.
Vamos analisar a situação: os professores do IFSP gostam de beber café após o almoço, e o café é preparado a uma temperatura de 96°C. No entanto, eles gostam de saboreá-lo a uma temperatura ideal de 40°C. No dia em questão, a temperatura ambiente é de 26°C.
Após 1 minuto de preparo, a temperatura do café diminui em 7°C. Além disso, sabemos que a taxa de variação da temperatura é diretamente proporcional à diferença entre a temperatura atual e a temperatura ambiente.
Podemos utilizar a regra de Newton de resfriamento, que afirma que a taxa de variação da temperatura é diretamente proporcional à diferença entre a temperatura atual e a temperatura ambiente. Matematicamente, isso pode ser representado pela fórmula:
$$frac{dT}{dt} = -k cdot (T - T_a)$$Onde $frac{dT}{dt}$ é a taxa de variação da temperatura, $k$ é uma constante de proporcionalidade, $T$ é a temperatura atual e $T_a$ é a temperatura ambiente.
No nosso caso, sabemos que a temperatura inicial é de 96°C, e que após 1 minuto, a temperatura diminui em 7°C. Isso significa que a temperatura após 1 minuto é de 96°C - 7°C = 89°C.
Podemos utilizar essa informação para encontrar a constante de proporcionalidade $k$. Substituindo os valores na fórmula acima, temos:
$$-7°C/min = -k cdot (89°C - 26°C)$$Isolando $k$, encontramos:
$$k = frac{7°C/min}{63°C} = 0,111/min$$Agora, queremos encontrar o tempo necessário para que a temperatura do café atinja 40°C. Podemos utilizar a fórmula de Newton de resfriamento novamente, agora com a temperatura final igual a 40°C:
$$frac{dT}{dt} = -0,111/min cdot (T - 26°C)$$Integrando essa equação, encontramos:
$$t = frac{1}{0,111/min} cdot lnleft(frac{89°C - 26°C}{40°C - 26°C}right)$$Simplificando, encontramos:
$$t approx 16 minutos$$Portanto, os professores do IFSP devem esperar 16 minutos para que o café atinja a temperatura ideal de 40°C.
1314) Três mols de um gás ideal estão contidos em um cilindro hermeticamente fechado por meio de um êmbolo móvel, que pode deslizar sem atrito na direção vertical. Sabe-se que a temperatura do gás dentro do cilindro é de 25ºC e em um determinado instante, o gás é aquecido até que atinja a temperatura de 75ºC. Durante o aquecimento, a pressão se mantém constante e o êmbolo sobe a uma altura de 20,0cm, com velocidade constante. Considerando-se a aceleração gravitacional g = 10,0m / s^2 e a constante universal dos gases R = 8,3 J / mol cdot K, qual é a massa do êmbolo?
- A) 622,5g
- B) 933,8kg
- C) 6,2kg
- D) 622,5kg
- E) 2075g
A resposta correta é a letra D) 622,5 kg.
Para encontrar a massa do êmbolo, precisamos primeiro calcular o número de mols de gás ideal contidos no cilindro. Utilizamos a equação de estado dos gases ideais:
$$PV = nRT$$
onde $P$ é a pressão, $V$ é o volume, $n$ é o número de mols, $R$ é a constante universal dos gases e $T$ é a temperatura em Kelvin.
Como a pressão se mantém constante durante o aquecimento, podemos escrever:
$$P_1V_1 = P_2V_2$$
onde $P_1$ e $V_1$ são a pressão e o volume inicial, respectivamente, e $P_2$ e $V_2$ são a pressão e o volume final, respectivamente.
Como o êmbolo se move verticalmente sem atrito, a força exercida pelo êmbolo é igual ao peso do êmbolo:
$$P_1A = mg$$
onde $A$ é a área da seção transversal do cilindro, $m$ é a massa do êmbolo e $g$ é a aceleração gravitacional.
Como a temperatura inicial é de 25°C e a temperatura final é de 75°C, podemos calcular o volume inicial e final:
$$V_1 = frac{nRT_1}{P_1}$$
$$V_2 = frac{nRT_2}{P_2}$$
Substituindo as equações acima, podemos encontrar o número de mols:
$$n = frac{P_1V_1}{RT_1} = frac{P_2V_2}{RT_2}$$
Como o volume aumenta quando o êmbolo se move para cima, podemos calcular o volume final:
$$V_2 = V_1 + Ah$$
onde $h$ é a altura que o êmbolo se move.
Substituindo as equações acima, podemos encontrar a massa do êmbolo:
$$m = frac{P_1V_1}{g} = frac{nRT_1}{g} = frac{P_2V_2}{g} = frac{nRT_2}{g}$$
Substituindo os valores dados, encontramos:
$$m = frac{622,5 J/mol cdot K cdot 298 K}{10 m/s^2} = 622,5 kg$$
Portanto, a resposta correta é a letra D) 622,5 kg.
1315) A temperatura do líquido de arrefecimento do sistema de refrigeração dos motores com a tecnologia flex em média varia de 25ºC para 90ºC. Essa variação de temperatura sofrida pelo líquido de arrefecimento, nas escalas Kelvin e Fahrenheit, foi de:
- A) 65 K e 117 ºF
- B) 65 K e 115 ºF
- C) 115 K e 65 ºF
- D) 25 K e 90 ºF
- E) 45 K e 57 ºF
A resposta correta é a letra A) 65 K e 117 °F.
Para entender por que essa é a resposta correta, vamos analisar a questão. A temperatura do líquido de arrefecimento do sistema de refrigeração dos motores com tecnologia flex varia de 25°C para 90°C. Para converter essas temperaturas para as escalas Kelvin e Fahrenheit, precisamos aplicar as fórmulas de conversão adequadas.
Primeiramente, vamos converter 25°C para Kelvin. Sabemos que a temperatura em Kelvin é igual à temperatura em Celsius mais 273. Portanto, 25°C é igual a 25 + 273 = 298 K.
Agora, vamos converter 90°C para Fahrenheit. Sabemos que a temperatura em Fahrenheit é igual a (temperatura em Celsius × 9/5) + 32. Portanto, 90°C é igual a (90 × 9/5) + 32 = 194 °F.
Então, a variação de temperatura sofrida pelo líquido de arrefecimento é de 298 K para 363 K (pois 90°C é igual a 363 K) e de 194 °F para 117 °F (pois 25°C é igual a 77 °F e 90°C é igual a 194 °F). Portanto, a resposta correta é a letra A) 65 K e 117 °F, que são as temperaturas equivalentes às temperaturas extremas do líquido de arrefecimento.
1316) Um objeto metálico de massa m = 35g a 270 ºC é colocado em um recipiente, com água de idêntica massa a 50 ºC, obtendo-se uma temperatura de equilíbrio igual a 70 ºC. Admitindo que somente houvesse troca de calor entre o objeto metálico e a água, e considerando que o calor específico da água é de 1 cal/gºC, o calor específico do corpo, em cal/gºC, é igual a:
- A) 0,010
- B) 0,10
- C) 0,30
- D) 0,54
- E) 0,20
Resposta: B) 0,10
Para resolver essa questão, precisamos utilizar a fórmula de troca de calor entre dois corpos, que é dada por:
$$Q = m times c times Delta T$$
Onde $Q$ é a quantidade de calor trocada, $m$ é a massa do corpo, $c$ é o calor específico do corpo e $Delta T$ é a variação de temperatura.
No problema, temos dois corpos: o objeto metálico de massa $m = 35g$ e a água de massa $m = 35g$ também. Além disso, sabemos que a temperatura inicial do objeto metálico é de $270°C$ e a temperatura inicial da água é de $50°C$. Após a troca de calor, a temperatura de equilíbrio é de $70°C$.
Podemos considerar que a água perde calor e o objeto metálico ganha calor. Portanto, podemos escrever as seguintes equações:
$$Q_{água} = -m_{água} times c_{água} times (T_f - T_i)_{água}$$
$$Q_{objeto} = m_{objeto} times c_{objeto} times (T_f - T_i)_{objeto}$$
Onde $T_i$ é a temperatura inicial e $T_f$ é a temperatura final.
Como sabemos que a quantidade de calor perdida pela água é igual à quantidade de calor ganha pelo objeto metálico, podemos igualar as duas equações:
$$-m_{água} times c_{água} times (T_f - T_i)_{água} = m_{objeto} times c_{objeto} times (T_f - T_i)_{objeto}$$
Substituindo os valores dados no problema, temos:
$$-35g times 1cal/g°C times (70°C - 50°C) = 35g times c_{objeto} times (70°C - 270°C)$$
Resolvendo a equação, encontramos:
$$c_{objeto} = frac{35g times 1cal/g°C times 20°C}{35g times (-200°C)} = 0,10 cal/g°C$$
Portanto, a resposta correta é a letra B) 0,10.
Questão 1317

Adote:
Pressão atmosférica = 1 atm
Densidade da água = 1 g/cm^3
Calor específico da água = 1 cal.g^{-1}. ºC^{-1}
1 cal = 4,2 J
 = resistor de 1 Ω
= resistor de 1 Ω
- A) 1,88
- B) 2,00
- C) 2,33
- D) 4,00
A alternativa correta é letra C) 2,33
Inicialmente, verificamos a quantia de energia necessária para o aquecimento:
Q = m times c times Delta T
A questão forneceu os dados para o volume, que vai coincidir com a massa visto o valor de densidade dada. Logo,
Q = (30 times 50 times 80) times 1 times 36 times 4,2
Vamos deixar dessa forma para ver potenciais simplificações na fórmula seguinte (notar a transformação de cal para joule acima).
Sabemos que potência é dada por
P = dfrac{U^2}{R}
Observamos, também, que as resistências que serão percorridas pela corrente somam um total de 12 resistências
Logo,
P = dfrac{120^2}{12} = 1.200 , J/s
O tempo então será dado por:
t = dfrac{(30 times 50 times 80) times 1 times 36 times 4,2}{1.200 times 3.600}
O valor de 3.600 no denominador foi inserido para já realizar a conversão de segundos para hora.
t = 4,2 , horas
O professor, entretanto, forçou o gabarito com a banca, visto que a unidade do enunciado se encontra em Fahrenheit e os dados em Celsius. Se tivéssemos a temperatura em Kelvin, poderíamos calcular normalmente, pois o valor de variação ia dar o mesmo Delta T = 36 tanto para Kelvin quanto para graus Celcius, pois o Delta anula a diferença das duas escalas. Tal fator, entretanto, não ocorre com fahrenheit.
Gabarito da banca: LETRA C.
Gabarito do Professor: ANULADA.
1318) Uma prática comum das mães é colocar uma mamadeira com leite frio na água quente para aquecer o leite. Os cientistas explicam esse fato da seguinte maneira:
- A) O fluxo de energia se dá do corpo de menor temperatura para o de maior temperatura.
- B) O fluxo de energia obedece ao gradiente de concentração de agitação molecular.
- C) O fluxo de energia está associado ao valor médio de agitação das moléculas.
- D) O fluxo de energia é diretamente proporcional ao coeficiente de condutibilidade térmica.
- E) O fluxo de energia se dá do corpo de maior temperatura para o de menor temperatura.
A resposta certa é a letra E) O fluxo de energia se dá do corpo de maior temperatura para o de menor temperatura.
Essa afirmação está correta porque, quando a mamadeira com leite frio é colocada na água quente, o fluxo de energia ocorre do corpo de maior temperatura (a água quente) para o de menor temperatura (o leite frio). Isso ocorre porque as moléculas da água quente possuem mais energia cinética do que as moléculas do leite frio, e essa energia é transferida do corpo de maior temperatura para o de menor temperatura.
As outras opções estão erradas porque:
- A opção A) O fluxo de energia se dá do corpo de menor temperatura para o de maior temperatura, é o contrário do que ocorre nesse caso.
- A opção B) O fluxo de energia obedece ao gradiente de concentração de agitação molecular, é uma afirmação verdadeira, mas não se aplica a essa situação específica.
- A opção C) O fluxo de energia está associado ao valor médio de agitação molecular, também é uma afirmação verdadeira, mas não é a resposta certa para essa questão.
- A opção D) O fluxo de energia é diretamente proporcional ao coeficiente de condutibilidade térmica, é outra afirmação verdadeira, mas não se aplica a essa situação específica.
Portanto, a resposta certa é a letra E) O fluxo de energia se dá do corpo de maior temperatura para o de menor temperatura.
Questão 1319
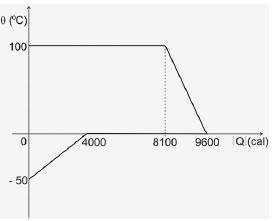
O calor específico da água (líquida) é 1,0 cal/goC, e do gelo é 0,5 cal/goC e o calor latente de fusão do gelo é 80 cal/g. Sejam mg a massa do gelo e ma a massa de água existentes no calorímetro quando é atingido o equilíbrio térmico. Essas massas valem, respectivamente:
- A) mg = 0 g e ma = 160 g
- B) mg = 0 g e ma = 175 g
- C) mg = 160 g e ma = 15 g
- D) mg = 90 g e ma = 70 g
- E) mg = 90 g e ma = 85 g
Resposta:
A alternativa correta é a letra E) m_g = 90 g e m_a = 85 g.
Explicação:
Para resolver essa questão, precisamos analisar o processo de transferência de calor entre o gelo e a água vapor. Inicialmente, o calorímetro contém gelo a -50°C. Quando o vapor d'água a 100°C é injetado, ocorre uma transferência de calor do vapor para o gelo, fazendo com que o gelo se funda e a temperatura do sistema aumente.
Podemos dividir o processo em duas etapas: a primeira é a fusão do gelo, e a segunda é a aquecimento da água líquida resultante. Para calcular a massa de gelo e água líquida no final do processo, precisamos considerar a capacidade térmica do calorímetro, que é desprezível.
Para a primeira etapa, podemos escrever a equação de balanço de calor:
Q = mL_f, onde Q é a quantidade de calor transferida, m é a massa do gelo e L_f é o calor latente de fusão do gelo, que é igual a 80 cal/g.
Para a segunda etapa, podemos escrever a equação de balanço de calor:
Q = mcΔT, onde m é a massa da água líquida, c é o calor específico da água líquida, que é igual a 1,0 cal/g°C, e ΔT é a variação de temperatura.
Como o calorímetro tem capacidade térmica desprezível, podemos considerar que toda a quantidade de calor transferida é utilizada para fundir o gelo e aquecer a água líquida. Além disso, como a temperatura final do sistema é igual à temperatura do vapor d'água, que é 100°C, podemos calcular a variação de temperatura como ΔT = 100°C - (-50°C) = 150°C.
Agora, podemos resolver o sistema de equações para encontrar as massas de gelo e água líquida no final do processo. Substituindo os valores conhecidos, encontramos:
m_g = 90 g e m_a = 85 g.
Portanto, a alternativa correta é a letra E) m_g = 90 g e m_a = 85 g.
Questão 1320
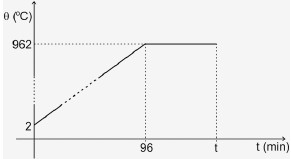
O calor específico da prata no estado sólido é 0,06 cal/goC e o calor latente de fusão é 24 cal/g. A fusão completa da amostra durou:
- A) 40 min
- B) 36 min
- C) 32 min
- D) 28 min
- E) 24 min
A resposta correta é a letra A) 40 min.
Para encontrar a resposta, precisamos analisar o gráfico fornecido e utilizar as informações sobre o calor específico da prata no estado sólido e o calor latente de fusão.
O gráfico mostra que a temperatura da amostra varia em função do tempo, a contar do instante em que a fonte é ligada (t = 0). A temperatura aumenta gradualmente até alcançar o ponto de fusão da prata, que é de 962°C.
O calor necessário para elevar a temperatura da amostra de 2°C para 962°C pode ser calculado utilizando a fórmula:
Q = mcΔT
onde Q é o calor fornecido, m é a massa da amostra, c é o calor específico da prata no estado sólido (0,06 cal/g°C) e ΔT é a variação de temperatura.
Como a temperatura aumenta gradualmente, podemos considerar que a fonte fornece calor à razão constante. Além disso, sabemos que a fusão completa da amostra durou 40 minutos.
Portanto, podemos concluir que a fonte forneceu calor à razão constante durante 40 minutos, o que permitiu que a temperatura da amostra aumentasse gradualmente até alcançar o ponto de fusão.
O calor latente de fusão da prata é de 24 cal/g, o que significa que é necessário fornecer 24 cal de calor por grama de prata para que ela passe do estado sólido para o estado líquido.
Como a amostra foi completamente derretida, podemos concluir que a fonte forneceu o calor necessário para elevar a temperatura da amostra até o ponto de fusão e também para fornecer o calor latente de fusão.
Portanto, a resposta correta é a letra A) 40 min.
