Questões Sobre Termologia - Física - concurso
1321) Ao se elevar a temperatura de uma substância, ocorre um aumento de seu volume. Considerando que a temperatura da água é aumentada de 0 °C à 4 °C, é correto afirmar que:
- A) o volume aumenta e a densidade diminui e, a partir de 4 °C, o volume aumenta e a densidade diminui;
- B) a densidade diminui e o volume também e, a partir de 4 °C tanto a densidade quanto o volume aumentam;
- C) o volume diminui e a densidade aumenta e, a partir de 4 °C, o volume aumenta e a densidade diminui;
- D) o volume e a densidade permanecem inalterados, visto que a variação de 0 °C à 4 °C da temperatura é muito pequena;
- E) o volume diminui e a densidade se mantém constante, e a partir de 4° C, o volume e a densidade aumentam.
A alternativa correta é letra C) o volume diminui e a densidade aumenta e, a partir de 4 °C, o volume aumenta e a densidade diminui;
Questão capciosa.
Quando aumentamos a temperatura de um material, ele aumenta seu volume e sua densidade diminui (d = dfrac{m}{V}), consequentemente (VIA DE REGRA).
Para a água entretanto, o comportamento é diferente dependendo do caso. Para temperaturas próximas a temperatura de congelamento (0 graus), ela tem um comportamento inverso:
Quanto maior a temperatura, menor o volume e maior a densidade.
A partir de uma temperatura mais elevada (mais distante do ponto de congelamento), aí sim teremos o comportamento "normal" de aumento de temperatura com aumento de volume (e consequente redução de densidade).
Logo, já eliminamos as alternativas A B D e E, ficando com nosso gabarito LETRA C.
A questão cravou a temperatura de virada desse comportamento como sendo a temperatura de 4 graus (que é realmente a temperatura que o comportamento acima é observado experimentalmente).
Gabarito: LETRA C.
1322) Um isolamento térmico eficiente é um constante desafio a ser superado para que o homem possa viver em condições extremas de temperatura.
- A) condução, convecção e radiação.
- B) condução, radiação e convecção.
- C) convecção, condução e radiação.
- D) convecção, radiação e condução.
A alternativa correta é letra D) convecção, radiação e condução.
Gabarito: LETRA D.
Vamos analisar cada uma das situações:
I. As prateleiras de uma geladeira doméstica são grades vazadas, para facilitar o fluxo de energia térmica até o congelador por convecção. A convecção é um processo de troca de calor que ocorre através do movimento de um fluido. No caso, o ar dentro da geladeira. As grades vazadas permitem que o ar circule livremente, promovendo a transferência de calor por convecção.
II. O único processo de troca de calor que pode ocorrer no vácuo é por radiação. A radiação térmica é a transferência de calor por meio de ondas eletromagnéticas, como a luz infravermelha. No vácuo, onde não há meio material para condução ou convecção, a radiação é o único mecanismo de transferência de calor possível, já que as ondas eletromagnéticas não necessitam de meio material para se propagarem.
III. Em uma garrafa térmica, é mantido vácuo entre as paredes duplas de vidro para evitar que o calor saia ou entre por condução. A condução é a transferência de calor através de contato direto entre materiais. No caso da garrafa térmica, o vácuo entre as paredes duplas de vidro impede a transferência de calor por condução, pois o vácuo é um isolante térmico eficiente.
Portanto, a resposta correta é a alternativa (d).
1323) Uma usina termoelétrica hipotética opera com vapor de água aquecido a uma temperatura de 500ºC e é resfriada com água a 50ºC. Considera-se que a usina funcione como uma máquina de Carnot e que ela recebe de uma fonte quente uma quantidade de calor Q por ciclo. Os valores da eficiência e do trabalho W, realizados em cada ciclo de operação da usina, são, respectivamente,
- A) 10% e W=0,9Q
- B) 90% e W=0,1Q
- C) 90% e W=0,9Q
- D) 50% e W=0,5Q
- E) 90% e W=0,5Q
Resposta:
A alternativa correta é: Não há alternativa correta, pois a questão foi anulada.
Explicação:
Antes de iniciar a resolução da questão, é importante notar que a mesma foi anulada, portanto, não há uma resposta correta. No entanto, vamos analisar as alternativas apresentadas e entender por que nenhuma delas é válida.
A eficiência de uma máquina de Carnot é dada pela fórmula η = 1 - (Tc / Th), onde η é a eficiência, Tc é a temperatura do reservatório frio e Th é a temperatura do reservatório quente. No caso da usina termoelétrica hipotética, temos Th = 500°C e Tc = 50°C.
Substituindo os valores na fórmula, obtemos η = 1 - (50 + 273) / (500 + 273) = 0,64 ou 64%. Isso significa que a eficiência da usina é de 64%.
Agora, vamos analisar as alternativas:
- A) 10% e W = 0,9Q: A eficiência é muito baixa em relação ao valor calculado.
- B) 90% e W = 0,1Q: A eficiência é muito alta e o trabalho realizado é muito baixo.
- C) 90% e W = 0,9Q: A eficiência é muito alta e o trabalho realizado é muito alto.
- D) 50% e W = 0,5Q: A eficiência é razoável, mas o trabalho realizado é muito baixo.
- E) 90% e W = 0,5Q: A eficiência é muito alta e o trabalho realizado é muito baixo.
Como podemos ver, nenhuma das alternativas apresentadas coincide com o valor de eficiência calculado. Além disso, as relações entre o trabalho realizado e a quantidade de calor Q também não são coerentes. Portanto, a questão foi anulada por não ter uma alternativa correta.
1324) Com base nas leis da termodinâmica, assinale a alternativa CORRETA.
- A) A expansão livre é um processo adiabático no qual as energias internas, inicial e final são diferentes.
- B) Num processo adiabático, um aumento da energia interna acarreta numa diminuição da temperatura do sistema e, inversamente, uma redução da energia interna acarreta um aumento da temperatura do sistema.
- C) As compressões e rarefações nas ondas sonoras são tão rápidas que o comportamento do gás que as transmite não é adiabático.
- D) O aquecimento que se observa nos pneus de bicicleta durante seu preenchimento é devido ao aumento de temperatura por uma compressão adiabática do ar.
- E) Num processo adiabático irreversível, a variação de entropia é nula.
A resposta certa é a letra D)
O aquecimento que se observa nos pneus de bicicleta durante seu preenchimento é devido ao aumento de temperatura por uma compressão adiabática do ar.
Isso ocorre porque, quando o ar é comprimido, sua energia interna aumenta, o que causa um aumento de temperatura. Esse processo é adiabático, pois não há troca de calor com o ambiente. Além disso, como a compressão é feita rapidamente, não há tempo para que o calor seja dissipado, o que leva a um aumento de temperatura.
Já as outras alternativas estão erradas:
A alternativa A está errada porque, em um processo adiabático, a energia interna do sistema pode aumentar ou diminuir, dependendo da natureza do processo.
A alternativa B está errada porque, em um processo adiabático, a temperatura do sistema pode aumentar ou diminuir, dependendo da variação da energia interna.
A alternativa C está errada porque as compressões e rarefações nas ondas sonoras não são processos adiabáticos.
A alternativa E está errada porque, em um processo adiabático irreversível, a variação de entropia é diferente de zero.
1325) Dois corpos A e B são aquecidos. O corpo A tem massa m, e o corpo B tem massa igual ao triplo da massa de A. O calor específico c do corpo B vale a metade do calor específico do corpo A.
- A) 0,5
- B) 1,0
- C) 1,5
- D) 2,0
- E) 3,0
A alternativa correta é letra C) 1,5
Pessoal, vamos chamar de m a massa que se iguala a massa de A.
m_A = m
m_B = 3 m
Já o calor específico,
c_A = c
c_B = dfrac{c}{2}
Em A,
Q = m c Delta T_A
Delta T_A = dfrac{Q}{m c }
Em B,
Q = 3m times dfrac{c}{2} Delta T = 1,5 m c Delta T_B
Delta T_B = dfrac{Q}{1,5 m c }
Logo,
dfrac{ Delta T_A}{Delta T_B} = dfrac { Q / (m c)} {Q / 1,5 m c} = 1,5
Gabarito: LETRA C.
1326) Numa escala hipotética H de temperatura, atribui-se o valor 60 °H para a temperatura de fusão do gelo e −180 °H para a temperatura de ebulição da água, sob pressão normal.
- A) − 68
- B) 100
- C) 2
- D) 48
- E) − 22
A alternativa correta é letra C) 2
Trata-se de um exercício de conversão de unidades de temperatura. Para resolver exercícios como este devemos montar o esquema abaixo comparando as escalas fornecidas no enunciado.
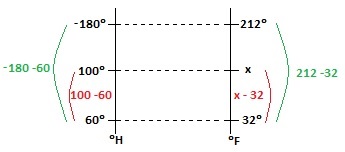
Em seguida, devemos relacionar as duas escalas com uma regra de três:
{100-60 over -180 -60} = {x - 32 over 212 -32}
{40 over -240} = {x - 32 over 180}
x = 2 º F
Resposta: Alternativa C
1327) Uma substância pura apresenta as seguintes características:
- A) 240
- B) 4200
- C) 2000
- D) 800
- E) 3360
A alternativa correta é letra B) 4200
Com os dados fornecidos podemos concluir que o líquido se encontra, inicialmente, no estado líquido. A energia Q_1 fornecida à substância irá aumentar sua temperatura de 20 ºC até 70 ºC, a partir deste momento, a temperatura permanecerá constante e o calor Q_2 será utilizado apenas para mudar o estado físico da substância.
Lembre-se:
- mudança de temperatura → Q = m cdot c cdot Delta T
- mudança de estado físico → Q = m cdot L (temperatura permanece constante na mudança de estado físico)
Cálculo de Q_1 :
Q_1 = m cdot c cdot Delta T
Q_1 = 10 cdot 0,4 cdot 50 = 200 cal
Cálculo de Q_2 :
Q_2 = m cdot L
Q_2 = 10 cdot 80 = 800 cal
A energia total fornecida a substância foi Q_1 + Q_2 = 1000 cal.
Conversão de unidades (cal to J)
1 cal to 4,2 J
1000 cal to x J
x = 4.200 J
Resposta: Alternativa B
1328) Em um calorímetro à temperatura ambiente de 30 °C, de capacidade térmica 40 cal/°C, são misturados 20 gramas de gelo a − 20 °C, 50 gramas de água a 25 °C e 10 gramas de vapor de água a 120 °C. Estabelecido o equilíbrio térmico, admitindo que não haja perda de calor para o ambiente, a temperatura final da mistura, em °C, é de aproximadamente
- A) 30
- B) 50
- C) 40
- D) 60
- E) 20
A alternativa correta é letra D) 60
O enunciado informou que não há perda de calor para o ambiente, portanto termos apenas o calor trocado entre os corpos, de forma que:
Q_{água} + Q_{gelo} + Q_{vapor} + Q_{calorímetro} =0 (1)
Para calcular os valores acima, é importante perceber que 20 < temperatura de equilíbrio < 60, conforme alternativas. Nestas temperaturas, os corpos no interior do calorímetro estarão no estado líquido.
Q_{água} = m.c.Delta T = 50.1.(T_e - 25)
Q_{água} = 50 . T_e - 1250
Q_{gelo} = (m.c.Delta T)_{sólido} + m.L + (m.c.Delta T)_{líquido}
Q_{gelo} = 20 . 0,5 . 20 + 20 . 80 + 20 . 1 .(T_e - 0)
Q_{gelo} = 1700 + 20 . T_e
Q_{vapor} = (m.c.Delta T)_{vapor} + m.L + (m.c.Delta T)_{líquido}
Q_{vapor} = 10 . 0,5 . (100-120) + 10 .(- 540) + 10 . 1 . (T_e - 100)
Q_{vapor} = - 6500 + 10 T_e
Q_{calorímetro} = C.Delta T = 40.(T_e -30)
Substituindo em (1), temos:
Q_{água} + Q_{gelo} + Q_{vapor} + Q_{calorímetro} =0
50. T_e - 1250 + 1700 + 20 . T_e - 6500 + 10 . T_e + 40 . T_e - 1200 = 0
T_e = 60,4 ºC
Resposta: Alternativa D
1329) Stefan e Boltzmann formularam uma lei que relaciona a potência irradiada P com a área A da superfície emissora e a temperatura absoluta T de um corpo.
- A) 5,0
- B) 30
- C) 20
- D) 10
- E) 40
A alternativa correta é letra D) 10
Atenção:
Sempre devemos observar as unidades das constantes para saber a unidade que devemos utilizar em todas as grandezas físicas envolvidas.
conversão de unidades: ºC to K
27ºC = (27 + 273) K = 300 K
127ºC = (127 + 273) K = 400 K
Potência irradiada:
P = epsilon . sigma . A . T^4
P = 0,05 cdot 5,7 cdot 10^{-8} cdot 0,2 cdot 400^4
P = 14,592 W
Potência absorvida:
P = epsilon . sigma . A . T^4
P = 0,05 cdot 5,7 cdot 10^{-8} cdot 0,2 cdot 300^4
P = 4,617 W
Potência efetiva:
Potência efetiva (P_e) = Potência irradiada + Potência absorvida
P_e = 14,592 - 4,617 = 9,975 simeq 10 W
Resposta: Alternativa D
Questão 1330

Assim, para se obter a temperatura de 160°C, deve‐se ajustar esse botão na posição:
- A) 2.
- B) 4.
- C) 6.
- D) 8.
A alternativa correta é letra A) 2.
Temos a relação do botão controlador de temperatura com a escala ºF, logo, será necessário fazer a conversão da temperatura solicitada (160º C) para ºF:
{c-0 over 100 - 0} = {f - 32 over 212-32}
{c over 5} = {f - 32 over 9}
{160 over 5} = {f - 32 over 9}
f = 320 º F
Com o valor da temperatura solicitada convertido na escala ºF, montaremos a relação desta escala com os números do botão controlador:
{x - 1 over 10 - 1} = {320 - 300 over 480- 300}
{x - 1 over 9} = {20 over 180}
x = 2
Resposta: Alternativa A
