Questões Sobre Termologia - Física - concurso
1391) Com relação à termologia, coloque V (verdadeiro) ou F (falso) e, a seguir, assinale a opção correta.
- A) (V) (V) (V) (F) (F) (V) (F)
- B) (F) (F) (V) (V) (F) (F) (V)
- C) (F) (F) (F) (V) (F) (V) (V)
- D) (V) (F) (F) (V) (V) (V) (F)
- E) (V) (V) (F) (F) (V) (F) (F)
A alternativa correta é letra D) (V) (F) (F) (V) (V) (V) (F)
ALTERNATIVA CORRETA: LETRA D
Com relação à termologia, coloque V (verdadeiro) ou F (falso) e, a seguir, assinale a opção correta.
( V ) Temperatura - grandeza física que representa a medida do estado de agitação médio das moléculas de um corpo.
( F ) Calor - energia térmica que passa, de forma espontânea do corpo de menor temperatura para o de maior temperatura.
Calor é energia térmica que passa, de forma espontânea, do corpo de maior temperatura para o de menor temperatura.
( F ) Fusão - mudança de estado físico sofrida por um líquido ao doar uma certa quantidade de calor.
Fusão é a mudança de estado físico sofrida por um sólido ao se transformar em líquido quando recebe uma certa quantidade de calor.
( V ) Evaporação passagem do estado líquido para o estado gasoso que ocorre de forma lenta.
( F ) Equilíbrio térmico - condição física na qual as trocas de calor entre dois ou mais corpos deixam de existir.
Equilíbrio térmico é a condição física na qual dois ou mais corpos ficam com a mesma temperatura (temperatura de equilíbrio térmico).
As trocas de calor podem não cessar, e os corpos podem continuar recebendo e cedendo calor na mesma proporção.
( V ) Convecção - processo de transmissão de calor que ocorre devido à movimentação de massas, em especial, nos líquidos e nos gases.
( F ) Caloria - quantidade de calor necessária para que 1g de qualquer substância tenha sua temperatura alterada em 1ºC.
Caloria é a quantidade de calor necessária para que 1g de água tenha sua temperatura alterada em 1°C .
ALTERNATIVA CORRETA: LETRA D
1392) Uma cidade localizada na Serra Catarinense a uma altitude de 1.450m acima do nível do mar, durante um determinado ano, registrou -8,9ºC, a mais baixa temperatura do inverno. Essa temperatura caso tivesse sido registrada na escala Fahrenheit, seria de aproximadamente
- A) 2ºF
- B) 8ºF
- C) 16ºF
- D) 22ºF
- E) 38°F
A alternativa correta é letra C) 16ºF
Gabarito: LETRA C.
Para encontrar uma relação entre duas escalas, é preciso conhecer pelo menos 2 pontos em comum entre elas. Sabemos que a fusão do gelo ocorre em 0°C, o que equivale a 32°F, e a vaporização da água ocorre em 100°C, correspondente a 212°F. Assim, podemos estabelecer uma relação entre as duas escalas como nos mostra a figura a seguir:
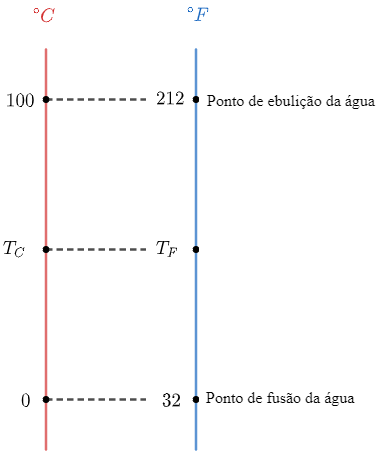
Assim, utilizando a relação de proporção entre as escalas Celsius e Fahrenheit, podemos escrever a equação:
dfrac { T_C - 0 } { 100 - 0 } = dfrac { T_F - 32 } { 212 - 32 }
dfrac { T_C } { 100 } = dfrac { T_F - 32 } { 180 }
dfrac { T_C } { 5 } = dfrac { T_F - 32 } { 9 }
T_F - 32 = dfrac 95 cdot T_C
T_F = dfrac 95 cdot T_C + 32
Então, para T_C = -8,9°C, temos:
T_F = dfrac 95 cdot left(-8,9right) + 32
T_F = 15,98°F
Portanto, a resposta correta é a alternativa (c).
1393) A termologia é a parte da Flsica que estuda os fenômenos determinados por energia térmica, que é a forma de energia relacionada à agitação das partículas de um corpo.
- A) Apenas a afirmativa I é verdadeira.
- B) Apenas as afirmativas I, lI e IlI são verdadeiras.
- C) Apenas as afirmativas I e IlI são verdadeiras.
- D) Apenas as afirmativas lI e IV são verdadeiras.
- E) Apenas as afirmativas I, IlI e IV são verdadeiras.
A alternativa correta é letra D) Apenas as afirmativas lI e IV são verdadeiras.
Gabarito: LETRA D.
Vamos analisar cada uma das afirmativas:
I - Quanto maior a energia cinética média das partículas, menor a temperatura do corpo. INCORRETA.
A temperatura é uma medida da energia térmica média das partículas em um sistema e está relacionada diretamente com a energia cinética média das partículas. Quanto maior a energia cinética média das partículas, maior será a temperatura do corpo.
lI - Para que haja transferência de calor entre dois corpos, eles devem estar a temperaturas diferentes. CORRETA.
A transferência de calor ocorre devido à diferença de temperatura entre dois corpos. O calor flui naturalmente do corpo com maior temperatura para o corpo com menor temperatura, buscando o equilíbrio térmico.
IlI - Quanto maior o calor específico de um material, menor a quantidade de calor necessária para o material ser aquecido até determinada temperatura. INCORRETA.
O calor específico de um material está relacionado com a quantidade de calor necessária para elevar a temperatura de uma unidade de massa desse material em uma unidade de temperatura. Dessa forma, quanto maior o calor específico, maior a quantidade de calor necessária para aquecer o material.
IV - No Sistema Internacional de Unidades, a quantidade de calor transferida de um corpo para outro é medida em joules. CORRETA.
O calor é uma forma de energia em trânsito e a unidade de medida para energia é o joule (J) no Sistema Internacional de Unidades (SI).
Portanto, a resposta correta é a alternativa (d).
1394) No início do século XX, Pierre Curie e colaboradores, emuma experiência para determinar características do recém- descoberto elemento químico rádio, colocaram uma pequena quantidade desse material em um calorímetro e verificaram que 1,30 grama de água líquida ia do ponto de congelamento ao ponto de ebulição em uma hora. A potência média liberada pelo rádio nesse período de tempo foi, aproximadamente,
- A) 0,06 W
- B) 0,10 W
- C) 0,14W
- D) 0,18 W
- E) 0,22 W
A alternativa correta é letra C) 0,14W
1º PASSO - Pelo fato de toda energia emitida pelo rádio ter sido empregada exclusivamente para elevar a temperatura da água, tem-se:
∆ε=Q
∆ε=m.c.∆T
∆ε=1,3.1.(100-0)
∆ε=130 cal
2º PASSO - Convertendo o valor de "caloria" para "Joule":
∆ε=130.4
∆ε=520 J
3º PASSO - Considerando o intervalo de uma hora (3600 s), a potência média liberada pelo rádio será:
P={∆ε over ∆t}
P={520 over 3600}
P=0,14 W
1395) Os oceanos e a atmosfera são considerados reservatórios térmicos naturais: para variar sua temperatura é preciso uma quantidade muito grande de calor. Por conta disso, eles são os principais responsáveis por manter as variações de temperatura no planeta mais amenas e suportáveis para a vida. Na superfície da Lua, por exemplo, onde não existem oceanos e a atmosfera é extremamente rarefeita, a temperatura em sua superfície varia de -173,1 ºC a 116,9 ºC. Qual característica física dos oceanos e da atmosfera possibilita essa propriedade?
- A) Calor latente elevado.
- B) Ponto de ebulição alto.
- C) Condução térmica baixa.
- D) Calor específico elevado.
- E) Capacidade térmica elevada.
A alternativa correta é letra E) Capacidade térmica elevada.
Analisando alternativa por alternativa:
a) Calor latente elevado. ERRADO. Isso não tem a ver com a capacidade de permanecer com temperatura estáveis.
b) Ponto de ebulição alto.
ERRADO. O ponto de ebulição diz qual a temperatura que a matéria troca de estado líquido para o gasoso.
c) Condução térmica baixa.
ERRADO. A condução térmica tem a ver com o fluxo de calor pelo meio. O aluno poderia ficar em dúvida com relação a essa. Porém, uma condução térmica baixa (baixo fluxo de calor) pode aumentar a temperatura de forma elevada a depender do material que estamos lidando.
d) Calor específico elevado.
ERRADO. Na opinião do professor essa alternativa também estaria correta, visto que calor específico relaciona a massa enquanto que a capacidade térmica apenas o corpo em questão. A questão porém colocou o gabarito na letra E. Tecnicamente a E está "mais correta". Porém, classificar esta alternativa como errada não parece o ideal.
e) Capacidade térmica elevada.
CORRETA. A capacidade térmica, assim como o calor específico, pode ser encarada como uma espécie de "resistência" ao aumento de temperatura de um corpo a partir de um fornecimento de calor ao mesmo. Podemos enxergar algebricamente pela relação abaixo:
Q = C times Delta T
Quanto maior o C, maior a necessidade de calor fornecida para alterar a temperatura.
Gabarito: LETRA E.
1396) Em um dia ensolarado no verão de Salvador, um turista passeia na praia às 10h da manhã e observa que a areia está quente e a água do mar gelada. Ao repetir o passeio às 22h, ele percebe que a areia já está fria e a água do mar permanece agradavelmente morna. Podemos explicar este fenômeno da seguinte forma:
- A) a areia resfria rapidamente na ausência dos raios solares devido à sua massa específica que é maior que a da água do mar.
- B) a areia apresenta maior calor específico e maior massa específica do que os apresentados pela água do mar.
- C) a areia apresenta calor específico significativamente menor do que o calor específico da água do mar.
- D) por apresentar calor específico maior, a areia sofre rápido aquecimento na presença dos raios solares.
A alternativa correta é letra C) a areia apresenta calor específico significativamente menor do que o calor específico da água do mar.
Gabarito: LETRA C.
A areia resfria rapidamente na ausência dos raios solares devido ao seu baixo calor específico, que é cerca de 5 vezes menor do que o da água do mar. Como necessita de uma quantidade menor de calor para variar sua temperatura, aproximadamente 0,2 cal/g°C, a areia resfria e aquece mais rapidamente que a água do mar, cujo calor específico é de 1,0 cal/g°C.
Portanto, a resposta correta é a alternativa (c).
1397) Em um dia muito quente, em que a temperatura ambiente era de 30oC, Sr. Aldemir pegou um copo com volume de 194 cm3 de suco à temperatura ambiente e mergulhou nele dois cubos de gelo de massa 15 g cada. O gelo estava a -4ºC e fundiu-se por completo. Supondo que o suco tem o mesmo calor específico e densidade que a água e que a troca de calor ocorra somente entre o gelo e suco, qual a temperatura final do suco do Sr. Aldemir? Assinale a alternativa CORRETA.
- A) 0ºC
- B) 2oC
- C) 12oC
- D) 15oC
- E) 26oC
A alternativa correta é letra D) 15oC
Gabarito: LETRA D.
De acordo com o enunciado, podemos afirmar que o calor cedido pela variação de temperatura do suco foi utilizado para aquecer e fundir o gelo, além de aquecer essa massa de água até a temperatura de equilíbrio, ou seja:
Q_{suco} = Q_{gelo_{aquec}} + Q_{gelo_{fus}} + Q_{água}
Logo,
m_{suco} cdot c_{suco} cdot Delta theta_{suco} = m_{gelo} cdot c_{gelo} cdot Delta theta_{gelo}+ m_{gelo} cdot L_{gelo} + m_{gelo} cdot c_{água} cdot Delta theta_{água}
rho_{suco} cdot V_{suco} cdot c_{suco} cdot Delta theta_{suco} = m_{gelo} cdot c_{gelo} cdot Delta theta_{gelo}+ m_{gelo} cdot L_{gelo} + m_{gelo} cdot c_{água} cdot Delta theta_{água}
1,0 cdot 194 cdot 1,0 left( 30-theta_{equi} right) = 30 cdot 0,5 cdot left( 0 - left( -4 right) right) + 30cdot 80 + 30 cdot 1,0 cdot left( theta_{equi} - 0 right)
5820-194 cdot theta_{equi} = 60 + 2400 + 30 cdot theta_{equi}
224 cdot theta_{equi} = 3360
theta_{equi} = 15°C
Portanto, a resposta correta é a alternativa (d).
1398) Um painel coletor de energia solar para aquecimento residencial de água, com 60% de eficiência, tem superfície coletora com área útil de 20 m2. A água circula em tubos fixados sob a superfície coletora. Suponha que a intensidade da energia solar incidente seja de 2,0 x 103 w/m2 e que a vazão de suprimento de água aquecida seja de 6,0 litros por minuto. Assinale a opção que indica aproximadamente a variação da temperatura da água. Dados: cágua = 1,0 cal/gºC; e 1 cal = 4,2 J.
- A) 12,2oC
- B) 22,7oC
- C) 37,3oC
- D) 45,6oC
- E) 57,1oC
A alternativa correta é letra E) 57,1oC
Gabarito: LETRA E.
Sabemos que a potência solar útil é dada pela razão entre a energia absorvida e o intervalo de tempo:
P_{útil} = dfrac { E } { Delta t }
Sendo eta a eficiência do painel e E a energia utilizada, na forma de calor, para aquecer a água, temos que:
eta cdot P_{incidente} = dfrac { Q } { Delta t }
Se I é a intensidade da energia solar incidente e A é a área da superfície, a equação acima se torna:
eta cdot I cdot A = dfrac { mcdot c cdot Delta theta } { Delta t }
Logo,
Delta theta = dfrac { eta cdot I cdot A cdot Delta t } { m cdot c }
Como a vazão de suprimento de água aquecida é de 6,0 litros por minuto, e a densidade de água é 1,0 kg por litro, podemos afirmar que, em 60 segundos, a massa de água aquecida é de 6,0 kg. Além disso, como cágua = 1,0 cal/gºC e 1 cal = 4,2 J, temos que cágua = 4200 J/kgºC. Assim, a equação acima se torna:
Delta theta = dfrac { 0,6 cdot 2,0 times 10^3 cdot 20 cdot 60 } { 6,0 cdot 4200 }
Delta theta approx 57,1 , °C
Portanto, a resposta correta é a alternativa (e).
Questão 1399
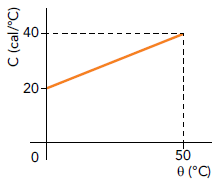
A quantidade de calor absorvida pelo material até a temperatura de 50 ºC, em calorias, é igual a:
- A) 500
- B) 1500
- C) 2000
- D) 2200
A alternativa correta é letra B) 1500
Gabarito: LETRA B.
A capacidade térmica C de um material é dada pela relação entre a quantidade de calor Q fornecida e a variação de temperatura Delta T, através da seguinte equação:
C = dfrac { Q } { Delta T }
Porém, quando a capacidade térmica é apresentada por meio de um gráfico, podemos calcular o calor transferido calculando a área sob a curva da capacidade térmica em função da temperatura.
Logo, a quantidade de calor absorvida pelo material até a temperatura de 50 ºC é numericamente igual à área sombreada do gráfico abaixo:
Então, como se trata de um trapézio, temos que:
Q = dfrac { left( 20 + 40 right) cdot 50 } { 2 }
Q = 1500 , cal
Portanto, a resposta correta é a alternativa (b).
Questão 1400
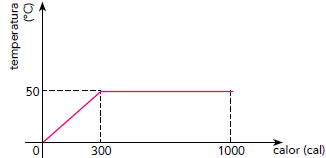
O calor latente de fusão dessa substância, em cal/g, é igual a:
- A) 70
- B) 80
- C) 90
- D) 100
A alternativa correta é letra A) 70
Gabarito: LETRA A.
Sabemos que, durante a mudança de fase, a temperatura da substância não varia.
Assim, observando o gráfico do enunciado, podemos afirmar que a substância inicia o processo de mudança de fase quando a quantidade de calor é 300 cal e passa integralmente da fase sólida para a fase líquida quando a quantidade de calor é 1000 cal, visto que a temperatura é mantida a 50° C.
Dessa forma, podemos afirmar que a quantidade de calor recebida durante a mudança de fase é dada por:
Q = 1000 - 300
Q = 700 , cal
Então, sendo m e L a massa e o calor latente de fusão da substância, respectivamente, temos que:
Q = m L
Logo,
L = dfrac { Q } { m }
L = dfrac { 700 , cal } { 10 , g }
L = 70 , cal/g
Portanto, a resposta correta é a alternativa (a).
