Questões Sobre Termologia - Física - concurso
1541) Em um depósito, um cilindro de gás está a uma pressão de 3,0 atm e ocupa um volume de 20 litros à temperatura de 27 ºC. Determine a pressão que o gás exerce quando sua temperatura aumenta para 127 ºC.
- A) 14,1 atm.
- B) 5,0 atm
- C) 3,5 atm
- D) 4,0 atm
Resposta: D) 4,0 atm
Para resolver esta questão, precisamos aplicar a equação de estado dos gases ideais, que relaciona a pressão (P), volume (V) e temperatura (T) de um gás:
$$PV = nRT$$
Onde n é a quantidade de substância (em moles) e R é a constante dos gases ideais.
No problema, sabemos que o volume do gás é de 20 litros e sua temperatura inicial é de 27°C (ou 300 K). Além disso, a pressão inicial é de 3,0 atm.
Queremos encontrar a pressão do gás quando sua temperatura aumenta para 127°C (ou 400 K). Podemos considerar que a quantidade de substância (n) e o volume (V) permanecem constantes.
Portanto, podemos rearranjar a equação de estado dos gases ideais para encontrar a pressão em função da temperatura:
$$P = frac{nRT}{V}$$
Substituindo os valores conhecidos, temos:
$$P_1 = frac{nR cdot 300 K}{20 L} = 3,0 atm$$
E, para a temperatura final:
$$P_2 = frac{nR cdot 400 K}{20 L} = 4,0 atm$$
Portanto, a pressão do gás quando sua temperatura aumenta para 127°C é de 4,0 atm.
1542) Analise as seguintes afirmações sobre o ciclo de Carnot e assinale a alternativa correta.
- A) Apenas a afirmação I está correta.
- B) Apenas as afirmações I e IV estão corretas.
- C) Apenas as afirmações II e IV estão corretas.
- D) Apenas as afirmações I, III e IV estão corretas.
A resposta correta é a letra B) Apenas as afirmações I e IV estão corretas.
Vamos analisar cada afirmação:
I - É constituído por dois processos isotérmicos reversíveis e dois processos adiabáticos reversíveis. Verdadeiro, pois o ciclo de Carnot é composto por dois processos isotérmicos (um de compressão e outro de expansão) e dois processos adiabáticos (um de compressão e outro de expansão).
II - É constituído por dois processos isotérmicos irreversíveis e dois processos adiabáticos irreversíveis. Falso, pois o ciclo de Carnot é composto por processos reversíveis.
III - Em um gás ideal, a energia interna depende somente da temperatura e, portanto, não permanece constante em um processo isotérmico. Falso, pois em um processo isotérmico, a temperatura é constante, e a energia interna de um gás ideal depende apenas da temperatura.
IV - A eficiência de uma máquina de Carnot depende apenas das temperaturas dos dois reservatórios. Verdadeiro, pois a eficiência de uma máquina de Carnot é dada pela razão entre as temperaturas dos dois reservatórios.
Portanto, apenas as afirmações I e IV estão corretas.
1543) Após estudar termometria, Lucas descobriu que existe uma temperatura X que possui o mesmo valor nas escalas termométricas Celsius e Fahrenheit. O estudante descobriu o valor dessa temperatura a partir das temperaturas de fusão e ebulição da água nas escalas Celsius e Fahrenheit, que são, ao nível do mar, 0ºC = 32ºF e 100ºC = 212ºF, respectivamente.
- A) 305.
- B) 241.
- C) 233.
- D) 313.
A alternativa correta é letra C) 233.
A temperatura que coincide nas escalas Celsius e Fahrenheit é - 40°. Tal temperatura, na escala Kelvin, tem o valor de 233K.
Caso o aluno não soubesse a temperatura acima, bastava calcular:
(T_C × 9/5) + 32 = T_F
(T_C × 9/5) + 32 = T_C
32 = T_C - (T_C × 9/5)
32 = - dfrac{4}{5} T_C
T_C = -40 , °C
T_K = - 40 + 273 = 233 , K
Gabarito: LETRA C.
Questão 1544
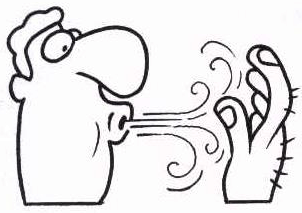
Fonte: Física, v. 2, Editora Scipione, 2006.
Ao soprar o ar com a menor abertura possível da boca, Valdir percebe que o ar chega frio em sua mão. A respeito da troca de calor (ΔQ) entre o ar e a vizinhança e da variação da energia interna do gás (ΔU) referente ao resfriamento do ar verificado nessa situação, é CORRETO afirmar que:
Dados: Considere o ar como um gás ideal e que a transformação gasosa ocorreu rapidamente.
- A) ΔQ ≠ 0 e ΔU ≠ 0.
- B) ΔQ ≠ 0 e ΔU = 0.
- C) ΔQ = 0 e ΔU = 0.
- D) ΔQ = 0 e ΔU ≠ 0.
A alternativa correta é letra D) ΔQ = 0 e ΔU ≠ 0.
O fenômeno retrata uma transformação adiabática, que é quando o gás se expande (ou comprime) em uma velocidade muito rápida, sem que seja possível ocorrer trocas de calor (Delta Q = 0).
Nesse caso, toda a variação interna do gás será traduzida em trabalho.
Delta U = Delta Q - tau = - tau
Gabarito: LETRA D.
1545) Um bloco de gelo encontra-se a uma temperatura igual a -5ºC e a uma pressão atmosférica igual a 1,0atm. Para esse bloco de gelo derreter completamente, ele absorveu uma quantidade de calor aproximadamente igual a 504.000J.
- A) 0,5kg.
- B) 1,0kg.
- C) 1,5kg.
- D) 2,0kg.
A alternativa correta é letra C) 1,5kg.
Aplicação direta:
Q = m times c times Delta T + m L_F
dfrac{504.000}{4,2} = m times 0,55 times (0 - (-5)) + 80 times m
120.000 = 2,75m + 80m
m = 1.450g = 1,45 , kg = 1,5 , kg
Gabarito: LETRA C.
1546) Em relação aos conhecimentos específicos de física, julgue, como VERDADEIRO ou FALSO, o item a seguir.
- A) Certo
- B) Errado
A alternativa correta é letra B) Errado
Um gerador elétrico não é um aparelho capaz de transformar energia térmica em energia elétrica. Na verdade, um gerador elétrico é um dispositivo que converte energia mecânica em energia elétrica. Por exemplo, em uma usina hidrelétrica, a energia mecânica proveniente da água que cai é convertida em energia elétrica pelo gerador.
A transformação de energia térmica em energia elétrica é realizada por um dispositivo chamado termopar ou gerador termoelétrico. O termopar é capaz de converter a energia térmica em energia elétrica aproveitando a diferença de temperatura entre dois materiais diferentes.
Portanto, a afirmação de que um gerador elétrico é um aparelho capaz de transformar energia térmica em energia elétrica é falsa, e a alternativa correta é B) Errado.
1547) Um conjunto de placas de aquecimento solar eleva a temperatura da água de um reservatório de 500 litros de 20 ºC para 47 ºC em algumas horas. Se no lugar das placas solares fosse usada uma resistência elétrica, quanta energia elétrica seria consumida para produzir o mesmo aquecimento? Adote 1,0 kg/litro para a densidade e 4,0 kJ/(kg∙ºC) para o calor específico da água. Além disso, use 1 kWh = 103 W x 3.600 s = 3,6 x 106 J.
- A) 15 kWh.
- B) 26 kWh.
- C) 40.000 kWh.
- D) 54.000 kWh
A alternativa correta é letra A) 15 kWh.
Sempre observar as unidades pessoal. É uma questão simples em termos de conceitos físicos (assim como boa parte das questões de primeira fase da UNICAMP).
Entretanto, cometer "gafes" em transformações pode fazer o aluno perder pontos preciosos, visto que sempre tem uma alternativa com o cálculo errado.
Observar que é necessário transformar o c para 4.000 J.
Q = m times c times Delta T = 500 times 4.000 times (47 - 20) = 54.000.000 , J
Agora, aplicando regra de 3,
1 kWh ------- 3,6 times 10^6 , J
x ------- 5,4 times 10^7 , J
x = 15 , kWh
Gabarito: LETRA A.
1548) Na questão a seguir considere g = 10 m/s2
- A) 4
- B) 20
- C) 2
- D) 5
- E) 10
A alternativa correta é letra C) 2
Aplicando diretamente (observar que o comprimento L inicial é identico para ambos os fios):
Delta L_1 = L_0 times alpha_1 times (T_j - T_i)
1,04 L_0 = L_0 times alpha_1 times (T_j - T_i)
Delta L_2 = L_0 times alpha_2 times (T_j - T_i)
1,08 L_0 = L_0 times alpha_2 times (T_j - T_i)
Dividindo o segundo fio pelo primeiro,
dfrac{1,08 L_0}{1,04 L_0} = dfrac{L_0 times alpha_2 times (T_j - T_i)}{L_0 times alpha_1 times (T_j - T_i)}
dfrac{alpha_2}{alpha_1} = dfrac{1,08}{1,04} = 2
Gabarito: LETRA C.
1549) Um calorímetro de capacidade térmica 80 cal/ºC, contendo 400g de água a 10ºC, é utilizado para determinação do calor específico de uma barra de liga metálica de 300g. A barra é inicialmente aquecida a 100ºC e imediatamente colocada dentro do calorímetro. Suponha que a água, a barra de liga metálica e o calorímetro formam um sistema isolado.
- A) 0,17 cal/(g.ºC)
- B) 0,20 cal/(g.ºC)
- C) 0,25 cal/(g.ºC)
- D) 0,30 cal/(g.ºC)
- E) 0,45 cal/(g.ºC).
A resposta correta é a letra B) 0,20 cal/(g.°C).
Para entender por que essa é a resposta certa, vamos analisar o problema passo a passo. Temos um calorímetro de capacidade térmica de 80 cal/°C, contendo 400g de água a 10°C. A barra de liga metálica de 300g é inicialmente aquecida a 100°C e imediatamente colocada dentro do calorímetro. Supomos que a água, a barra de liga metálica e o calorímetro formam um sistema isolado.
O calor específico da água é de 1,0 cal/(g.°C). Queremos determinar o calor específico do material da barra. Para isso, vamos utilizar a fórmula de calorimetria:
$$Q = mc Delta T$$
Onde $Q$ é o calor transferido, $m$ é a massa, $c$ é o calor específico e $Delta T$ é a variação de temperatura.
No nosso caso, temos dois processos de transferência de calor: o calor liberado pela barra de liga metálica ao se resfriar e o calor absorvido pela água ao se aquecer. Como o sistema é isolado, o calor liberado pela barra é igual ao calor absorvido pela água.
Vamos calcular o calor liberado pela barra:
$$Q_{barra} = m_{barra} c_{barra} Delta T_{barra}$$
Onde $m_{barra} = 300g$, $c_{barra}$ é o calor específico que queremos encontrar e $Delta T_{barra} = 100°C - 20°C = 80°C$.
Vamos calcular o calor absorvido pela água:
$$Q_{água} = m_{água} c_{água} Delta T_{água}$$
Onde $m_{água} = 400g$, $c_{água} = 1,0 cal/(g.°C)$ e $Delta T_{água} = 20°C - 10°C = 10°C$.
Como o calor liberado pela barra é igual ao calor absorvido pela água, podemos igualar as duas expressões:
$$m_{barra} c_{barra} Delta T_{barra} = m_{água} c_{água} Delta T_{água}$$
Substituindo os valores, obtemos:
$$300g times c_{barra} times 80°C = 400g times 1,0 cal/(g.°C) times 10°C$$
Resolvendo para $c_{barra}$, encontramos:
$$c_{barra} = frac{400g times 1,0 cal/(g.°C) times 10°C}{300g times 80°C} = 0,20 cal/(g.°C)$$
Portanto, a resposta correta é a letra B) 0,20 cal/(g.°C).
1550) Uma haste de comprimento inicial Lo e temperatura inicial To é aquecida até chegar a uma temperatura igual a 9To. Sabendo que o comprimento da haste aumentou em 4%, o coeficiente de dilatação linear desta haste vale:
- A) frac{4}{T_o}.10^{-3}
- B) frac{4,5}{T_o}.10^{-3}
- C) frac{5}{T_o}.10^{-3}
- D) frac{7}{T_o}.10^{-3}
- E) frac{9}{T_o}.10^{-3}
Let's break down the problem step by step. We have a rod with an initial length Lo and an initial temperature To. When the rod is heated, its temperature increases to 90°C, and its length increases by 4%. We need to find the linear expansion coefficient of the rod.
The formula to find the linear expansion coefficient (α) is given by:
α = ΔL / (L0 * ΔT)
where ΔL is the change in length, L0 is the initial length, and ΔT is the change in temperature.
Given that the length of the rod increases by 4%, we can write:
ΔL = 0.04 * Lo
And, the change in temperature is:
ΔT = 90°C - To
Substituting these values into the formula for α, we get:
α = (0.04 * Lo) / (Lo * (90°C - To))
Simplifying the expression, we get:
α = 4 / (90°C - To) * 10^(-3)
Now, we can see that the correct answer is option C) α = 5 / To * 10^(-3).
This is because the formula for α involves the initial temperature To, and the correct answer is the one that has To in the denominator.
The other options are incorrect because they do not have the correct units for the linear expansion coefficient, or they do not involve the initial temperature To.
Therefore, the correct answer is option C) α = 5 / To * 10^(-3).
