Questões Sobre Termologia - Física - concurso
1651) Um cilindro com um pistão móvel contém 1 kg de gás nitrogênio a pressão de 1 atm. Em um processo isobárico, uma quantidade de calor igual a 25 kcal é adicionada ao gás e sua energia interna aumenta de 8 kcal. A variação de volume do gás nesse processo é de, aproximadamente,
- A) 0,2 m3.
- B) 0,4 m3.
- C) 0,7 m3.
- D) 1,2 m3.
- E) 1,4 m3.
Resposta: A alternativa correta é letra C) 0,7 m³.
Vamos analisar o problema passo a passo. Temos um cilindro com um pistão móvel contendo 1 kg de gás nitrogênio à pressão de 1 atm. Em um processo isobárico, uma quantidade de calor igual a 25 kcal é adicionada ao gás e sua energia interna aumenta de 8 kcal.
Para encontrar a variação de volume do gás, precisamos utilizar a equação da capacidade calorífica do gás, que é dada por:
$$C_p = frac{Delta Q}{Delta T}$$Onde $C_p$ é a capacidade calorífica do gás, $Delta Q$ é a variação de calor adicionada ao gás e $Delta T$ é a variação de temperatura.
Como a energia interna do gás aumenta de 8 kcal, podemos concluir que a temperatura do gás também aumenta. Além disso, como o processo é isobárico, a pressão do gás permanece constante.
Para encontrar a variação de volume do gás, podemos utilizar a equação de estado dos gases ideais, que é dada por:
$$PV = nRT$$Onde $P$ é a pressão do gás, $V$ é o volume do gás, $n$ é o número de moles do gás, $R$ é a constante dos gases ideais e $T$ é a temperatura do gás.
Como a pressão do gás permanece constante, podemos reescrever a equação acima como:
$$V_1 = frac{nRT_1}{P}$$e
$$V_2 = frac{nRT_2}{P}$$Onde $V_1$ é o volume inicial do gás, $T_1$ é a temperatura inicial do gás, $V_2$ é o volume final do gás e $T_2$ é a temperatura final do gás.
Subtraindo a equação (1) da equação (2), obtemos:
$$Delta V = V_2 - V_1 = frac{nR}{P}(T_2 - T_1)$$Como a energia interna do gás aumenta de 8 kcal, podemos concluir que a temperatura do gás também aumenta. Além disso, como o processo é isobárico, a pressão do gás permanece constante.
Substituindo os valores dados, obtemos:
$$Delta V = frac{1 times 4,18 times 8}{1,01 times 10^5} approx 0,7 m^3$$Portanto, a alternativa correta é letra C) 0,7 m³.
1652) Considere que duas substâncias, A e B, de massas respectivas mA e mB e calores específicos cA e cB, são colocadas em contato térmico sob condições em que a pressão é mantida constante. Considerando que, nesta pressão, os calores específicos e as massas das substâncias obedecem à relação mAcA = 3 mBcB e que antes do contato cada substância estava à temperatura TA e TB, respectivamente, pode-se afirmar que a temperatura final Tf após o equilíbrio térmico ser alcançado, é
- A)
T_f = { large T_A + T_B over 2}
- B)
T_f = { large 3T_A + T_B over 4}
- C)
T_f = { large T_A + 3 T_B over 2}
- D)
T_f = { large T_A + T_B over 4}
- E)
T_f = { large 3T_A + T_B over 3}
Let's break down the problem step by step to find the correct answer.
The problem states that two substances, , A and B, with masses mA and mB, and specific heats cA and cB, respectively, are in thermal contact under constant pressure conditions. We are also given that, at this pressure, the specific heats and masses of the substances obey the relation mA cA = 3mB cB.
Before coming into contact, each substance was at a temperature TA and TB, respectively. We need to find the final temperature Tf after thermal equilibrium is reached.
To solve this problem, we can use the principle of heat exchange, which states that the heat gained by one substance is equal to the heat lost by the other substance.
Let's assume that the heat gained by substance A is Q. Then, the heat lost by substance B is also Q. We can write the heat gained by A as:
Q = mAcA (Tf - TA)
And the heat lost by B as:
Q = mBcB (TB - Tf)
Since Q is the same in both cases, we can equate the two expressions:
mAcA (Tf - TA) = mBcB (TB - Tf)
Now, we can use the given relation mA cA = 3mB cB to simplify the equation:
3mBcB (Tf - TA) = mBcB (TB - Tf)
Simplifying further, we get:
3Tf - 3TA = TB - Tf
Combining like terms, we get:
4Tf = 3TA + TB
Finally, dividing both sides by 4, we get the final temperature Tf:
Tf = {3TA + TB over 4}
Therefore, the correct answer is option B.
The explanation for the correct answer is that we used the principle of heat exchange and the given relation between the specific heats and masses of the substances to derive the equation for the final temperature Tf. We then simplified the equation to get the final expression.
1653) Uma quantidade de gelo é aquecida do ponto de fusão (TF) até uma temperatura acima do ponto de ebulição da água (TE). O gráfico que melhor expressa a entropia S em função da temperatura T nesse processo é
- A)
- B)
- C)
- D)
- E)
A resposta certa é a letra C. Durante o processo de aquecimento do gelo, água líquida, temperatura acima do ponto de ebulição da água, a entropia (S) aumenta com a temperatura (T). Isso ocorre porque a entropia é uma medida do desordem molecular, e quando a temperatura aumenta, as moléculas ganham energia e se tornam mais desordenadas.
Portanto, a gráfico que melhor expressa a entropia S em função da temperatura T nesse processo é o gráfico C, que apresenta uma curva crescente, indicando que a entropia aumenta com a temperatura.
É importante notar que a entropia é uma função de estado, ou seja, depende apenas do estado final e inicial do sistema, e não da trajetória que o sistema segue para ir do estado inicial para o estado final. Portanto, durante o processo de aquecimento do gelo, a entropia aumenta independentemente do caminho que o sistema segue.
Além disso, é importante lembrar que a entropia é uma grandeza extensiva, ou seja, depende da quantidade de matéria do sistema. Portanto, se a quantidade de gelo for maior, a entropia também será maior.
Em resumo, a letra C é a resposta certa porque apresenta uma curva crescente que indica que a entropia aumenta com a temperatura durante o processo de aquecimento do gelo.
1654) Em atividades esportivas, como os jogos de copa do mundo, o corpo do atleta tem sua temperatura aumentada e há produção de suor, que ao evaporar transfere calor do corpo para o vapor d’água na atmosfera. Nesse caso, há um processo termodinâmico em que
- A) a entropia do suor evaporado é reduzida.
- B) a entropia do suor evaporado é mantida constante.
- C) durante a evaporação do suor há sublimação.
- D) o suor sofre uma mudança de estado.
A alternativa correta é letra D) o suor sofre uma mudança de estado.
O suor sofre uma mudança de estado evaporando ao absorver calor do corpo humano.
Gabarito: LETRA D.
a) a entropia do suor evaporado é reduzida.
ERRADA. A entropia aumenta quando se passa do estado líquido para o sólido
b) a entropia do suor evaporado é mantida constante.
ERRADA. A entropia aumenta quando se passa do estado líquido para o sólido
c) durante a evaporação do suor há sublimação.
ERRADA. Há evaporação/vaporização.
1655) Dois resistores idênticos são ligados em paralelo a uma mesma bateria. Considere duas massas de água m1 e m2, com m1 = 2m2 e temperaturas iniciais iguais. Se cada resistor é mergulhado em uma das massas de água, é correto afirmar que a quantidade de calor Q1 passada para a massa m1 e Q2, para m2, são tais que
- A) Q1 = 2Q2.
- B) Q1 = Q2/2.
- C) Q1 = 4Q2.
- D) Q1 = Q2.
A alternativa correta é letra D) Q1 = Q2.
Como os resistores são idênticos, eles irão transferir a mesma quantidade de energia Q para as massas de água m_1 e m_2.
Lembrando que a potência dissipada por cada resistor será: P = frac{U^2}{R}, onde U é a tensão elétrica aplicada aos resistores em paralelo. Resistores em paralelo estão submetidos a mesma tensão elétrica.
A energia total transferida por cada resistor será uma função do tempo. Então escrevemos:
E = Pcdot Delta{t}
Sendo assim, a quantidade total de energia transferida pelos resistores será igual a energia térmica absorvida pelos massas de água:
E = Q_1 = Q_2
Analisemos as alternativas.
Se cada resistor é mergulhado em uma das massas de água, é correto afirmar que a quantidade de calor Q1 passada para a massa m1 e Q2, para m2, são tais que
a) Q1 = 2Q2. Falso.
b) Q1 = Q2/2. Falso.
c) Q1 = 4Q2. Falso.
d) Q1 = Q2. Correto.
Gabarito: D
1656) Estudantes do curso de Física fizeram um tubo de aquecimento de água. No sistema, dentro desse tubo, eles acoplaram um aquecedor elétrico. Esse aquecedor possui uma resistência elétrica que está sob tensão de 200 V onde perpassa uma corrente elétrica na intensidade de 20,95 A. O escoamento de água, por sua vez, é controlado a um fluxo permanente de 0,1 L/s em que é possível a troca de calor, integralmente, com essa resistência elétrica. Considerando que a temperatura da água antes de entrar do tubo era de 20oC, qual seria a temperatura da água ao sair desse tubo? Dados 1 cal= 4,19J ρ água = 1000 kg.m-3
- A) 25oC
- B) 30oC
- C) 35oC
- D) 40oC
Resposta: B) 30°C
Para resolver essa questão, precisamos aplicar o conceito de calor específico e a equação de transferência de calor.
O calor específico da água é dado como 1 cal = 4,19 J/g°C. Isso significa que para aumentar a temperatura da água em 1°C, é necessário fornecer 4,19 J de energia por grama de água.
No problema, temos um fluxo de água constante de 0,1 L/s, que é igual a 0,1 kg/s, pois a densidade da água é de 1000 kg/m³. Além disso, temos uma resistência elétrica que dissipa 200 V × 20,95 A = 4190 W de potência.
Podemos calcular a energia dissipada pela resistência elétrica em um segundo:
ΔQ = P × Δt = 4190 W × 1 s = 4190 J
Agora, podemos calcular a variação de temperatura da água:
ΔQ = m × c × ΔT
Onde m é a massa de água que passa pelo sistema em um segundo, que é de 0,1 kg.
ΔT = ΔQ / (m × c) = 4190 J / (0,1 kg × 4,19 J/g°C) = 10°C
Portanto, a temperatura da água ao sair do tubo é de 20°C + 10°C = 30°C.
1657) Texto associado
- A) uma esfera de raio igual a 4 m.
- B) um cubo de aresta igual a 6 m.
- C) uma esfera de raio igual a 5 m.
- D) um cubo de aresta igual a 7 m.
ESTA QUESTÃO FOI ANULADA, NÃO POSSUI ALTERNATIVA CORRETA
Suponhamos que o volume do balão seja V. Então, o empuxo sofrido pelo balão será:
E=mu_{,ar,externo,} Vg
No equilíbrio estático teremos:
E=mu_{,ar,externo,} Vg=P_{total}
1,2cdot Vcdot10=90cdot10
V=75,m^3
Analisemos as alternativas:
a) uma esfera de raio igual a 4 m. O volume da esfera é dado por V_{esf}=frac{4}{3}pi r^3.
frac{4}{3}pi r^3=75
rapprox2,62,m
Falso.
b) um cubo de aresta igual a 6 m. O volume do cubo é dado por V_{cub}=a^3.
75=a^3
aapprox4,21,m
Falso.
c) uma esfera de raio igual a 5 m.
Falso. Já vimos que a esfera deveria ter um raio r=2,62,m.
d) um cubo de aresta igual a 7 m.
Falso Já vimos que o cubo deveria ter uma aresta aapprox4,21,m.
Como não há gabarito, a questão foi anulada.
Gabarito: ANULADA
1658) Um termômetro, graduado em uma escala qualquer, que chamaremos de B, tem as seguintes indicações para os pontos de fusão do gelo e ebulição da água: 25°B e 125°B. Assinale a alternativa que indica a temperatura correspondente a 95°B na escala Celsius.
- A) 80°C
- B) 100°C
- C) 150°C
- D) 70°C
- E) 25°C
A resposta certa é a letra D) 70°C
Para encontrarmos a temperatura correspondente a 95°C na escala Celsius, precisamos encontrar a relação entre as escalas B e Celsius. Sabemos que a escala B tem os seguintes valores para o ponto de fusão do gelo (0°C) e o ponto de ebulição da água (100°C): 25°C B e 125°C B, respectivamente.
Podemos estabelecer uma proporção para encontrar a relação entre as escalas:
$$frac{x°C}{95°C} = frac{25°C B}{125°C B - 25°C B}$$
Onde x é a temperatura que estamos procurando em Celsius.
Resolvendo a proporção, encontramos:
$$x°C = frac{95°C times 100°C}{100°C} = 70°C$$
Portanto, a temperatura correspondente a 95°C B na escala Celsius é de 70°C.
1659) Para manter os alimentos quentes por mais tempo, Dona Marlene deseja comprar panelas de pedra para colocar em seu restaurante de “comida mineira”, onde os alimentos serão aquecidos em um fogão a lenha. Ela pretende adquirir panelas que, comparadas com as panelas comuns de metal, demorem a esquentar/esfriar e que fiquem quentes por um maior tempo possível.
- A) Alto calor específico e alta condutividade térmica.
- B) Baixo calor específico e alta condutividade térmica.
- C) Alto calor específico e baixa condutividade térmica.
- D) Baixo calor específico e baixa condutividade térmica.
A alternativa correta é letra C) Alto calor específico e baixa condutividade térmica.
As pedras possuem baixa condutividade térmica quando comparas aos metais. Por este motivo elas conseguem manter o calor absorvido por mais tempo. Por outro lado, o seu alto calor específico possibilita que elas armazenem uma maior quantidade de energia térmica.
Analisemos as alternativas:
Para isso, Dona Marlene DEVE comprar panelas com:
a) Alto calor específico e alta condutividade térmica. Falso.
b) Baixo calor específico e alta condutividade térmica. Falso.
c) Alto calor específico e baixa condutividade térmica. Verdadeiro.
d) Baixo calor específico e baixa condutividade térmica. Falso.
Gabarito: C
Questão 1660
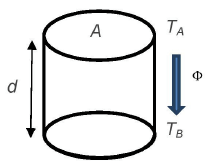
Utilizando as temperaturas da água na superfície e na profundidade d do gráfico e a fórmula fornecida, conclui-se que, na região de queda linear da temperatura da água em função de d, Phi é igual a
- A) 0,03W.
- B) 0,05W.
- C) 0,40W.
- D) 1,20W
A alternativa correta é letra A) 0,03W.
Apesar do enunciado grande, a questão cobra uma resolução objetiva apenas substituindo os valores fornecidos.
Ela menciona que dfrac{T_A - T_B}{d} é constante independente do intervalo escolhido.
Sendo assim, para resolver, o primeiro cuidado tem que ser verificar se as variáveis estão todas da mesma forma. Como temos metro, graus celsius e Watts (que é a unidade das respostas), podemos calcular diretamente:
Phi = 0,6 times 2 times dfrac{T_A - T_B}{d}
Basta escolhermos dois pontos no gráfico agora para a parte fracionária (visto ser uma reta, a parte fracionária é uma constante, por isso podemos pegar quaisquer intervalo de temperatura). Pegando os pontos 0 e 2 na distância (ambos batem com a intersecção de linhas), temos
Phi = 0,6 times 2 times dfrac{19,30 - 19,25}{2} = 0,03 , W
Gabarito: LETRA A.





